Clear Sky Science · sv
Tumör-suppressorfunktion för SHMT i en Drosophila RasV12DlgRNAi-modell: DNA-skador och synergistisk gen-näringsinteraktion med PLP
Varför den här fruktflugehistorien spelar roll
Cancer omprogrammerar ofta hur celler använder näringsämnen, men samma molekyler som driver tumörer kan ibland också hålla dem tillbaka. I denna studie använde forskare fruktflugor för att kartlägga hur ett enda enzym som sköter vitamin‑kopplad kemi i cellerna kan fungera som en broms för cancer. De visar att när detta enzym sviktar blir DNA instabilt, tumörer växer mer aggressivt, och ett vanligt vitamin samt en antioxidant kan skifta balansen mellan tumörtillväxt och celldöd.
Cellens lilla koldioxid‑trafiknav
Inuti våra celler stödjer ett nätverk som kallas enkolsmetabolism tyst livet genom att mata byggstenar till DNA‑produktion och kemiska märken som styr genaktivitet. I centrum för detta nätverk finns ett enzym kallat SHMT, som arbetar tillsammans med vitamin B6 i dess aktiva form. SHMT hjälper till att omvandla en aminosyra till en annan samtidigt som det levererar små kolenheter som behövs för att bygga DNA. I många mänskliga cancerformer finns varianter av detta enzym på höga nivåer och anses kunna stödja tumörtillväxt. Men i vissa cancerformer kopplas låga nivåer av en form av SHMT till sämre prognos, vilket antyder att enzymet också kan fungera som en tumörsuppressor beroende på sammanhang.
Använda fruktflugor för att se tumörer växa
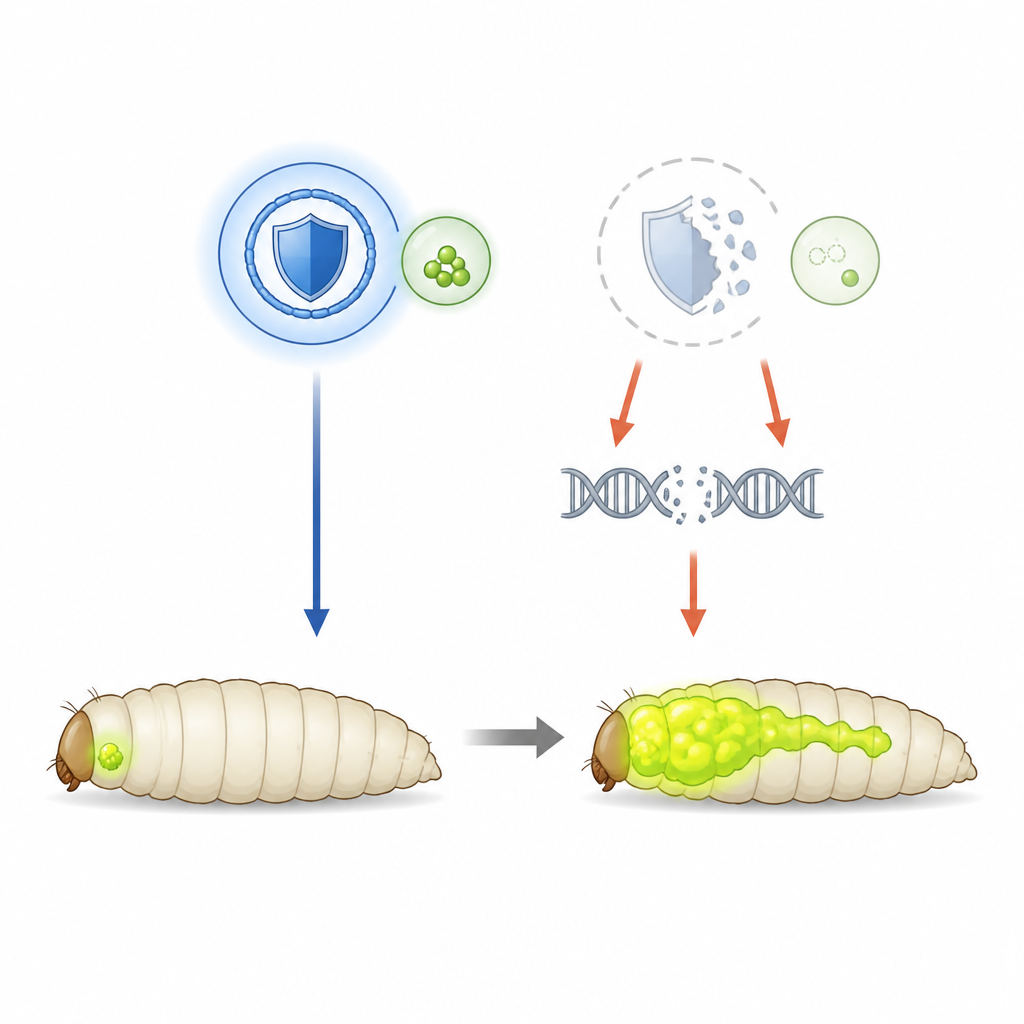
För att reda ut SHMT:s skyddande roll vände sig teamet till fruktflugor konstruerade för att utveckla aggressiva ögontumörer drivna av ett överaktivt Ras‑gen och förlust av en gen för cellpolaritetsreglering. Dessa tumörer lyser grönt, vilket tillåter forskarna att följa deras storlek och spridning i larvstadiet. I detta system är SHMT‑nivåerna normala, så forskarna kunde avsiktligt sänka enzymet med hjälp av RNA‑interferens. När SHMT‑aktiviteten reducerades växte primärtumörerna och invaderade flugans nervsystem oftare, vilket visar att SHMT här fungerar som en broms för cancerprogression snarare än som bränsle.
DNA‑byggstenar, skador och oxidativ stress
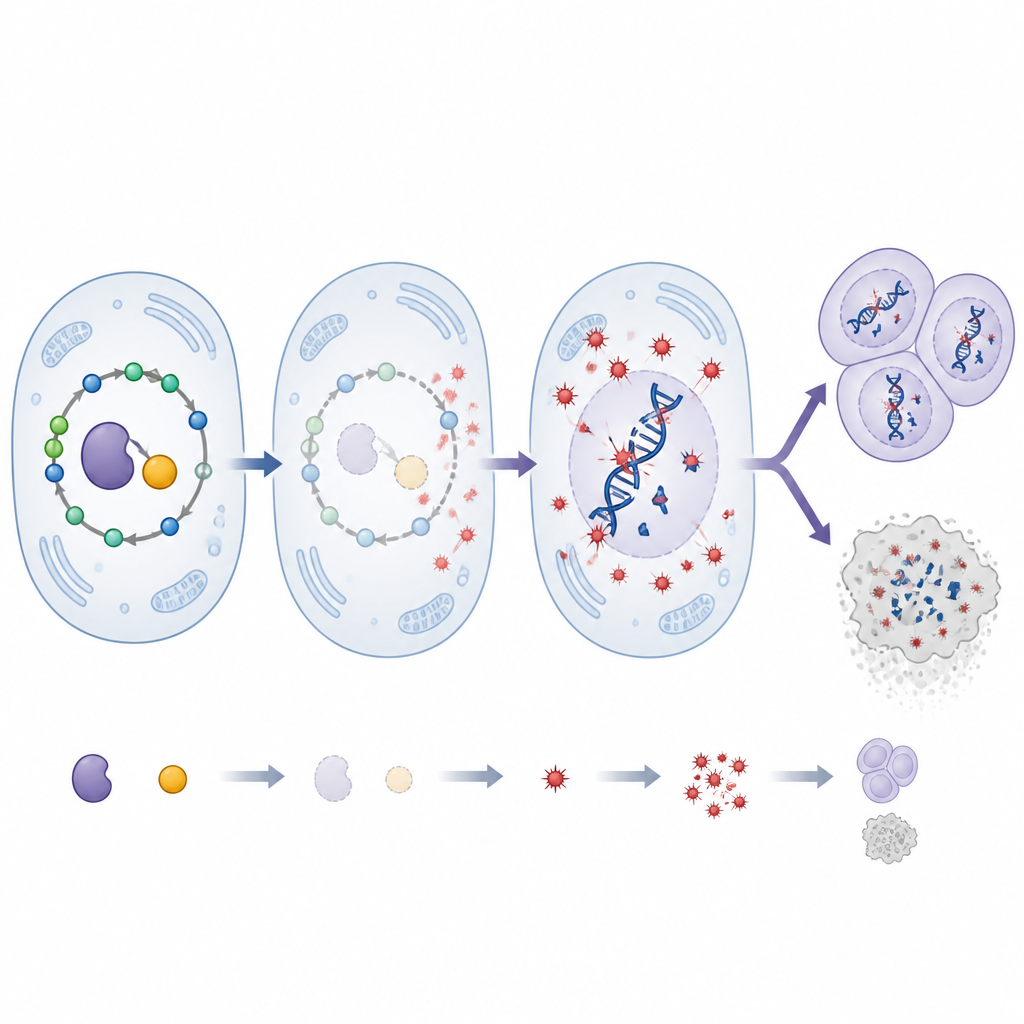
SHMT matar normalt en väg som producerar tymidylat, en nödvändig DNA‑byggsten. När SHMT tystades upphörde tillförseln av denna byggsten. Resultatet blev en våg av dubbelsträngsbrott i DNA och synligt sönderslagna kromosomer i tumörcellerna, klara tecken på genominstabilitet. Dessa celler blev också ovanligt känsliga för DNA‑skadande röntgenstrålning och för läkemedel som saktar ner DNA‑kopiering, och de hade svårt att reparera brott när de väl uppstått. Samtidigt ökade nivåerna av reaktiva syreföreningar kraftigt. Behandling av larver med tymidylat återställde DNA‑byggstenarna och minskade både DNA‑skador och oxidativ stress, medan en antioxidant, N‑acetylcystein, sänkte nivåerna av reaktiva syreföreningar, kromosomskador och tumörtillväxt. Tillsammans pekar dessa fynd på en händelsekedja där bristande tillgång på DNA‑byggstenar ökar oxidativ stress, som i sin tur angriper DNA och underlättar tumörutveckling.
En vitaminkofaktor tippar vågskålen
SHMT är beroende av pyridoxal‑5′‑fosfat, den aktiva formen av vitamin B6, för att fungera. Forskarna sänkte detta vitamin i flugor genom en dietär blockerare och undersökte hur det samverkade med reducerad SHMT. Att minska SHMT ensamt påskyndade tumörtillväxten och ökade DNA‑skador. Att sänka vitamin B6 ensam gav mildare effekter. Slående nog orsakade kombinationen av båda förändringarna en dramatisk ökning av oxidativ stress och DNA‑brott, långt mer än någon av förändringarna för sig. Detta gav emellertid inte proportionellt mycket större tumörer. Istället slog många tumörceller på ett nyckelenzym för celldöd och genomgick apoptos, vilket tyder på att mycket skadade celler eliminerades. Behandling med hög dos antioxidant minskade återigen oxidativ stress, DNA‑skador och tumörstorlek, vilket understryker de reaktiva syreföreningarnas centrala roll i dessa utfall.
Vad detta betyder för cancer och kost
Denna studie visar att SHMT i ett levande djur kan fungera som tumörsuppressor genom att hjälpa till att bevara DNA‑stabilitet och hålla oxidativ stress i schack. När SHMT‑aktiviteten sjunker, särskilt tillsammans med minskat vitamin B6, ackumulerar tumörceller DNA‑skador som antingen kan driva cancerprogression eller, om skadan blir för omfattande, utlösa deras egen död. Studien avslöjar också en direkt gen–näringsinteraktion mellan SHMT och vitamin B6 som formar hur tumörer växer. Även om dessa fynd kommer från fruktflugor, speglar de mönster som setts i vissa mänskliga cancerformer och tyder på att riktade insatser mot SHMT, dess vitaminkofaktor och reaktiva syreföreningar tillsammans kan informera framtida strategier för att kontrollera tumörtillväxt utan att förlita sig enbart på att döda delande celler.
Citering: Angioli, C., Ferriero, A., Pilesi, E. et al. Tumor suppressor function of SHMT in a Drosophila RasV12DlgRNAi model: DNA damage and synergistic gene-nutrient interaction with PLP. Cell Death Dis 17, 427 (2026). https://doi.org/10.1038/s41419-026-08602-7
Nyckelord: cancermetabolism, DNA‑skador, reaktiva syreföreningar, vitamin B6, Drosophila‑tumörer