Clear Sky Science · fr
Fonction suppresseur de tumeur de la SHMT dans un modèle Drosophila RasV12DlgRNAi : dommages à l’ADN et interaction synergiques gène-nutriment avec le PLP
Pourquoi cette histoire de mouche du vinaigre est importante
Le cancer réorganise souvent l’usage des nutriments par les cellules, mais les mêmes molécules qui alimentent les tumeurs peuvent parfois les freiner. Dans cette étude, des chercheurs ont utilisé la mouche du vinaigre pour révéler comment une enzyme unique impliquée dans la chimie liée aux vitamines à l’intérieur des cellules peut jouer le rôle de frein sur le cancer. Ils montrent que lorsque cette enzyme défaillit, l’ADN devient instable, les tumeurs croissent plus agressivement, et une vitamine commune ainsi qu’un antioxydant peuvent faire basculer l’équilibre entre croissance tumorale et mort cellulaire.
Le minuscule carrefour carboné de la cellule
À l’intérieur de nos cellules, un réseau connu sous le nom de métabolisme du carbone unitaire soutient discrètement la vie en fournissant des éléments de base à la production d’ADN et des groupements chimiques qui contrôlent l’activité des gènes. Au centre de ce réseau se trouve une enzyme appelée SHMT, qui travaille de concert avec la vitamine B6 sous sa forme active. La SHMT aide à convertir un acide aminé en un autre tout en transférant de petits unités carbonées nécessaires à la synthèse de l’ADN. Dans de nombreux cancers humains, des versions de cette enzyme sont présentes à des niveaux élevés et sont supposées favoriser la croissance tumorale. Pourtant, dans certains cancers, de faibles niveaux d’une forme de SHMT sont associés à de moins bons pronostics, ce qui suggère que l’enzyme peut aussi agir comme suppresseur de tumeur selon le contexte.
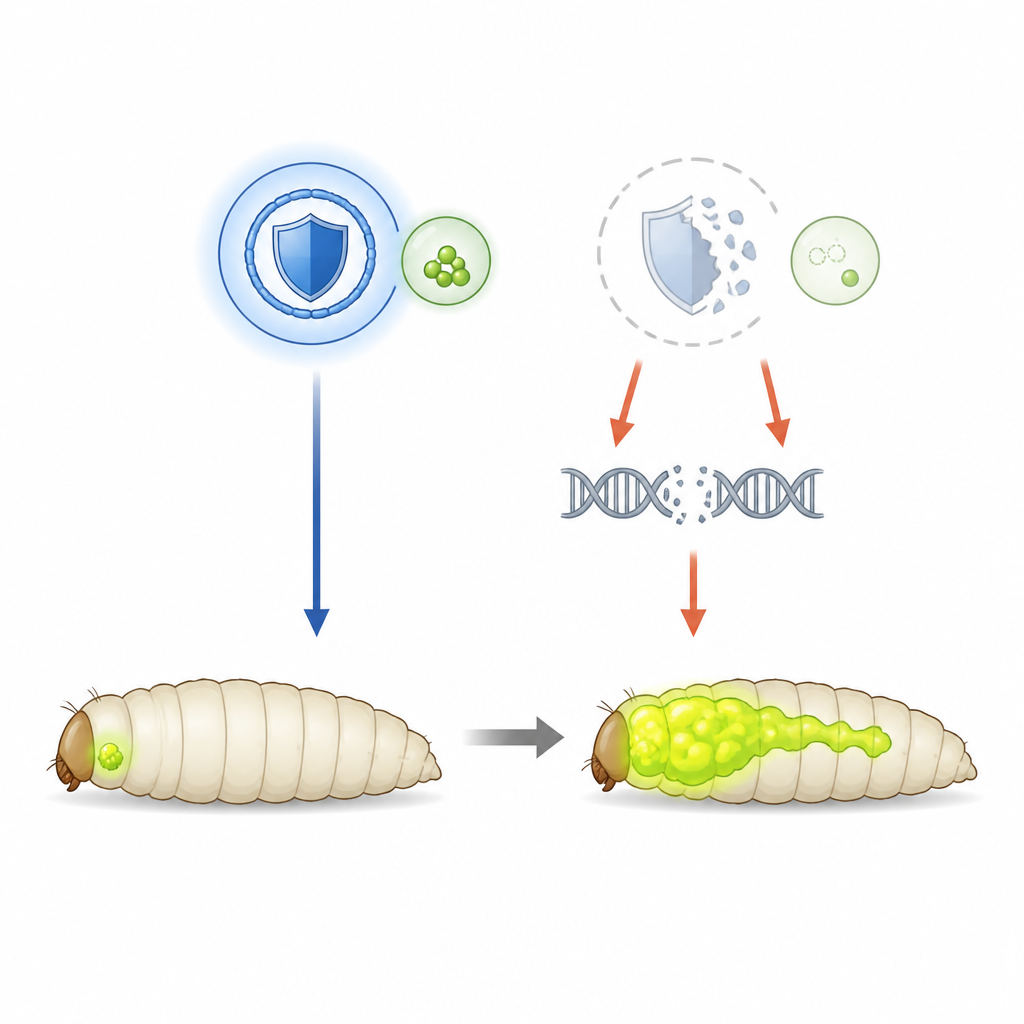
Utiliser la mouche pour observer la croissance tumorale
Pour démêler le rôle protecteur de la SHMT, l’équipe s’est tournée vers des mouches du vinaigre génétiquement modifiées pour développer des tumeurs oculaires agressives provoquées par un gène Ras hyperactif et la perte d’un gène de polarité cellulaire. Ces tumeurs brillent en vert, permettant aux scientifiques de suivre leur taille et leur extension chez la larve. Dans ce contexte, les niveaux de SHMT sont normaux, si bien que les chercheurs ont pu réduire délibérément l’enzyme par interférence ARN. Lorsque l’activité de la SHMT a été diminuée, les tumeurs primaires ont grossi et ont envahi le système nerveux de la mouche plus fréquemment, montrant qu’ici la SHMT agit comme un frein à la progression tumorale plutôt que comme un carburant.
Blocs de construction de l’ADN, dommages et stress oxydatif
La SHMT alimente normalement une voie qui produit la thymidylate, un élément de base essentiel de l’ADN. Lorsque la SHMT a été silencée, l’approvisionnement en ce constituant a fléchi. Le résultat a été une augmentation des cassures double brin de l’ADN et des chromosomes visiblement fragmentés à l’intérieur des cellules tumorales, signes clairs d’instabilité du génome. Ces cellules sont également devenues exceptionnellement sensibles aux rayons X endommageant l’ADN et aux médicaments qui ralentissent la réplication de l’ADN, et elles peinaient à réparer les cassures une fois apparues. Parallèlement, les niveaux d’espèces réactives de l’oxygène, des molécules oxygénées nocives, ont fortement augmenté. Le traitement des larves par de la thymidylate a permis de restaurer les blocs de construction de l’ADN et de réduire à la fois les dommages à l’ADN et le stress oxydatif, tandis qu’un antioxydant, la N‑acétyl‑cystéine, a réduit les espèces réactives de l’oxygène, les dommages chromosomiques et la croissance tumorale. Ensemble, ces résultats suggèrent une chaîne d’événements dans laquelle une mauvaise disponibilité des blocs de construction de l’ADN accroît le stress oxydatif, qui attaque ensuite l’ADN et favorise l’avancée tumorale.
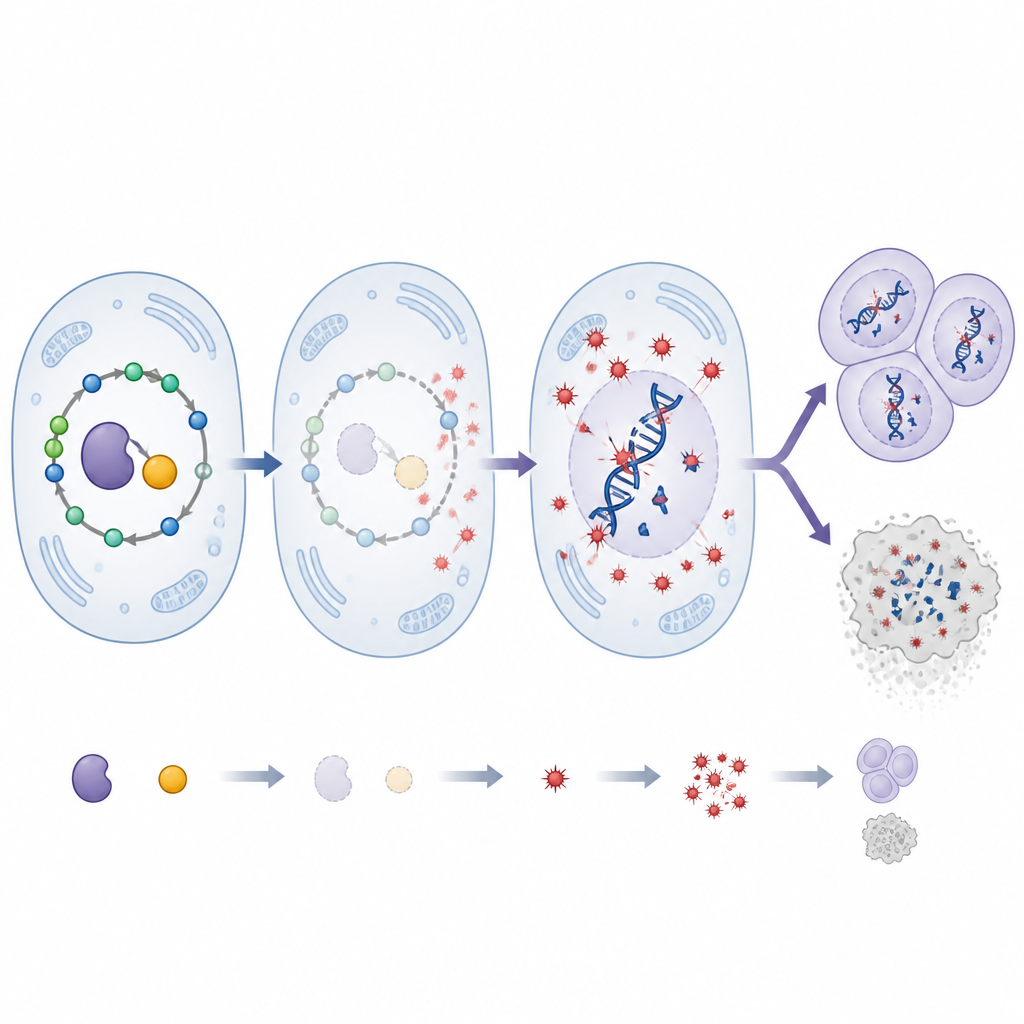
Un cofacteur vitaminique fait pencher la balance
La SHMT dépend du pyridoxal 5′‑phosphate, la forme active de la vitamine B6, pour fonctionner. Les chercheurs ont réduit cette vitamine chez les mouches en utilisant un bloqueur alimentaire et ont étudié son interaction avec la réduction de la SHMT. Réduire la SHMT seule a accéléré la croissance tumorale et augmenté les dommages à l’ADN. La diminution de la vitamine B6 seule a eu des effets plus modérés. De manière frappante, la combinaison des deux altérations a provoqué une flambée spectaculaire du stress oxydatif et des cassures de l’ADN, bien supérieure à celle observée avec chaque perturbation prise isolément. Pourtant, cela n’a pas produit des tumeurs proportionnellement plus volumineuses. Au contraire, de nombreuses cellules tumorales ont activé une enzyme clé de mort cellulaire et sont entrées en apoptose, suggérant que les cellules extrêmement endommagées étaient éliminées. Un traitement antioxydant à forte dose a de nouveau réduit le stress oxydatif, les dommages à l’ADN et la taille tumorale, soulignant le rôle central des espèces réactives de l’oxygène dans ces phénomènes.
Ce que cela signifie pour le cancer et l’alimentation
Ce travail montre que, chez un animal vivant, la SHMT peut agir comme suppresseur de tumeur en aidant à maintenir la stabilité de l’ADN et à contenir le stress oxydatif. Lorsque l’activité de la SHMT diminue, surtout en association avec une réduction de la vitamine B6, les cellules tumorales accumulent des dommages à l’ADN qui peuvent soit alimenter la progression du cancer, soit, si la détérioration est trop importante, déclencher leur propre mort. L’étude révèle également une interaction directe gène–nutriment entre la SHMT et la vitamine B6 qui façonne la croissance tumorale. Bien que ces conclusions proviennent de mouches du vinaigre, elles reflètent des schémas observés dans certains cancers humains et suggèrent que cibler simultanément la SHMT, son cofacteur vitaminique et les espèces réactives de l’oxygène pourrait éclairer des stratégies futures pour contrôler la croissance tumorale sans se limiter à tuer les cellules en division.
Citation: Angioli, C., Ferriero, A., Pilesi, E. et al. Tumor suppressor function of SHMT in a Drosophila RasV12DlgRNAi model: DNA damage and synergistic gene-nutrient interaction with PLP. Cell Death Dis 17, 427 (2026). https://doi.org/10.1038/s41419-026-08602-7
Mots-clés: métabolisme du cancer, dommages à l’ADN, espèces réactives de l’oxygène, vitamine B6, tumeurs de Drosophila