Clear Sky Science · es
Función supresora de tumores de SHMT en un modelo Drosophila RasV12DlgRNAi: daño en el ADN e interacción sinérgica gen-nutriente con PLP
Por qué importa esta historia de la mosca de la fruta
El cáncer a menudo reconfigura la forma en que las células usan los nutrientes, pero las mismas moléculas que alimentan a los tumores a veces pueden frenarlos. En este estudio, los investigadores usaron moscas de la fruta para desentrañar cómo una única enzima que maneja química ligada a vitaminas dentro de las células puede actuar como freno del cáncer. Demuestran que cuando dicha enzima falla, el ADN se vuelve inestable, los tumores crecen con más agresividad y una vitamina común y un antioxidante pueden inclinar la balanza entre el crecimiento tumoral y la muerte celular.
El pequeño centro de tráfico de carbonos de la célula
Dentro de nuestras células, una red conocida como metabolismo de un carbono sostiene discretamente la vida al proporcionar bloques de construcción para la producción de ADN y etiquetas químicas que controlan la actividad génica. En el centro de esta red se encuentra una enzima llamada SHMT, que trabaja junto a la vitamina B6 en su forma activa. SHMT ayuda a convertir un aminoácido en otro mientras transfiere pequeñas unidades de carbono necesarias para fabricar ADN. En muchos cánceres humanos, versiones de esta enzima se encuentran en niveles elevados y se piensa que favorecen el crecimiento tumoral. Sin embargo, en algunos cánceres, niveles bajos de una forma de SHMT se asocian con peores resultados, lo que sugiere que la enzima también puede actuar como supresora tumoral, según el contexto.
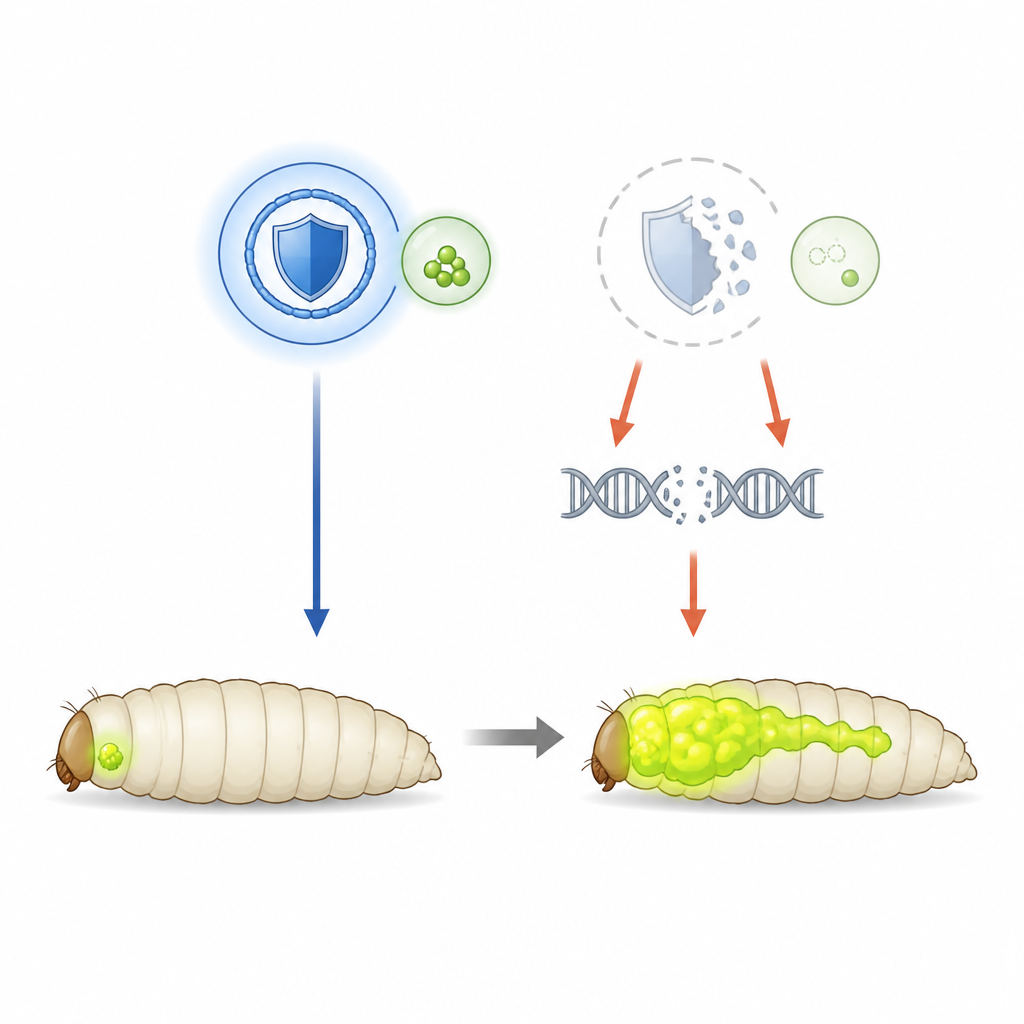
Usar moscas de la fruta para observar crecimiento tumoral
Para desenmarañar el papel protector de SHMT, el equipo recurrió a moscas de la fruta diseñadas para desarrollar tumores oculares agresivos impulsados por un gen Ras hiperactivo y la pérdida de un gen de polaridad celular. Estos tumores brillan en verde, lo que permite a los científicos seguir su tamaño y diseminación en la larva. En este contexto, los niveles de SHMT son normales, por lo que los investigadores pudieron reducir deliberadamente la enzima mediante interferencia de ARN. Cuando la actividad de SHMT se redujo, los tumores primarios crecieron más y penetraron con mayor frecuencia en el sistema nervioso de la mosca, mostrando que, en este caso, SHMT actúa como freno de la progresión tumoral en lugar de como combustible.
Bloques de construcción del ADN, daño y estrés oxidativo
SHMT alimenta normalmente una vía que produce timidilato, un bloque de construcción esencial del ADN. Cuando SHMT se silenció, el suministro de este componente falló. El resultado fue un aumento de roturas de doble cadena del ADN y cromosomas visiblemente fragmentados dentro de las células tumorales, signos claros de inestabilidad genómica. Estas células también se volvieron inusualmente sensibles a rayos X que dañan el ADN y a fármacos que ralentizan la copia del ADN, y tuvieron dificultades para reparar las roturas una vez que ocurrían. Al mismo tiempo, los niveles de especies reactivas de oxígeno, moléculas nocivas que contienen oxígeno, aumentaron drásticamente. Tratar las larvas con timidilato restauró los bloques de construcción del ADN y redujo tanto el daño en el ADN como el estrés oxidativo, mientras que un antioxidante, N-acetilcisteína, disminuyó las especies reactivas de oxígeno, el daño cromosómico y el crecimiento tumoral. En conjunto, estos hallazgos apuntan a una cadena de acontecimientos en la que el déficit de bloques de construcción del ADN aumenta el estrés oxidativo, que a su vez ataca el ADN y facilita el avance tumoral.
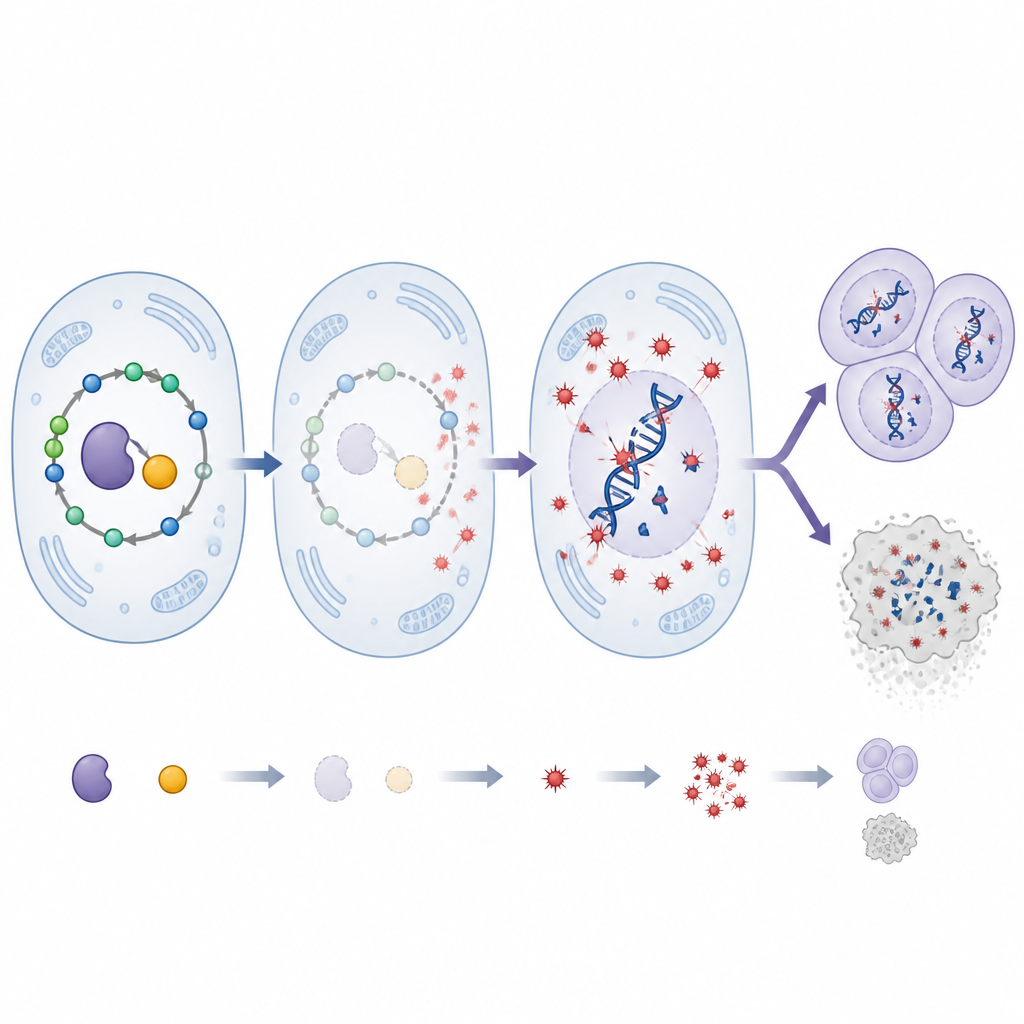
Un cofactor vitamínico inclina la balanza
SHMT depende de la piridoxal 5’-fosfato, la forma activa de la vitamina B6, para funcionar. Los investigadores redujeron esta vitamina en las moscas mediante un bloqueador dietético y estudiaron cómo interactuaba con la reducción de SHMT. Cortar solo SHMT aceleró el crecimiento tumoral y aumentó el daño en el ADN. Reducir la vitamina B6 por sí sola tuvo efectos más leves. De forma llamativa, la combinación de ambos cambios provocó un pico dramático en el estrés oxidativo y en las roturas del ADN, muy superior al de cada intervención por separado. No obstante, esto no produjo tumores proporcionalmente más grandes. En cambio, muchas células tumorales activaron una enzima clave de muerte celular y sufrieron apoptosis, lo que sugiere que las células extremadamente dañadas estaban siendo eliminadas. El tratamiento con altas dosis de antioxidante volvió a reducir el estrés oxidativo, el daño en el ADN y el tamaño tumoral, subrayando el papel central de las especies reactivas de oxígeno en estos resultados.
Qué significa esto para el cáncer y la dieta
Este trabajo muestra que, en un animal vivo, SHMT puede actuar como supresora tumoral ayudando a mantener la estabilidad del ADN y a controlar el estrés oxidativo. Cuando la actividad de SHMT cae, especialmente junto con la reducción de la vitamina B6, las células tumorales acumulan daño en el ADN que puede, o bien impulsar la progresión del cáncer o, si se lleva al extremo, desencadenar su propia muerte. El estudio también revela una interacción directa gen–nutriente entre SHMT y la vitamina B6 que moldea cómo crecen los tumores. Aunque estos hallazgos proceden de moscas de la fruta, reflejan patrones observados en algunos cánceres humanos y sugieren que apuntar conjuntamente a SHMT, su cofactor vitamínico y a las especies reactivas de oxígeno podría informar estrategias futuras para controlar el crecimiento tumoral sin depender únicamente de matar células en división.
Cita: Angioli, C., Ferriero, A., Pilesi, E. et al. Tumor suppressor function of SHMT in a Drosophila RasV12DlgRNAi model: DNA damage and synergistic gene-nutrient interaction with PLP. Cell Death Dis 17, 427 (2026). https://doi.org/10.1038/s41419-026-08602-7
Palabras clave: metabolismo del cáncer, daño en el ADN, especies reactivas de oxígeno, vitamina B6, tumores de Drosophila