Clear Sky Science · nl
Tumorremmende functie van SHMT in een Drosophila RasV12DlgRNAi-model: DNA-schade en synergistische gen–voedingsinteractie met PLP
Waarom dit fruitvliegverhaal ertoe doet
Kanker herprogrammeert vaak hoe cellen voedingsstoffen gebruiken, maar dezelfde moleculen die tumoren voeden kunnen ze soms ook remmen. In deze studie gebruikten onderzoekers fruitvliegjes om te onthullen hoe één enzym dat vitamine-gerelateerde chemie in cellen regelt als een rem op kanker kan werken. Ze tonen aan dat wanneer dit enzym faalt, DNA instabiel wordt, tumoren agressiever groeien, en dat een veelvoorkomende vitamine en een antioxidant de balans tussen tumorgroei en celdood kunnen verschuiven.
Het kleine koolstofverkeerscentrum van de cel
In onze cellen ondersteunt een netwerk dat bekendstaat als één-koolstofmetabolisme stilletjes het leven door bouwstenen te leveren voor DNA-productie en chemische labels die genactiviteit regelen. In het midden van dit netwerk staat een enzym genaamd SHMT, dat samenwerkt met vitamine B6 in zijn actieve vorm. SHMT helpt één aminozuur omzetten in een ander terwijl het kleine koolstofeenheden overdraagt die nodig zijn om DNA te maken. In veel menselijke kankers worden hoge niveaus van dit enzym aangetroffen en men denkt dat het tumoren kan helpen groeien. Toch worden in sommige kankers lage niveaus van één SHMT-vorm geassocieerd met slechtere uitkomsten, wat suggereert dat het enzym, afhankelijk van de context, ook als tumorremmend kan fungeren.
Fruitvliegjes gebruiken om tumoren te volgen
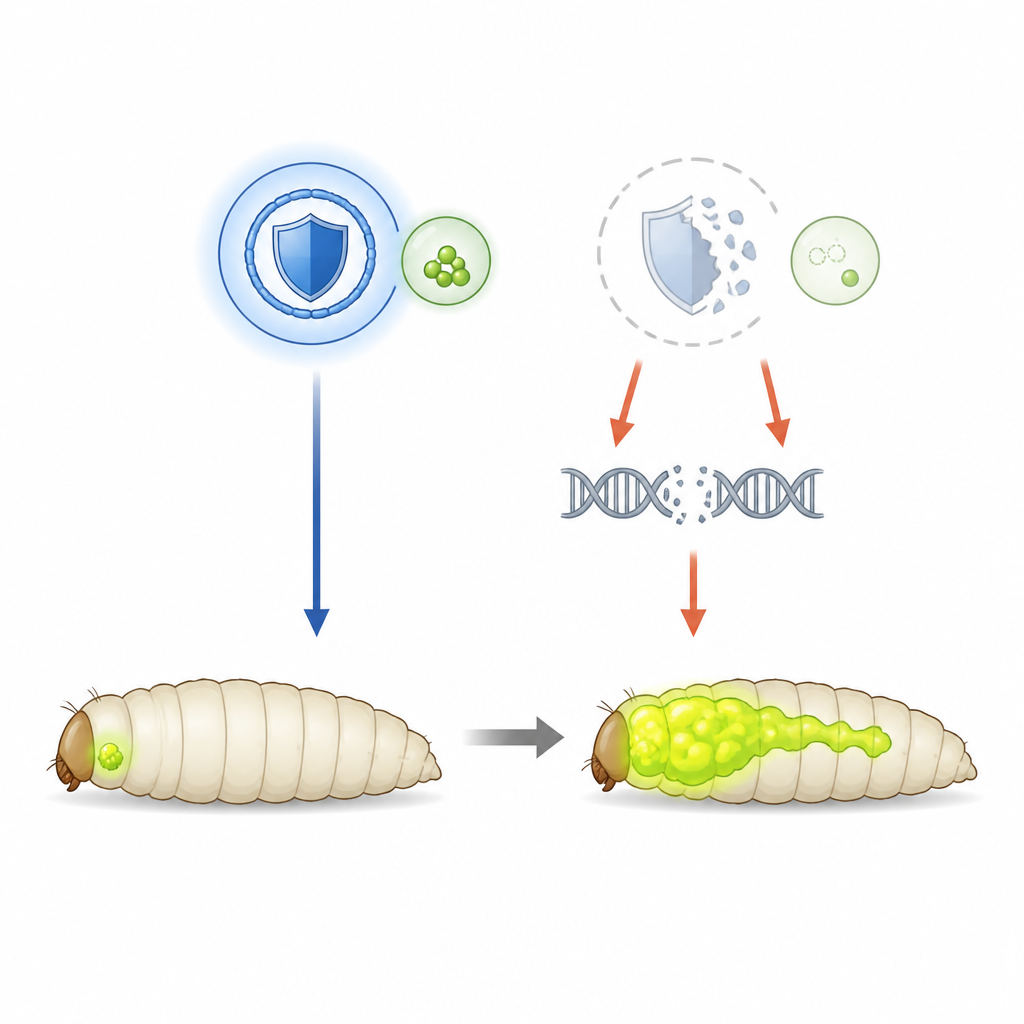
Om de beschermende rol van SHMT te ontrafelen, wendde het team zich tot fruitvliegjes die waren ontworpen om agressieve oogtumoren te ontwikkelen, aangedreven door een overactief Ras-gen en verlies van een gen voor cellulaire polariteit. Deze tumoren gloeien groen, waardoor wetenschappers hun grootte en uitzaaiing in de larve kunnen volgen. In deze situatie zijn de SHMT-niveaus normaal, zodat de onderzoekers het enzym doelbewust konden verminderen met RNA-interferentie. Toen SHMT-activiteit werd verlaagd, werden de primaire tumoren groter en drongen ze vaker het zenuwstelsel van de vlieg binnen, wat laat zien dat SHMT hier werkt als een rem op kankerprogressie in plaats van als brandstof.
DNA-bouwstenen, schade en oxidatieve stress
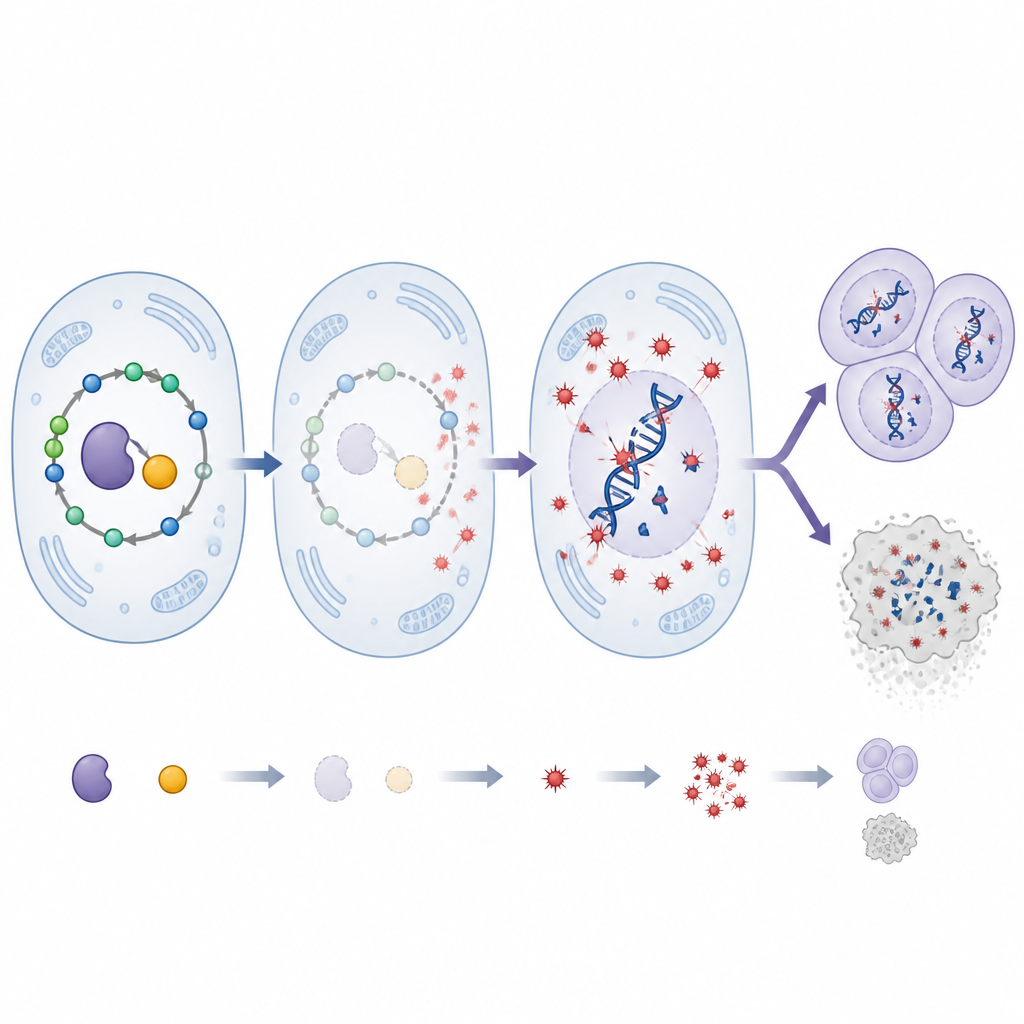
SHMT voedt normaal een route die thymidylaat produceert, een essentiële bouwsteen van DNA. Toen SHMT werd stilgelegd, stokte de aanvoer van deze bouwsteen. Het resultaat was een toename van dubbelstrengsbreuken in DNA en duidelijk verbrijzelde chromosomen in tumoren, duidelijke tekenen van genome-instabiliteit. Deze cellen werden ook ongewoon gevoelig voor DNA-beschadigende röntgenstraling en voor medicijnen die DNA-replicatie vertragen, en ze hadden moeite om breuken te herstellen zodra die optraden. Tegelijkertijd stegen de niveaus van reactieve zuurstofsoorten, schadelijke zuurstofbevattende moleculen, sterk. Behandeling van larven met thymidylaat herstelde de DNA-bouwstenen en verlaagde zowel DNA-schade als oxidatieve stress, terwijl een antioxidant, N-acetylcysteïne, de reactieve zuurstofsoorten, chromosoomschade en tumorgroei verminderde. Samen wijzen deze bevindingen op een keten van gebeurtenissen waarin een slechte aanvoer van DNA-bouwstenen oxidatieve stress verhoogt, wat vervolgens DNA aanvalt en tumoren helpt voortschrijden.
Een vitaminecofactor kantelt de balans
SHMT is afhankelijk van pyridoxal-5'-fosfaat, de actieve vorm van vitamine B6, om te functioneren. De onderzoekers verlaagden deze vitamine in de vliegen met behulp van een dieetblokker en onderzochten hoe dit samenwerkte met verminderd SHMT. Alleen SHMT verminderen versnelde tumorgroei en verhoogde DNA-schade. Het verlagen van vitamine B6 alleen had mildere effecten. Opvallend genoeg veroorzaakte de combinatie van beide veranderingen een dramatische piek in oxidatieve stress en DNA-breuken, veel meer dan één van beide veranderingen afzonderlijk. Dit leidde echter niet tot proportioneel grotere tumoren. In plaats daarvan schakelden veel tumorcellen een sleutel-enzym voor celdood aan en ondergingen ze apoptose, wat suggereert dat extreem beschadigde cellen werden geëlimineerd. Behandeling met hoge doses antioxidant verlaagde opnieuw oxidatieve stress, DNA-schade en tumorgrootte, wat de centrale rol van reactieve zuurstofsoorten bij deze uitkomsten onderstreept.
Wat dit betekent voor kanker en voeding
Dit werk toont aan dat SHMT in een levend dier als tumorremmend kan optreden door bij te dragen aan DNA-stabiliteit en het beheersen van oxidatieve stress. Wanneer SHMT-activiteit daalt, vooral samen met verminderde vitamine B6, hopen tumorcellen DNA-schade op die ofwel de kanker vooruit helpt of, bij een te grote belasting, hun eigen dood activeert. De studie onthult ook een directe gen–voedingsinteractie tussen SHMT en vitamine B6 die bepaalt hoe tumoren groeien. Hoewel deze bevindingen uit fruitvliegjes komen, weerspiegelen ze patronen die in sommige menselijke kankers worden gezien en suggereren ze dat het samen richten op SHMT, zijn vitaminecofactor en reactieve zuurstofsoorten toekomstige strategieën kan informeren om tumorgroei te beheersen zonder uitsluitend te vertrouwen op het doden van deeltelende cellen.
Bronvermelding: Angioli, C., Ferriero, A., Pilesi, E. et al. Tumor suppressor function of SHMT in a Drosophila RasV12DlgRNAi model: DNA damage and synergistic gene-nutrient interaction with PLP. Cell Death Dis 17, 427 (2026). https://doi.org/10.1038/s41419-026-08602-7
Trefwoorden: kankermetabolisme, DNA-schade, reactieve zuurstofsoorten, vitamine B6, Drosophila-tumoren