Clear Sky Science · sv
Cysteinreaktiva medel som mildrar småkärlssjukdoms‑relaterade NOTCH3‑mutanter
Varför denna studie av hjärnans blodkärl är viktig
Cerebral småkärlssjukdom är en huvudorsak till stroke och demens, men många ärftliga former saknar behandling. En sådan sjukdom, CADASIL, drivs av förändringar i ett enda protein i väggarna på små hjärnartärer och leder till progressiva skador över årtionden. Denna studie undersöker om vissa små, läkemedelsliknande kemikalier kan styra det defekta proteinet tillbaka mot en friskare form, vilket antyder en ny möjlighet att bromsa eller förebygga sjukdom hos personer som bär riskabla genvarianter.
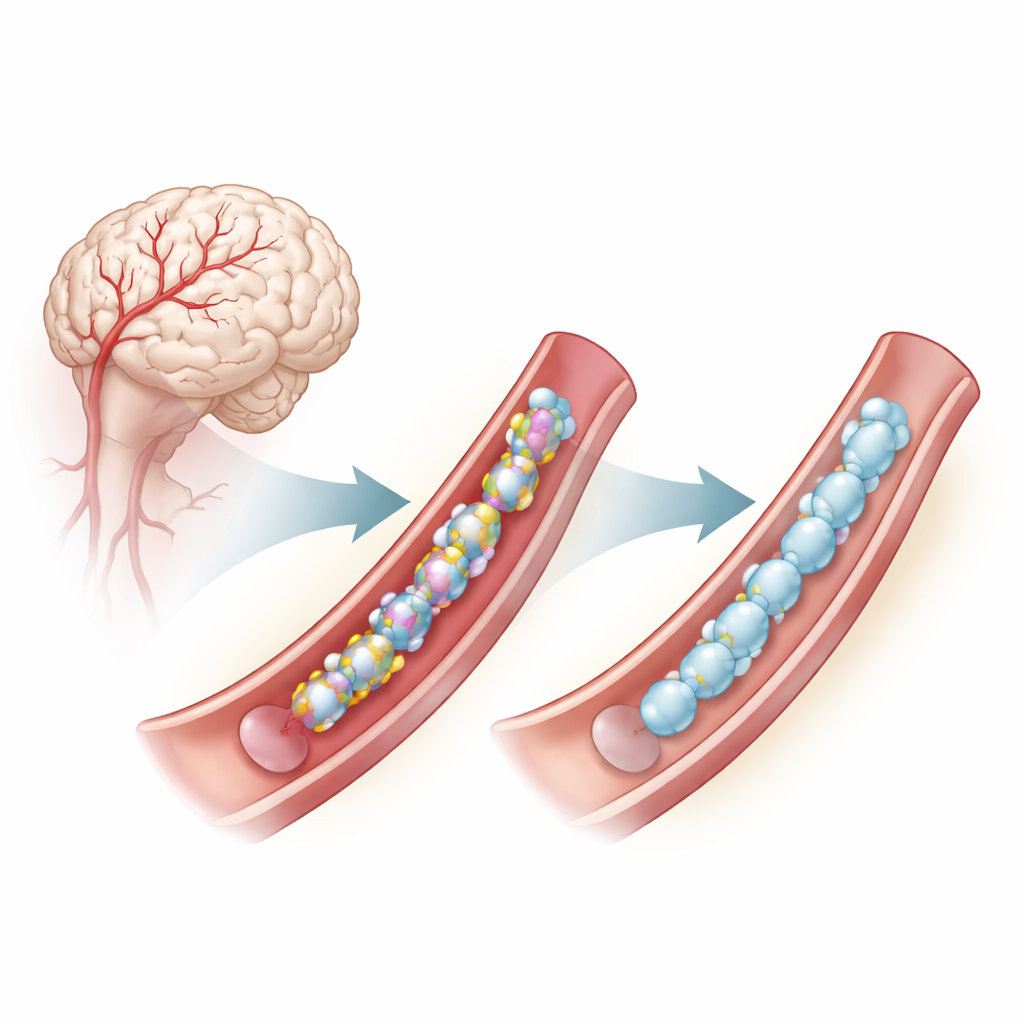
Ett problem djupt inne i hjärnans blodkärlväggar
CADASIL orsakas av mutationer i en gen kallad NOTCH3, som är aktiv i glatta muskelceller som bekläder små hjärnartärer. Dessa mutationer förändrar ofta antalet eller placeringen av en särskild byggsten, cystein, inom upprepade segment av NOTCH3‑proteinet. Cysteinenheter bildar normalt par och disulfidbryggor, små kemiska länkar som hjälper proteinet att veckas korrekt. När antalet cysteiner är felaktigt tenderar NOTCH3 att felveckas, klumpa ihop sig utanför cellerna och störa blodkärlens funktion, vilket bidrar till tidiga strokekänsliga händelser och kognitiv försämring. Även vissa mutationer som inte direkt ändrar cystein verkar ge upphov till liknande felveckningar som är beroende av dessa disulfidbindningar.
Ett ljusbaserat test för snedvridna proteiner
För att söka efter sätt att rädda felaktigt NOTCH3 använde forskarna ett känsligt laboratorieverktyg de tidigare utvecklat: ett split‑luciferas‑rapporteringssystem kallat LSL‑NOTCH3. I denna uppställning är delar av NOTCH3‑proteinet fästa mellan två halvor av ett ljusemitterande enzym. När NOTCH3 produceras, veckas och utsöndras korrekt från celler återförenas enzymhalvorna och ger en stark ljussignal i omgivande vätska. När proteinet felveckas minskar produktionen och utsöndringen, och ljusstyrkan faller. En andra mätning i samma analys följer hur stor andel av proteinet som har korrekta disulfidbindningar genom att jämföra ljuset före och efter kemisk ”upplåsning” av dolda, onormala bindningar. Tillsammans ger dessa avläsningar ett snabbt sätt att se om någon behandling får mutant NOTCH3 att bete sig mer som sin friska motsvarighet.
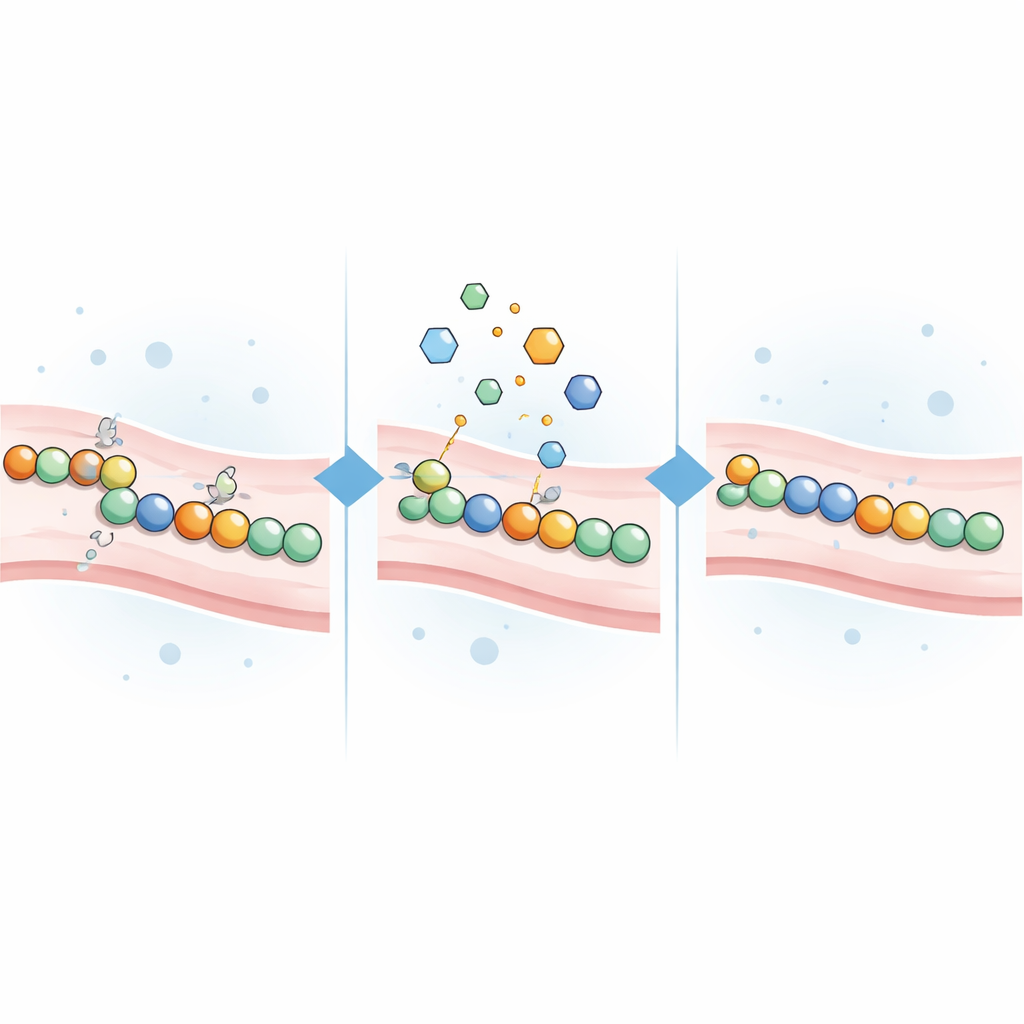
Test av cysteinsökande kemikalier som reparatörer
Eftersom CADASIL‑mutationer ofta lämnar cysteingrupper opaired resonerade teamet att små molekyler som reagerar med cystein skulle kunna hjälpa. De samlade 21 cysteinreaktiva föreningar, inklusive klassiska laboratoriereagens och flera godkända eller undersökta läkemedel ursprungligen utvecklade för cancer, magsyrarelaterade störningar eller andra tillstånd. Varje förening tillsattes till celler som uttryckte en av 16 olika sjukdomsframkallande NOTCH3‑varianter som täckte flera riskkopplade regioner av proteinet, liksom till celler som uttryckte normala eller ofarliga varianter. Forskarna mätte sedan hur mycket ljussignalen förändrades som svar på varje behandling.
Bredverkande hjälpmedel framträder i screeningen
Mer än hälften av de testade föreningarna förbättrade åtminstone en sjukdomsframkallande NOTCH3‑variant, och fem kemikalier ökade huvudljussignalen i hälften eller fler av mutanterna. Bland dessa kom de starkaste och bredaste effekterna från disulfiram, ett etablerat läkemedel för alkoholberoende, och auranofin, ett guldinnehållande läkemedel som används vid reumatoid artrit. Dessa föreningar ökade inte bara den totala ljusutgången, vilket tyder på bättre proteinproduktion och utsöndring, utan förbättrade också andelen protein med gynnsamma disulfidbindningsmönster. Viktigt är att de inte påverkade normal NOTCH3, vilket antyder viss selektivitet för de felveckade formerna. Ytterligare experiment visade att kemikalierna behövde vara närvarande medan cellerna syntetiserade proteinet och inte fungerade på redan utsöndrat protein, vilket indikerar att de sannolikt verkar under veckningen inne i cellen.
Bortom en gen och en mutation
Forskarna undersökte om nyttan av cysteinreaktiva föreningar berodde på vilken aminosyra som ersatte cystein i en mutation. Genom systematiska substitutioner av många olika rester på nyckelpositioner fann de att disulfiram och en relaterad förening ändå förbättrade rapportöraktiviteten i nästan alla fall. Detta stöder idén att läkemedlen riktar sig mot det gemensamma problemet med saknade cysteinpar snarare än någon särskild ersättning. De testade också ett andra, oberoende rapportsystem baserat på en annan split‑luciferas‑design och bekräftade att disulfiram på liknande sätt förbättrade sekretionen av mutanta NOTCH3‑fragment men inte den normala formen. När de vände sig till ett annat cysteinrikt protein involverat i Marfans syndrom, FBN1, hjälpte disulfiram endast ett fåtal mutanter och auranofin hjälpte ingen, vilket antyder att NOTCH3 i CADASIL kan vara särskilt känsligt för denna strategi.
Vad detta kan innebära för framtida behandlingar
Detta arbete visar att det är möjligt att delvis korrigera beteendet hos många olika NOTCH3‑mutanter med brett cysteinreaktiva små molekyler, inklusive läkemedel som redan används kliniskt för andra sjukdomar. Resultaten pekar mot en enhetlig mekanism där extra eller exponerade cysteingrupper i mutant NOTCH3 driver skadlig felveckning, och där kapsling av dessa reaktiva platser kan återställa mer normal proteinveckning och utsöndring. Även om dessa resultat kommer från cellbaserade modeller och ännu inte från patienter eller djurstudier, lägger de grunden för att utveckla eller återanvända cysteinriktade läkemedel som potentiella terapier för CADASIL och relaterade störningar i små hjärnkärl.
Citering: Cartee, N.M.P., Zhang, X., Lee, S.J. et al. Cysteine-reactive mitigators of small vessel disease-related NOTCH3 mutants. Sci Rep 16, 14300 (2026). https://doi.org/10.1038/s41598-026-45103-1
Nyckelord: CADASIL, NOTCH3‑mutationer, småkärlssjukdom, läkemedel som riktar cystein, proteinfelveckning