Clear Sky Science · fr
Atténuateurs réactifs à la cystéine des mutants NOTCH3 liés à la maladie des petits vaisseaux
Pourquoi cette étude sur les vaisseaux sanguins cérébraux est importante
La maladie cérébrale des petits vaisseaux est une cause majeure d’accidents vasculaires cérébraux et de démence, et de nombreuses formes héréditaires restent sans traitement. Une de ces affections, appelée CADASIL, est provoquée par des altérations d’une seule protéine dans les parois des petites artères cérébrales, entraînant des lésions progressives sur des décennies. Cette étude examine si certaines petites molécules de type médicament peuvent inciter cette protéine défectueuse à reprendre une conformation plus saine, suggérant une nouvelle voie pour ralentir ou prévenir la maladie chez les porteurs de variants génétiques à risque.
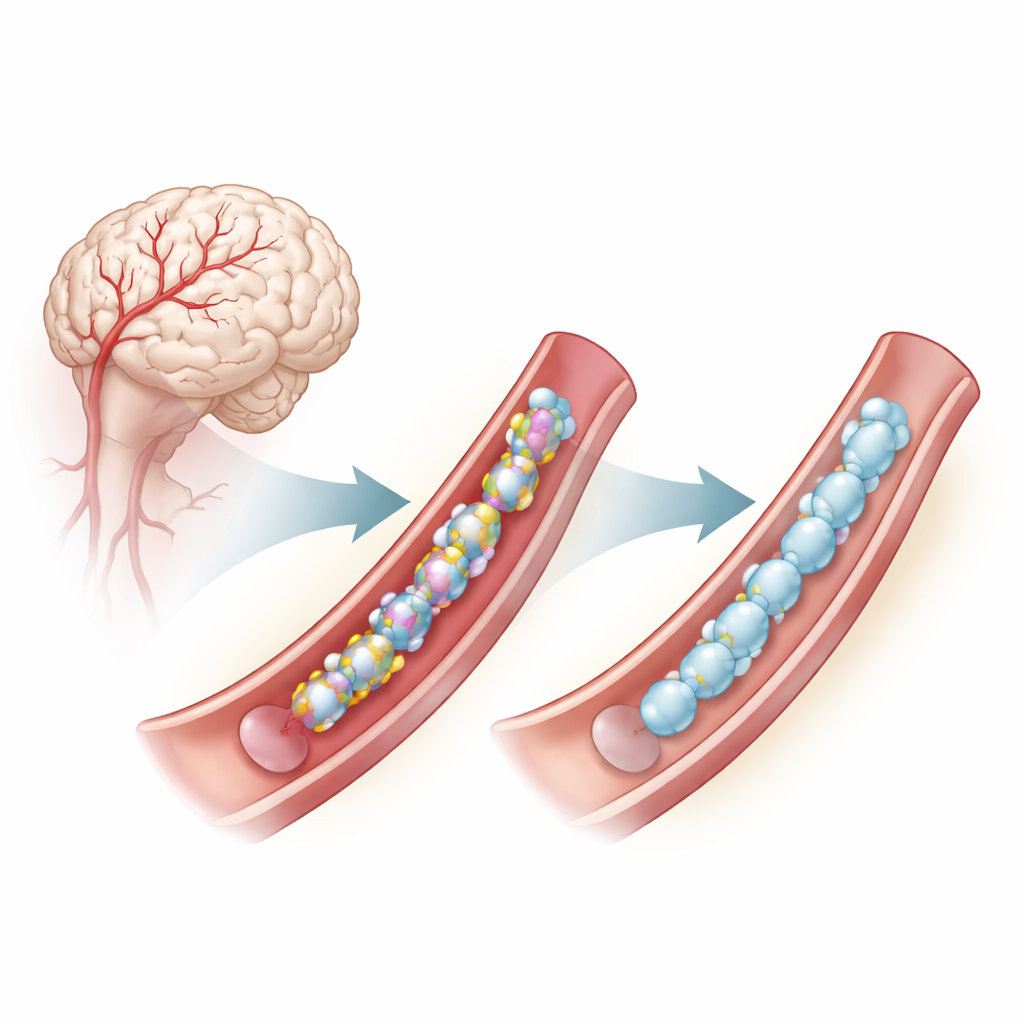
Un problème niché dans les parois des petits vaisseaux cérébraux
Le CADASIL est causé par des mutations dans un gène appelé NOTCH3, qui est actif dans les cellules musculaires lisses qui tapissent les petites artères cérébrales. Ces mutations modifient souvent le nombre ou la position d’un acide aminé particulier, la cystéine, au sein de répétitions du domaine de la protéine NOTCH3. Les résidus de cystéine s’apparient normalement pour former des ponts disulfure, de petits ponts chimiques qui aident la protéine à se replier correctement. Lorsque le nombre de cystéines est perturbé, NOTCH3 a tendance à se mal replier, à s’agréger à l’extérieur des cellules et à perturber le fonctionnement des vaisseaux, contribuant aux AVC précoces et au déclin cognitif. Même certaines mutations qui ne modifient pas directement la cystéine semblent engendrer des problèmes de repliement similaires dépendants de ces ponts disulfure.
Un test basé sur la lumière pour détecter les protéines mal conformées
Pour rechercher des moyens de restaurer un NOTCH3 défaillant, les chercheurs ont utilisé un outil sensible développé précédemment : un système rapporteur à luciférase scindée appelé LSL-NOTCH3. Dans ce dispositif, des fragments de la protéine NOTCH3 sont fusionnés entre deux moitiés d’une enzyme émettrice de lumière. Lorsque NOTCH3 est synthétisé, replié et sécrété correctement par les cellules, les demi‑enzymes se rejoignent et produisent un signal lumineux fort dans le milieu environnant. Quand la protéine se mal reploie, la production et la sécrétion chutent, et l’intensité lumineuse diminue. Une seconde mesure dans le même test évalue la proportion de protéine ayant les ponts disulfure corrects en comparant la lumière avant et après le « déverrouillage » chimique de liaisons anormales cachées. Ensemble, ces lectures offrent un moyen rapide de voir si un traitement rend un NOTCH3 mutant plus proche de sa forme saine.
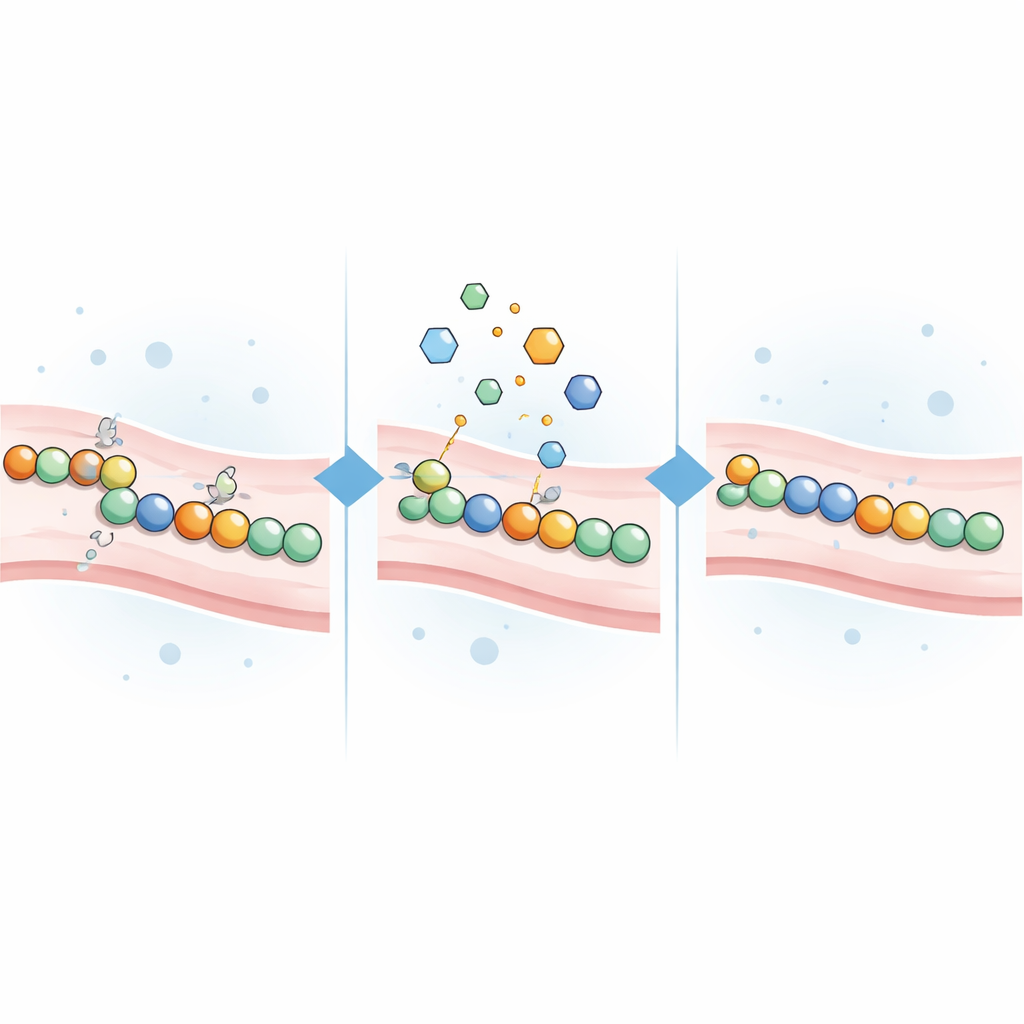
Tester des molécules ciblant la cystéine comme réparatrices
Parce que les mutations du CADASIL laissent souvent des groupes cystéine sans appariement, l’équipe a émis l’hypothèse que de petites molécules réactives envers la cystéine pourraient aider. Ils ont rassemblé 21 composés réactifs à la cystéine, comprenant des réactifs classiques de laboratoire et plusieurs médicaments approuvés ou en investigation initialement développés pour le cancer, les troubles de l’acidité gastrique ou d’autres indications. Chaque composé a été ajouté à des cellules exprimant l’un des 16 variants pathogènes de NOTCH3 couvrant plusieurs régions liées au risque, ainsi qu’à des cellules exprimant des variantes normales ou bénignes. Les scientifiques ont ensuite mesuré combien le signal lumineux variait en réponse à chaque traitement.
Des aides à large spectre émergent du criblage
Plus de la moitié des composés testés ont amélioré au moins un variant pathogène de NOTCH3, et cinq molécules ont augmenté le signal lumineux principal dans la moitié ou plus des mutants. Parmi elles, les effets les plus forts et les plus larges provenaient du disulfirame, un médicament classique contre la dépendance à l’alcool, et de l’auranofine, un médicament à base d’or utilisé pour la polyarthrite rhumatoïde. Ces composés ont non seulement augmenté la lumière globale, suggérant une meilleure production et sécrétion de la protéine, mais ont aussi amélioré la fraction de protéine présentant des ponts disulfure favorables. Fait important, ils n’agissaient pas sur le NOTCH3 normal, ce qui suggère une certaine sélectivité pour les formes mal repliées. Des expériences supplémentaires ont montré que les composés devaient être présents pendant la synthèse de la protéine par les cellules et n’agissaient pas sur la protéine déjà sécrétée, indiquant qu’ils interviennent probablement lors du repliement intracellulaire.
Au‑delà d’un gène et d’une mutation
Les chercheurs ont cherché à savoir si l’effet des composés réactifs à la cystéine dépendait de l’acide aminé ayant remplacé la cystéine dans une mutation. En substituant systématiquement de nombreux résidus à des positions clés, ils ont constaté que le disulfirame et un composé apparenté amélioraient encore l’activité du rapporteur dans presque tous les cas. Cela soutient l’idée que les médicaments ciblent le problème commun des paires de cystéine manquantes, plutôt qu’un remplacement spécifique. Ils ont également testé un second système rapporteur indépendant basé sur une autre conception de luciférase scindée et confirmé que le disulfirame améliorait de la même manière la sécrétion de fragments mutants de NOTCH3 mais pas la forme normale. Lorsqu’ils se sont tournés vers une autre protéine riche en cystéine impliquée dans le syndrome de Marfan, FBN1, le disulfirame n’a aidé que quelques mutants et l’auranofine n’aida aucun, suggérant que NOTCH3 dans le CADASIL peut être particulièrement sensible à cette stratégie.
Ce que cela pourrait signifier pour de futurs traitements
Ce travail montre qu’il est possible de corriger partiellement le comportement de nombreux mutants NOTCH3 différents en utilisant de petites molécules réactives à la cystéine à large spectre, y compris des médicaments déjà en clinique pour d’autres maladies. Les résultats pointent vers un mécanisme unificateur dans lequel des cystéines supplémentaires ou exposées dans NOTCH3 mutant favorisent un mauvais repliement délétère, et où le blocage de ces sites réactifs peut restaurer un repliement et une sécrétion plus normaux. Bien que ces résultats proviennent de modèles cellulaires et non encore de patients ou d’études animales, ils posent les bases du développement ou du repositionnement de médicaments ciblant la cystéine comme thérapies potentielles pour le CADASIL et les troubles apparentés des petits vaisseaux cérébraux.
Citation: Cartee, N.M.P., Zhang, X., Lee, S.J. et al. Cysteine-reactive mitigators of small vessel disease-related NOTCH3 mutants. Sci Rep 16, 14300 (2026). https://doi.org/10.1038/s41598-026-45103-1
Mots-clés: CADASIL, mutations de NOTCH3, maladie des petits vaisseaux, médicaments ciblant la cystéine, dénaturation des protéines