Clear Sky Science · ja
小血管疾患関連NOTCH3変異体に対するシステイン反応性の緩和剤
この脳の血管研究が重要な理由
脳の小血管疾患は脳卒中や認知症の主な原因のひとつですが、遺伝性の多くの型には治療法がありません。CADASILと呼ばれる一つの疾患は、細い脳動脈の壁にある単一のタンパク質の変化によって引き起こされ、数十年にわたって進行性の損傷をもたらします。本研究は、いくつかの小さな薬剤様化合物がその異常なタンパク質をより健康的な立体構造へと戻すように働きかけられるかを調べ、リスクの高い遺伝子変異を持つ人々の病気を遅らせたり予防したりする新たな方法の可能性を示唆します。
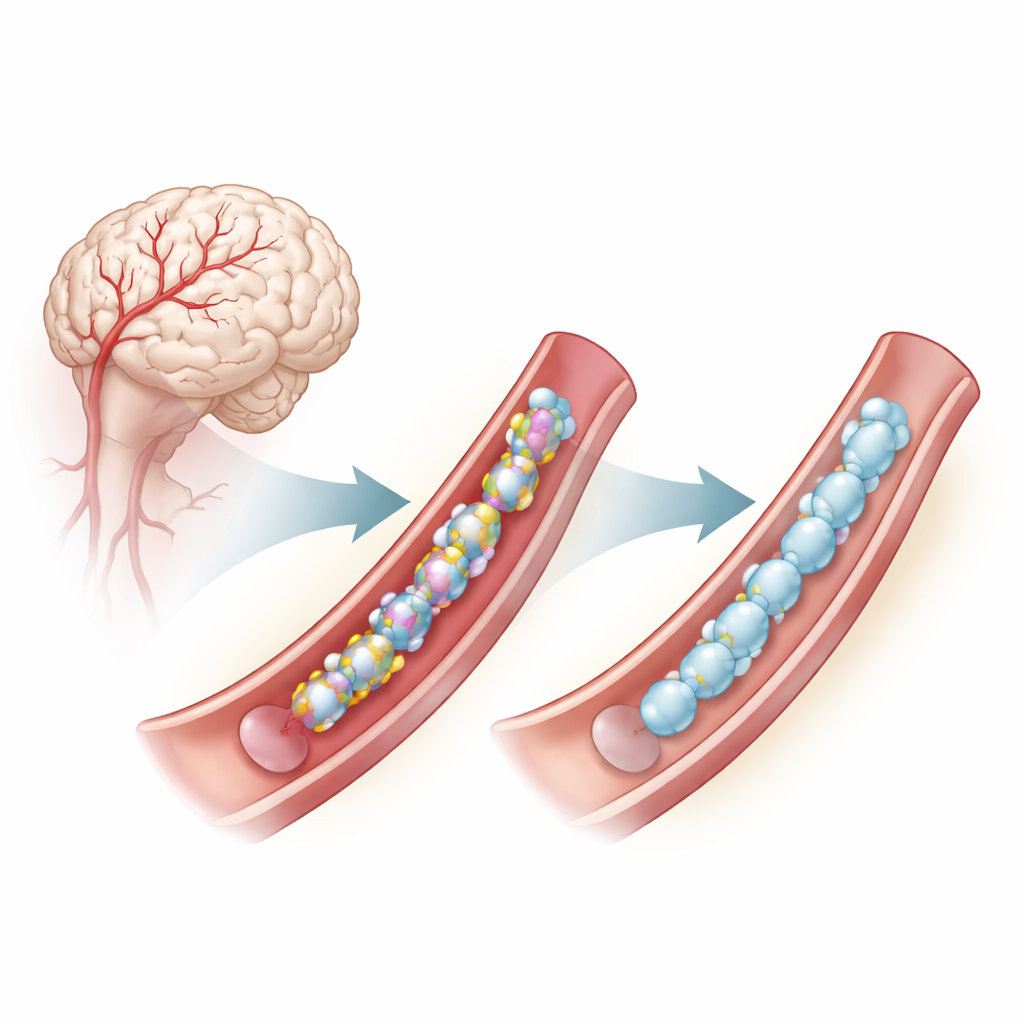
脳の血管壁の奥にある問題
CADASILはNOTCH3と呼ばれる遺伝子の変異によって引き起こされ、これは小さな脳動脈を裏打ちする平滑筋細胞で発現します。これらの変異はしばしばNOTCH3タンパク質の繰り返し領域内の特定の構成要素であるシステインの数や配置を変えます。システイン残基は通常、ジスルフィド結合として互いに対を作り、タンパク質が正しく折りたたまれるのを助ける微細な化学的橋を形成します。システインの数が不適切になると、NOTCH3は誤って折りたたまれやすく、細胞外で凝集し、血管機能を乱して早期の脳卒中や認知機能低下に寄与します。システインを直接変えない変異ですら、これらのジスルフィド結合に依存した類似の誤folding問題を生む場合があります。
変形したタンパク質を光で調べる検査
研究者たちは、欠陥のあるNOTCH3を救う方法を探るため、以前に開発した感度の高い実験ツールを用いました:LSL-NOTCH3と呼ばれるスプリットルシフェラーゼレポーターシステムです。この仕組みでは、NOTCH3の断片が発光酵素の二つの半分の間に融合されています。NOTCH3が細胞内で正しく合成・折りたたまれ、分泌されると酵素の半分同士が再結合して周囲の溶液に強い光信号を生じます。タンパク質が誤って折りたたまれると、生産と分泌が低下し、光出力が落ちます。同じアッセイ内の二つ目の測定は、化学的に隠れた異常な結合を「解除」する前後の光を比較することで、正しいジスルフィド結合を持つタンパク質の割合を追跡します。これらの指標を組み合わせることで、どの治療が変異型NOTCH3をより健康な型に近づけるかを迅速に評価できます。
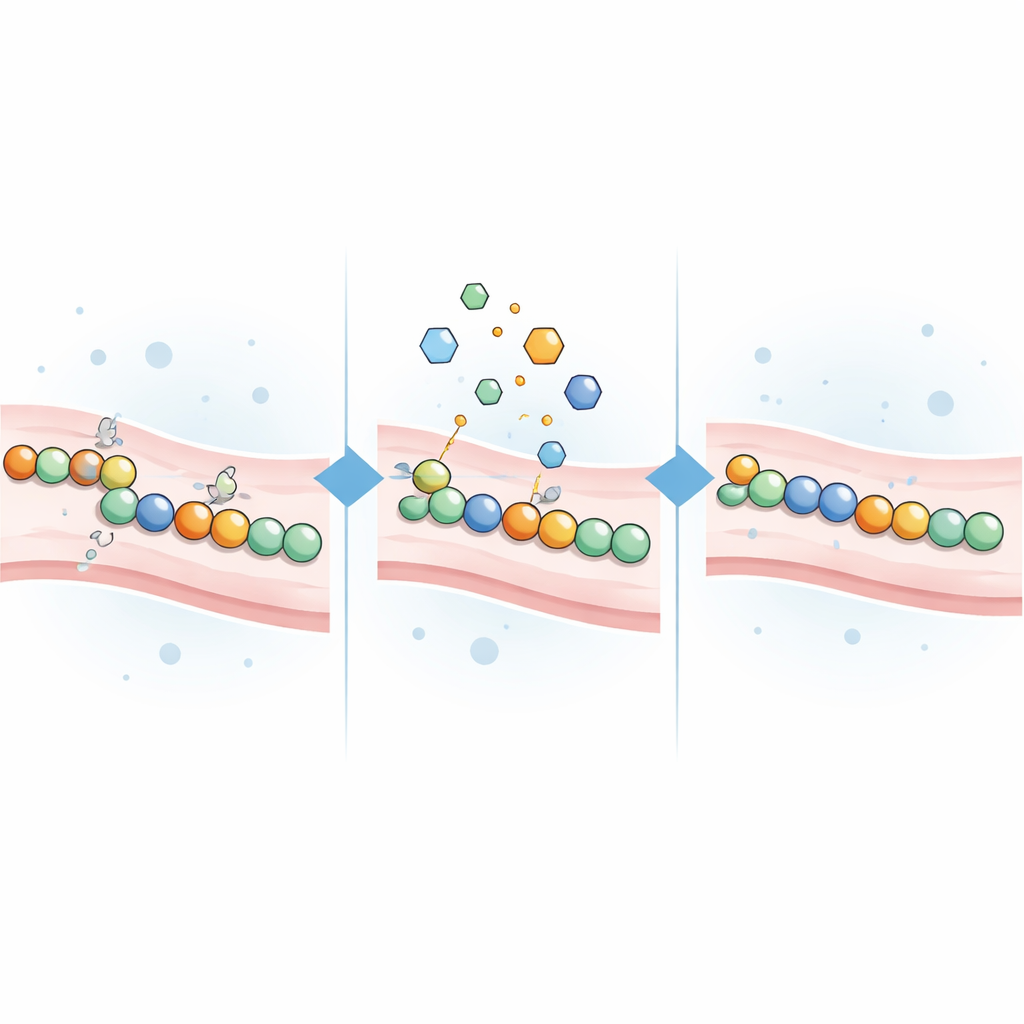
システインを標的にする化合物を修復剤として検査
CADASIL変異はしばしばシステイン残基の対が欠けるため、チームはシステインと反応する小分子が助けになるかもしれないと考えました。彼らは、古典的な試薬やがん、胃酸関連疾患、その他の適応で開発された承認薬や治験薬を含む21種類のシステイン反応性化合物を集めました。各化合物は、タンパク質のいくつかのリスクに関連する領域にまたがる16種類の疾患原因NOTCH3変異体のうちの一つを発現する細胞、ならびに正常型や無害な変異を発現する細胞に添加されました。その後、各処理に対して光シグナルがどの程度変化したかを測定しました。
スクリーニングから見つかった広範に作用する助っ人
試験された化合物の半数以上が少なくとも一つの疾患原因NOTCH3変異体を改善し、五つの化学物質は主要な光シグナルを変異体の半数以上で増加させました。その中でも、最も強く広範な効果を示したのは、アルコール依存症治療薬として確立されたジスルフィラムと、リウマチ治療に用いられる金含有薬オーラノフィンでした。これらの化合物は、タンパク質の生産と分泌が改善されたことを示す全体の光出力を増やしただけでなく、有利なジスルフィド結合パターンを持つタンパク質の割合も改善しました。重要なことに、これらは正常なNOTCH3には影響を与えず、誤って折りたたまれた形に対してある程度の選択性があることを示唆します。追加実験では、化合物は細胞がタンパク質を合成している間に存在する必要があり、分泌済みのタンパク質単独には効果がなかったため、これらが細胞内での折りたたみ過程中に作用している可能性が高いことが示されました。
一つの遺伝子や一つの変異にとどまらない効果
研究者たちは、システイン反応性化合物の効果がシステインの代わりにどのアミノ酸が入るかに依存するかどうかを検討しました。主要な位置に多数の異なる残基を系統的に置換したところ、ジスルフィラムと関連化合物はほぼすべての場合でレポーター活性を改善しました。これは、薬剤が特定の置換ではなく、欠けたシステイン対という共通の問題を標的にしているという考えを支持します。別の独立したスプリットルシフェラーゼ設計に基づく検出系でも検証したところ、ジスルフィラムは同様に変異型NOTCH3断片の分泌を促進しましたが正常型には効果がありませんでした。さらに、マルファン症候群に関わる別のシステイン多寡の高いタンパク質であるFBN1に目を向けたところ、ジスルフィラムは一部の変異でのみ効果があり、オーラノフィンは効果がなかったため、CADASILのNOTCH3はこの戦略に特に感受性が高い可能性が示唆されます。
将来の治療にとっての意味
この研究は、他の疾患で臨床使用されている薬剤を含む広範なシステイン反応性小分子を用いて、多様なNOTCH3変異体の挙動を部分的に修正できる可能性を示しています。結果は、変異NOTCH3における余分または露出したシステイン残基が有害な誤foldingを引き起こし、それらの反応性部位をキャップすることでより正常な折りたたみと分泌が回復しうるという統一的なメカニズムを示唆します。これらの結果は細胞ベースのモデルから得られたものであり、患者や動物での検証はまだですが、CADASILや関連する小脳血管障害に対するシステイン標的薬を開発・再利用するための基盤を築きます。
引用: Cartee, N.M.P., Zhang, X., Lee, S.J. et al. Cysteine-reactive mitigators of small vessel disease-related NOTCH3 mutants. Sci Rep 16, 14300 (2026). https://doi.org/10.1038/s41598-026-45103-1
キーワード: CADASIL, NOTCH3変異, 小血管疾患, システイン標的薬, タンパク質の誤った折りたたみ