Clear Sky Science · de
Cystein-reaktive Milder für NOTCH3-Mutanten bei Erkrankungen der kleinen Gefäße
Warum diese Studie zu Blutgefäßen im Gehirn wichtig ist
Die zerebrale Small-Vessel-Erkrankung ist eine Hauptursache für Schlaganfall und Demenz, doch viele vererbte Formen sind unbehandelt. Eine dieser Erkrankungen, CADASIL genannt, wird durch Veränderungen eines einzelnen Proteins in den Wänden kleiner Hirnarterien verursacht und führt über Jahrzehnte zu fortschreitenden Schäden. Diese Studie untersucht, ob bestimmte kleine, medikamentenähnliche Verbindungen das fehlerhafte Protein wieder in eine gesündere Form bringen können — ein Hinweis auf einen neuen Weg, die Krankheit bei Menschen mit riskanten Genvarianten zu verlangsamen oder zu verhindern.
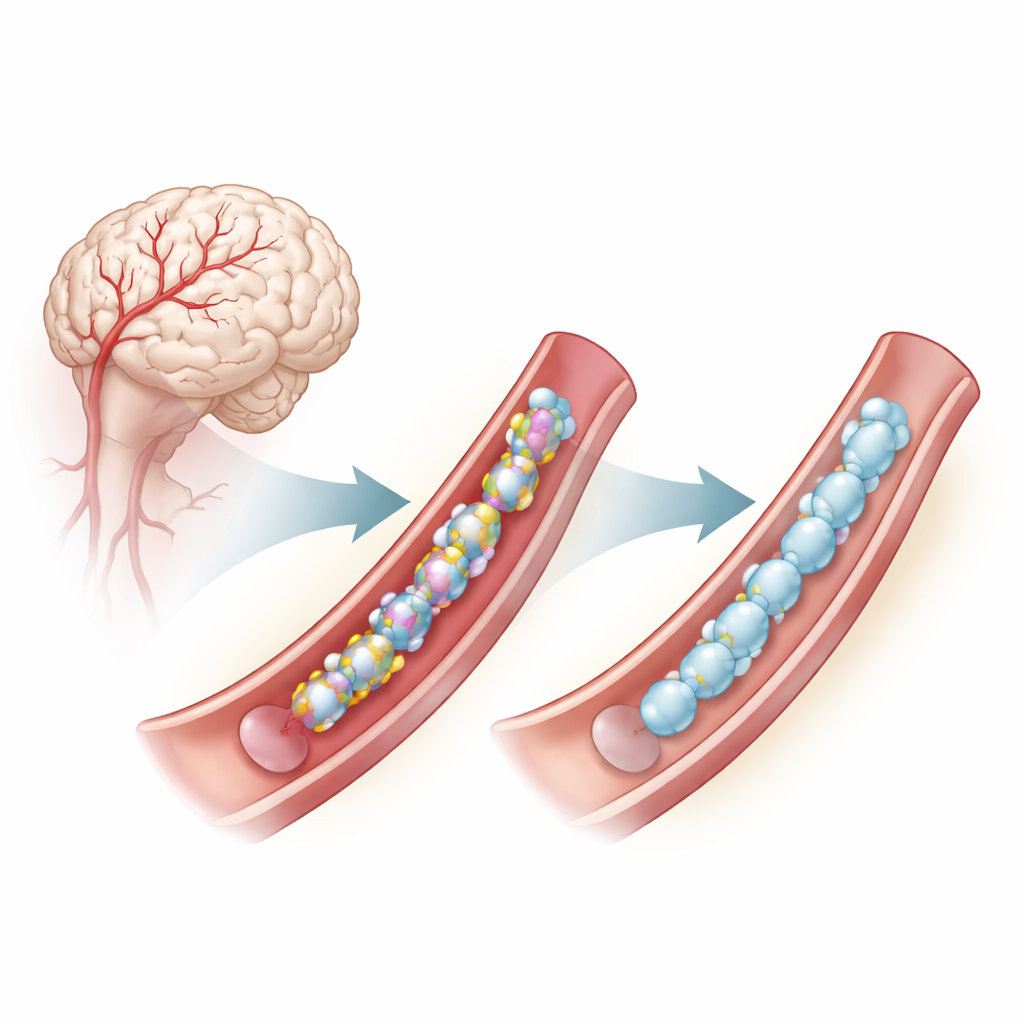
Ein Problem tief in den Gefäßwänden des Gehirns
CADASIL wird durch Mutationen in einem Gen namens NOTCH3 verursacht, das in den glatten Muskelzellen der kleinen Hirnarterien aktiv ist. Diese Mutationen verändern oft die Anzahl oder die Position eines bestimmten Bausteins, Cystein, innerhalb wiederkehrender Abschnitte des NOTCH3-Proteins. Cysteinreste paaren sich normalerweise zu Disulfidbrücken, winzigen chemischen Bindungen, die dem Protein helfen, korrekt zu falten. Ist die Anzahl der Cysteine falsch, neigt NOTCH3 zur Fehlfaltung, verklumpt außerhalb der Zellen und stört die Gefäßfunktion, was zu frühen Schlaganfällen und kognitivem Abbau beiträgt. Selbst einige Mutationen, die Cysteine nicht direkt verändern, scheinen ähnliche fehlgefaltete Probleme zu erzeugen, die von diesen Disulfidbrücken abhängen.
Ein lichtbasierter Test für verformte Proteine
Um nach Wegen zu suchen, fehlerhaftes NOTCH3 zu retten, verwendeten die Forscher ein sensibles Labortool, das sie zuvor entwickelt hatten: ein geteiltes Luciferase-Reportersystem namens LSL-NOTCH3. In diesem Aufbau sind Teile des NOTCH3-Proteins zwischen zwei Hälften eines lichtemittierenden Enzyms eingefügt. Wenn NOTCH3 korrekt hergestellt, gefaltet und aus Zellen ausgeschieden wird, fügen sich die Enzymhälften wieder zusammen und erzeugen ein starkes Lichtsignal in der umgebenden Flüssigkeit. Falzt das Protein, sinken Produktion und Sekretion und damit das Lichtsignal. Eine zweite Messung im selben Test erfasst, wie viel des Proteins die richtigen Disulfidbrücken aufweist, indem das Licht vor und nach dem chemischen "Aufschließen" verborgener, abnormaler Bindungen verglichen wird. Zusammen liefern diese Messwerte eine schnelle Möglichkeit zu erkennen, ob eine Behandlung mutiertes NOTCH3 wieder seiner gesunden Form annähert.
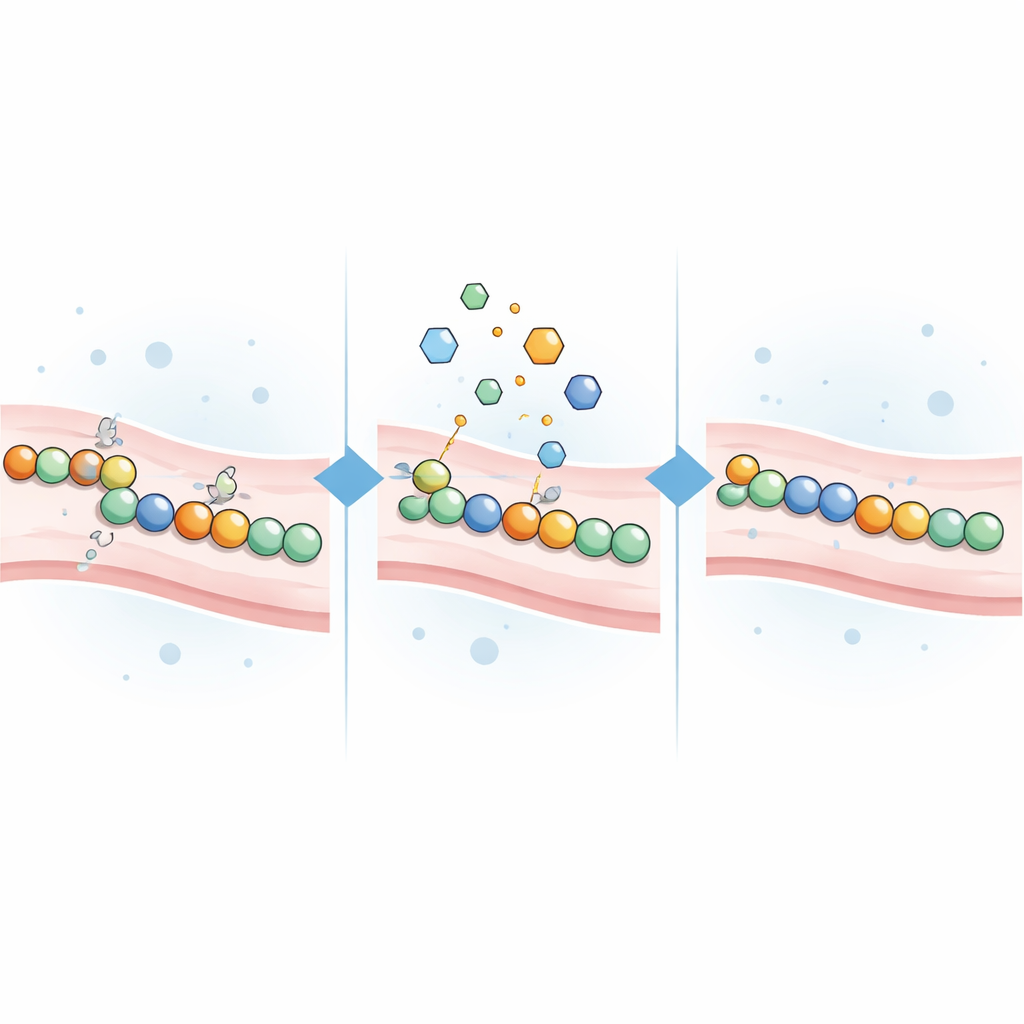
Testen cystein-gerichteter Verbindungen als Korrektoren
Da CADASIL-Mutationen häufig Cysteinreste unpaarig lassen, vermutete das Team, dass kleine Moleküle, die mit Cystein reagieren, helfen könnten. Sie stellten 21 cystein-reaktive Verbindungen zusammen, darunter klassische Laborreagenzien und mehrere zugelassene oder in der Untersuchung befindliche Medikamente, die ursprünglich für Krebs, Magenaciditätsstörungen oder andere Erkrankungen entwickelt wurden. Jede Verbindung wurde Zellen hinzugefügt, die eine von 16 verschiedenen krankheitsverursachenden NOTCH3-Varianten exprimierten, die mehrere risikobehaftete Abschnitte des Proteins abdecken, sowie Zellen mit normaler oder harmloser Variante. Die Wissenschaftler maßen dann, wie stark sich das Lichtsignal als Reaktion auf jede Behandlung veränderte.
Breit wirkende Helfer aus dem Screening
Mehr als die Hälfte der getesteten Verbindungen verbesserte mindestens eine krankheitsverursachende NOTCH3-Variante, und fünf Chemikalien steigerten das primäre Lichtsignal bei der Hälfte oder mehr der Mutanten. Am stärksten und breitesten wirkten Disulfiram, ein etabliertes Medikament zur Behandlung von Alkoholabhängigkeit, und Auranofin, ein goldhaltiges Medikament gegen rheumatoide Arthritis. Diese Verbindungen erhöhten nicht nur die Gesamtlichtstärke, was auf bessere Proteinproduktion und -sekretion hindeutet, sondern verbesserten auch den Anteil des Proteins mit günstigen Disulfid-Bindungsmustern. Wichtig ist, dass sie keine Wirkung auf normales NOTCH3 zeigten, was auf eine gewisse Selektivität für die fehlgefalteten Formen hindeutet. Weitere Experimente zeigten, dass die Chemikalien während der Proteinsynthese in den Zellen vorhanden sein mussten und nicht auf bereits ausgeschiedenes Protein allein wirkten, was darauf hindeutet, dass sie wahrscheinlich während der Faltung innerhalb der Zelle einwirken.
Über ein Gen und eine Mutation hinaus
Die Forscher untersuchten, ob der Nutzen cystein-reaktiver Verbindungen vom spezifischen Aminosäureaustausch abhing, der das Cystein ersetzt. Durch systematisches Ersetzen vieler unterschiedlicher Reste an Schlüsselpositionen stellten sie fest, dass Disulfiram und eine verwandte Verbindung die Reporteraktivität in nahezu allen Fällen weiterhin verbesserten. Das stützt die Idee, dass die Medikamente das gemeinsame Problem fehlender Cysteinpaare ansprechen, statt eine bestimmte Ersatzaminosäure. Sie testeten außerdem ein zweites, unabhängiges Reportersystem auf Basis eines anderen Split-Luciferase-Designs und bestätigten, dass Disulfiram ähnlich die Sekretion mutanter NOTCH3-Fragmente, aber nicht der normalen Form, förderte. Als sie ein weiteres cysteinreiches Protein untersuchten, das bei Marfan-Syndrom eine Rolle spielt (FBN1), half Disulfiram nur einigen wenigen Mutanten und Auranofin gar keinem, was darauf hindeutet, dass NOTCH3 bei CADASIL besonders anfällig für diese Strategie sein könnte.
Was das für künftige Therapien bedeuten könnte
Diese Arbeit zeigt, dass es möglich ist, das Verhalten vieler verschiedener NOTCH3-Mutanten teilweise zu korrigieren, indem breit cystein-reaktive kleine Moleküle eingesetzt werden, einschließlich bereits klinisch verwendeter Medikamente für andere Erkrankungen. Die Ergebnisse deuten auf einen vereinheitlichenden Mechanismus hin, bei dem zusätzliche oder exponierte Cysteinreste in mutiertem NOTCH3 schädliche Fehlfaltung antreiben und das Verschließen dieser reaktiven Stellen normalere Proteinfaltung und -sekretion wiederherstellen kann. Zwar stammen diese Befunde aus zellbasierten Modellen und nicht noch aus Patienten- oder Tierstudien, doch sie legen die Grundlage für die Entwicklung oder Umwidmung cystein-gerichteter Medikamente als potenzielle Therapien für CADASIL und verwandte Erkrankungen der kleinen Hirngefäße.
Zitation: Cartee, N.M.P., Zhang, X., Lee, S.J. et al. Cysteine-reactive mitigators of small vessel disease-related NOTCH3 mutants. Sci Rep 16, 14300 (2026). https://doi.org/10.1038/s41598-026-45103-1
Schlüsselwörter: CADASIL, NOTCH3-Mutationen, Erkrankung der kleinen Gefäße, cystein-gerichtete Medikamente, Proteinfehlfaltung