Clear Sky Science · pl
Środki reagujące z cysteiną łagodzące mutacje NOTCH3 związane z chorobą małych naczyń
Dlaczego to badanie naczyń mózgowych ma znaczenie
Choroba małych naczyń mózgu jest istotną przyczyną udaru i otępienia, a wiele uwarunkowanych genetycznie postaci nie ma leczenia. Jedną z takich chorób jest CADASIL, wywoływana zmianami w pojedynczym białku w ścianach drobnych tętnic mózgowych, prowadzącymi do stopniowego uszkodzenia trwającego dekady. Badanie to analizuje, czy pewne niewielkie, przypominające leki chemikalia mogą skłonić wadliwe białko do przyjęcia zdrowszego kształtu, sugerując nowy sposób spowolnienia albo zapobiegania chorobie u osób noszących ryzykowne warianty genowe.
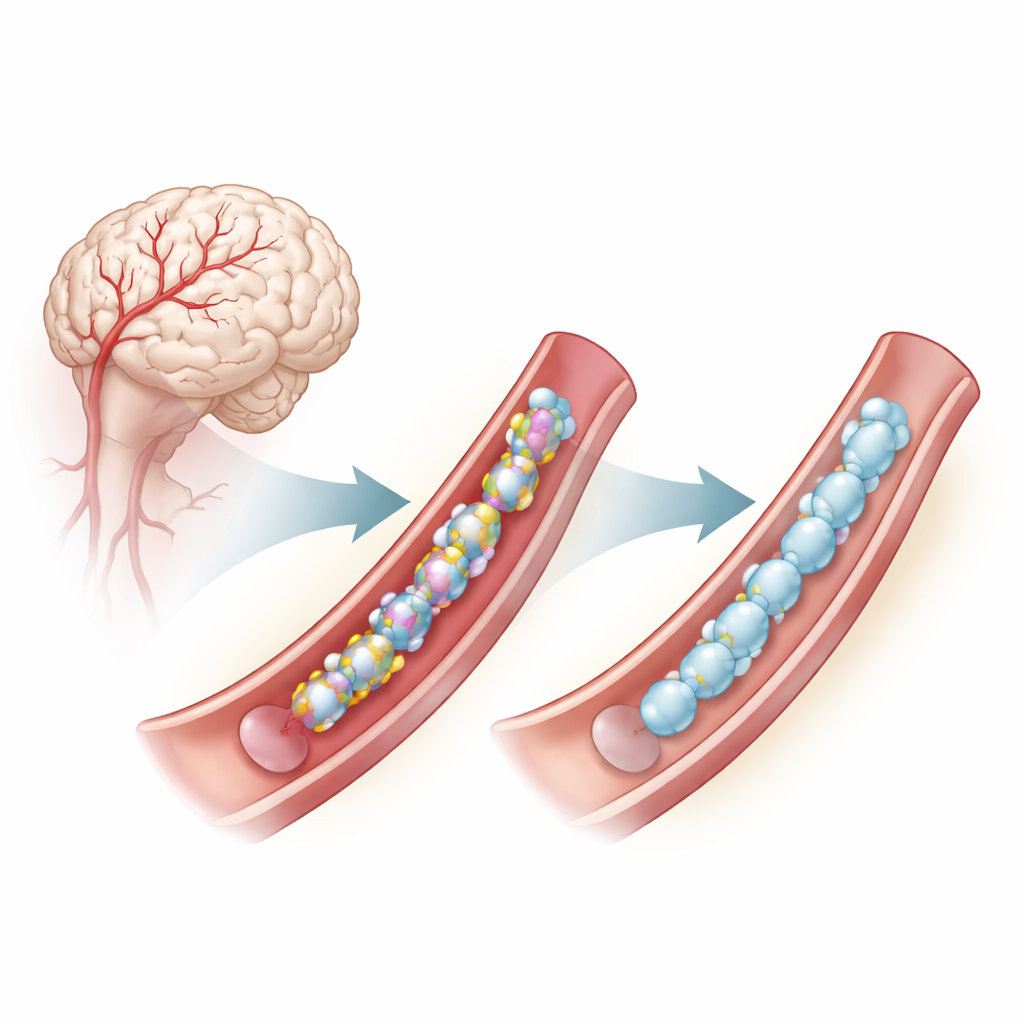
Problem głęboko wewnątrz ścian naczyń mózgowych
CADASIL jest wywoływany mutacjami w genie o nazwie NOTCH3, który jest aktywny w komórkach mięśni gładkich wyściełających drobne tętnice mózgowe. Mutacje te często zmieniają liczbę lub położenie konkretnego elementu budulcowego — cysteiny — w powtarzających się segmentach białka NOTCH3. Reszty cysteiny zwykle łączą się parami, tworząc mostki disiarczkowe, maleńkie chemiczne „mostki”, które pomagają białku prawidłowo się fałdować. Gdy liczba cystein jest nieprawidłowa, NOTCH3 ma tendencję do nieprawidłowego fałdowania, agregowania poza komórkami i zaburzania funkcji naczyń, przyczyniając się do wczesnych udarów i pogorszenia funkcji poznawczych. Nawet niektóre mutacje, które nie zmieniają bezpośrednio cysteiny, wydają się wywoływać podobne problemy z fałdowaniem zależne od tych mostków disiarczkowych.
Test świetlny na zniekształcone białka
Aby poszukać sposobów naprawy wadliwego NOTCH3, badacze użyli czułego narzędzia laboratoryjnego opracowanego wcześniej: systemu raportera typu split-luciferase nazwanego LSL-NOTCH3. W tym układzie fragmenty białka NOTCH3 są połączone między dwiema połówkami enzymu emitującego światło. Gdy NOTCH3 jest produkowany, prawidłowo fałdowany i wydzielany z komórek, połówki enzymu łączą się ponownie i generują silny sygnał świetlny w otaczającym płynie. Gdy białko fałduje się nieprawidłowo, produkcja i wydzielanie spadają, a emisja światła maleje. Drugie pomiar w tym samym teście śledzi, jaka część białka ma poprawne mostki disiarczkowe, porównując światło przed i po chemicznym „odblokowaniu” ukrytych, nieprawidłowych wiązań. Razem te odczyty dostarczają szybkiego sposobu sprawdzenia, czy jakiekolwiek leczenie sprawia, że mutacyjny NOTCH3 zachowuje się bardziej jak jego zdrowy odpowiednik.
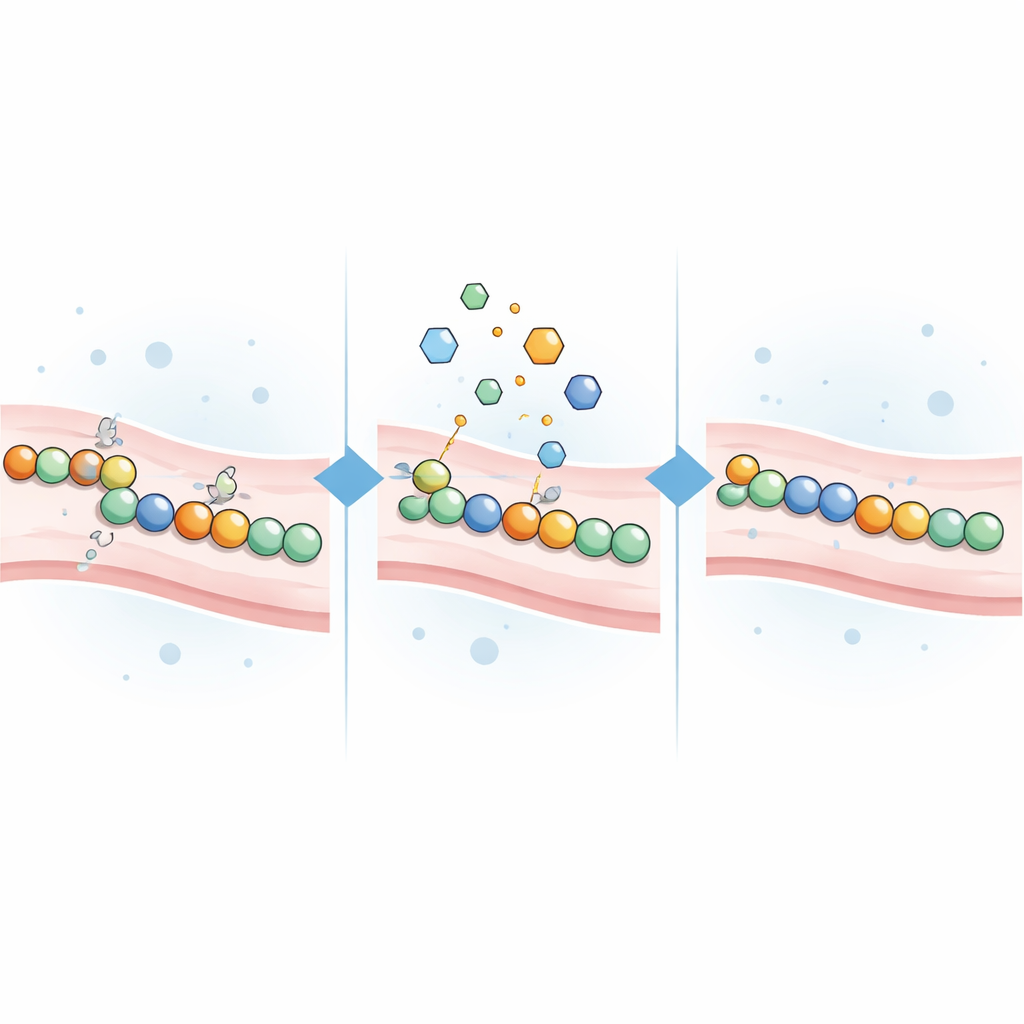
Testowanie związków reagujących z cysteiną jako naprawiaczy
Ponieważ mutacje w CADASIL często pozostawiają reszty cysteiny niepołączone, zespół przypuszczał, że małe cząsteczki reagujące z cysteiną mogą pomóc. Zgromadzili 21 związków reagujących z cysteiną, w tym klasyczne odczynniki laboratoryjne oraz kilka zatwierdzonych lub badanych leków pierwotnie opracowanych do leczenia nowotworów, chorób związanych z nadkwasotą żołądka lub innych schorzeń. Każdy związek dodano do komórek ekspresujących jedną z 16 różnych chorobotwórczych wariantów NOTCH3 obejmujących kilka regionów związanych z ryzykiem, a także do komórek ekspresujących warianty normalne lub łagodne. Następnie naukowcy zmierzyli, jak bardzo sygnał świetlny zmieniał się w odpowiedzi na każde leczenie.
Pojawiają się szeroko działające pomocniki
Więcej niż połowa przetestowanych związków poprawiła przynajmniej jeden chorobotwórczy wariant NOTCH3, a pięć związków zwiększyło główny sygnał świetlny w połowie lub więcej mutantów. Wśród nich najsilniejsze i najszersze efekty wykazały disulfiram, znany lek stosowany w uzależnieniu od alkoholu, oraz auranofina, lek zawierający złoto stosowany w reumatoidalnym zapaleniu stawów. Związki te nie tylko zwiększały całkowitą emisję światła, co sugeruje lepszą produkcję i wydzielanie białka, lecz także poprawiały ułamek białka o korzystnych wzorcach wiązań disiarczkowych. Co ważne, nie miały wpływu na normalny NOTCH3, co sugeruje pewną wybiórczość wobec form nieprawidłowo sfałdowanych. Dodatkowe eksperymenty wykazały, że chemikalia musiały być obecne podczas syntezy białka w komórkach i nie działały na białko już wydzielone, co wskazuje, że prawdopodobnie działają podczas fałdowania wewnątrz komórki.
Poza jednym genem i jedną mutacją
Badacze sprawdzili, czy korzyść związków reagujących z cysteiną zależy od konkretnego aminokwasu, który zastąpił cysteinę w mutacji. Poprzez systematyczne podstawianie różnych reszt w kluczowych pozycjach stwierdzili, że disulfiram i powiązany związek nadal poprawiały aktywność raportera w niemal wszystkich przypadkach. Wspiera to ideę, że leki celują w wspólny problem brakujących par cystein, a nie w konkretną zamianę. Przetestowali też drugi, niezależny system raportujący oparty na innym projekcie split-luciferazy i potwierdzili, że disulfiram podobnie zwiększał wydzielanie mutantarnych fragmentów NOTCH3, ale nie formy normalnej. Gdy zwrócono się do innego białka bogatego w cysteiny związanego z zespołem Marfana, FBN1, disulfiram pomógł tylko kilku mutantom, auranofina nie pomogła żadnemu, co sugeruje, że NOTCH3 w CADASIL może być szczególnie podatny na tę strategię.
Co to może znaczyć dla przyszłych terapii
Praca ta pokazuje, że możliwe jest częściowe skorygowanie zachowania wielu różnych mutantów NOTCH3 przy użyciu szeroko reagujących z cysteiną małych cząsteczek, w tym leków już stosowanych klinicznie w innych chorobach. Wyniki wskazują na ujednolicający mechanizm, w którym dodatkowe lub odsłonięte reszty cysteiny w mutacyjnym NOTCH3 napędzają szkodliwe nieprawidłowe fałdowanie, a „zamykanie” tych reaktywnych miejsc może przywrócić bardziej normalne fałdowanie i wydzielanie białka. Chociaż wyniki pochodzą z modeli komórkowych, a nie jeszcze od pacjentów czy w badaniach na zwierzętach, stanowią one podstawę do opracowania lub repurposingowania leków celujących w cysteinę jako potencjalnych terapii dla CADASIL i pokrewnych zaburzeń małych naczyń mózgowych.
Cytowanie: Cartee, N.M.P., Zhang, X., Lee, S.J. et al. Cysteine-reactive mitigators of small vessel disease-related NOTCH3 mutants. Sci Rep 16, 14300 (2026). https://doi.org/10.1038/s41598-026-45103-1
Słowa kluczowe: CADASIL, mutacje NOTCH3, choroba małych naczyń, leki celujące w cysteinę, zaginanie białek