Clear Sky Science · it
Mitigatori reattivi alla cisteina per i mutanti NOTCH3 legati alla malattia dei piccoli vasi
Perché questo studio sui vasi sanguigni cerebrali è importante
La malattia dei piccoli vasi cerebrali è una causa principale di ictus e demenza, eppure molte forme ereditarie non hanno terapie. Una di queste condizioni, chiamata CADASIL, è provocata da alterazioni in una singola proteina nelle pareti delle piccole arterie cerebrali, che portano a un danno progressivo nell’arco di decenni. Questo studio esplora se piccole molecole simili a farmaci possono spingere quella proteina difettosa verso una conformazione più sana, suggerendo un nuovo approccio per rallentare o prevenire la malattia nelle persone portatrici di varianti genetiche a rischio.
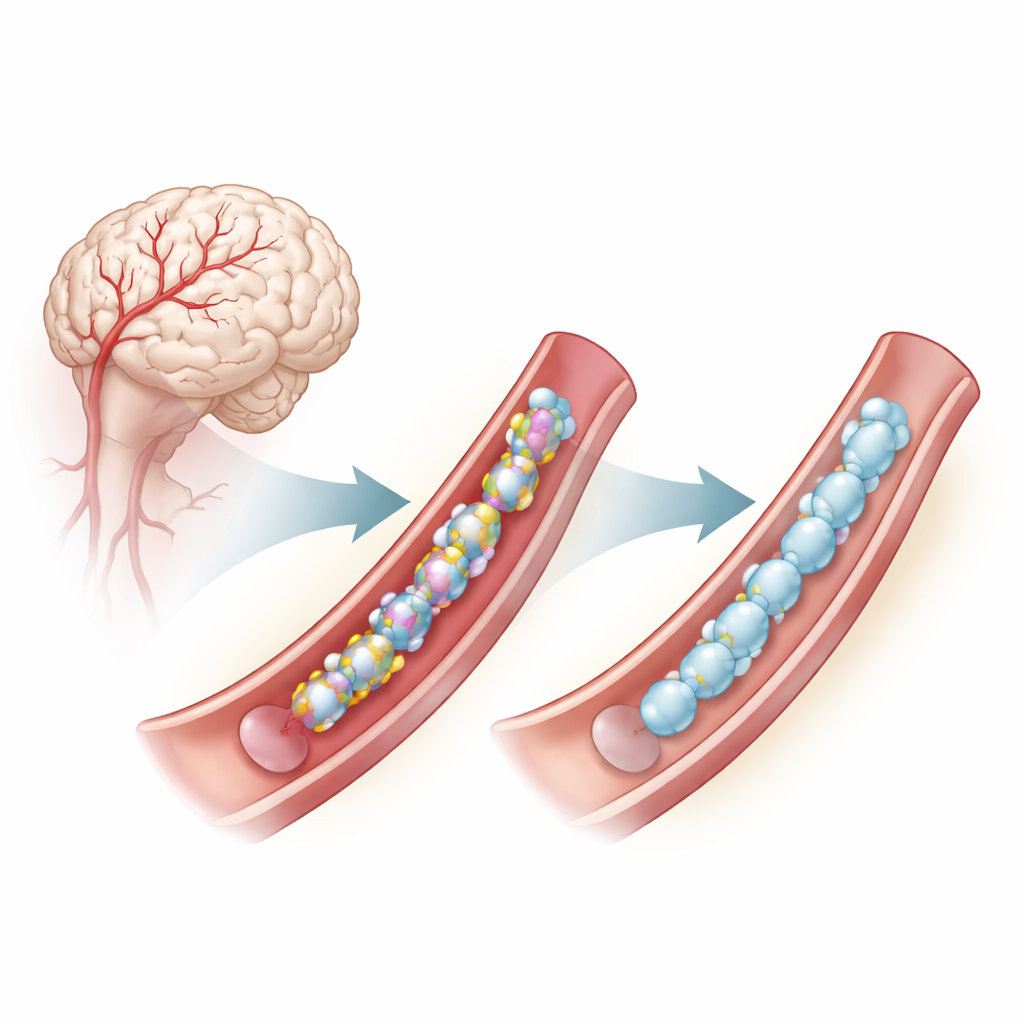
Un problema in profondità nelle pareti dei vasi cerebrali
La CADASIL è causata da mutazioni in un gene chiamato NOTCH3, attivo nelle cellule muscolari lisce che rivestono le piccole arterie cerebrali. Queste mutazioni spesso modificano il numero o la posizione di un particolare elemento costituente, la cisteina, all’interno di segmenti ripetuti della proteina NOTCH3. Le unità di cisteina normalmente si accoppiano formando legami disolfuro, microscopici ponti chimici che aiutano la proteina a piegarsi correttamente. Quando il numero di cisteine è scorretto, NOTCH3 tende a malripiegarsi, aggregarsi fuori dalle cellule e compromettere la funzione vascolare, contribuendo a ictus precoci e declino cognitivo. Anche alcune mutazioni che non cambiano direttamente la cisteina sembrano provocare problemi di malripiegamento simili dipendenti da questi legami disolfuro.
Un test basato sulla luce per proteine deformate
Per cercare modi per recuperare NOTCH3 difettoso, i ricercatori hanno utilizzato uno strumento di laboratorio sensibile che avevano sviluppato in precedenza: un sistema reportere split-luciferasi chiamato LSL-NOTCH3. In questo approccio, porzioni della proteina NOTCH3 sono fuse tra due metà di un enzima che emette luce. Quando NOTCH3 viene sintetizzato, ripiegato e secreto correttamente dalle cellule, le metà enzimatiche si ricongiungono e producono un forte segnale luminoso nel liquido circostante. Quando la proteina è malripiegata, la produzione e la secrezione diminuiscono e l’emissione luminosa cala. Una seconda misurazione nello stesso saggio monitora quanta della proteina presenta i corretti legami disolfuro confrontando la luce prima e dopo lo “sblocco” chimico di legami anomali nascosti. Queste letture insieme forniscono un modo rapido per capire se un trattamento fa comportare i mutanti NOTCH3 più come la forma sana.
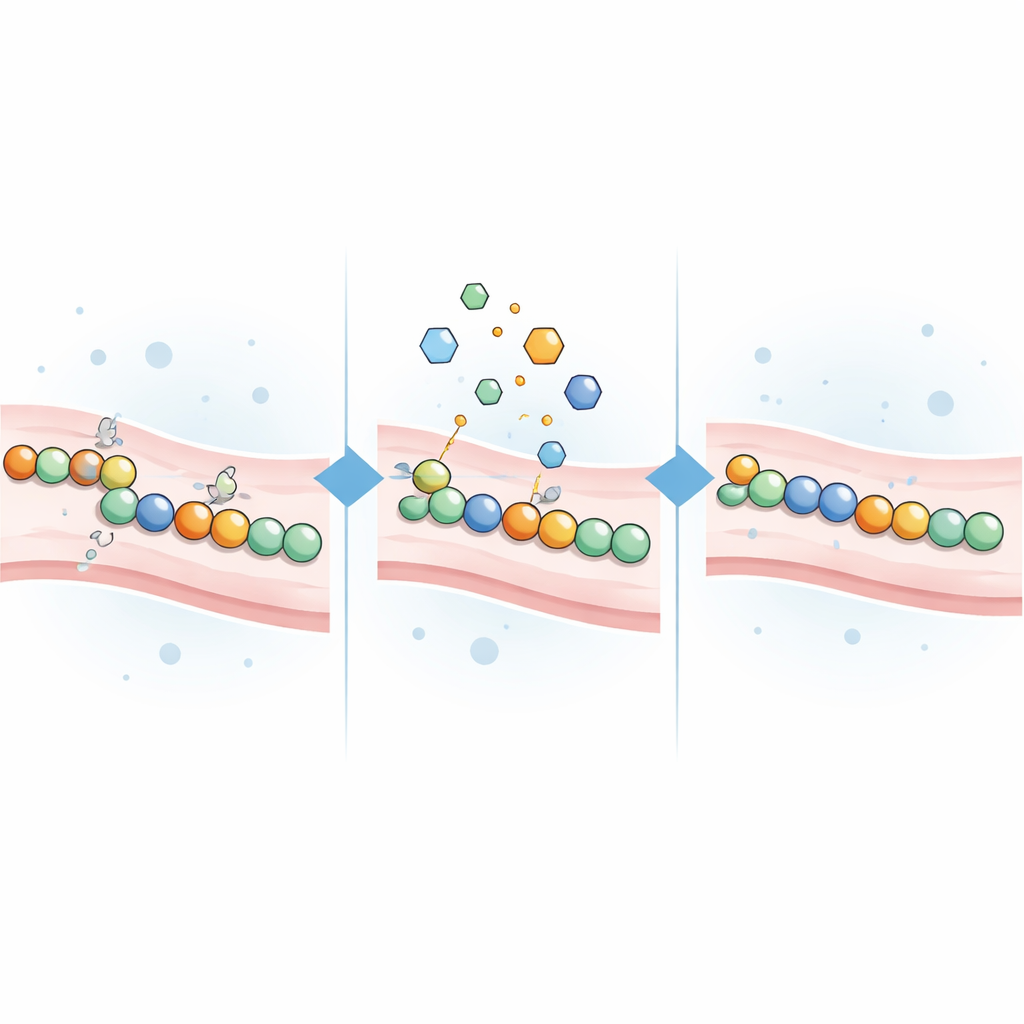
Testare composti che cercano la cisteina come correttivi
Poiché le mutazioni tipiche della CADASIL spesso lasciano gruppi di cisteina non appaiati, il team ha ipotizzato che piccole molecole reattive verso la cisteina potrebbero aiutare. Hanno assemblato 21 composti reattivi alla cisteina, includendo reagenti di laboratorio classici e diversi farmaci approvati o in fase di studio originariamente sviluppati per il cancro, disturbi dell’acido gastrico o altre condizioni. Ogni composto è stato aggiunto a cellule che esprimevano una delle 16 diverse varianti NOTCH3 causa di malattia che coprono varie regioni associate al rischio, così come a cellule che esprimevano varianti normali o innocue. Gli scienziati hanno quindi misurato quanto il segnale luminoso cambiasse in risposta a ciascun trattamento.
Emergono aiutanti ad ampio spettro dallo screening
Più della metà dei composti testati ha migliorato almeno una variante NOTCH3 patogenica, e cinque sostanze hanno aumentato il segnale luminoso primario in metà o più dei mutanti. Tra queste, gli effetti più forti e diffusi sono stati osservati con disulfiram, un farmaco consolidato per la dipendenza da alcol, e auranofin, un farmaco contenente oro usato per l’artrite reumatoide. Questi composti non solo hanno aumentato l’emissione luminosa complessiva, suggerendo una migliore produzione e secrezione della proteina, ma hanno anche migliorato la frazione di proteina con modelli di legame disolfuro favorevoli. È importante che non abbiano mostrato effetto sul NOTCH3 normale, implicando una certa selettività per le forme malripiegate. Esperimenti aggiuntivi hanno mostrato che i chimici dovevano essere presenti mentre le cellule sintetizzavano la proteina, e non funzionavano sulla proteina già secreta, indicando che probabilmente agiscono durante il ripiegamento intracellulare.
Oltre un gene e una mutazione
I ricercatori hanno verificato se il beneficio dei composti reattivi alla cisteina dipendesse dall’amminoacido specifico che sostituisce la cisteina in una mutazione. Sostituendo sistematicamente molti residui diversi in posizioni chiave, hanno scoperto che disulfiram e un composto correlato miglioravano ancora l’attività del reporter in quasi tutti i casi. Ciò supporta l’idea che i farmaci mirino al problema comune delle coppie di cisteina mancanti, piuttosto che a una sostituzione particolare. Hanno inoltre testato un secondo sistema di reporting indipendente basato su un diverso disegno split-luciferasi e confermato che il disulfiram aumentava in modo analogo la secrezione di frammenti mutanti di NOTCH3 ma non della forma normale. Quando hanno esaminato un’altra proteina ricca di cisteine coinvolta nella sindrome di Marfan, FBN1, il disulfiram ha aiutato solo pochi mutanti e l’auranofin non ha aiutato nessuno, suggerendo che NOTCH3 nella CADASIL può essere particolarmente suscettibile a questa strategia.
Cosa potrebbe significare per future terapie
Questo lavoro mostra che è possibile correggere parzialmente il comportamento di molte diverse mutazioni NOTCH3 usando piccole molecole ampiamente reattive verso la cisteina, inclusi farmaci già in uso clinico per altre malattie. I risultati indicano un meccanismo unificante in cui gruppi di cisteina in eccesso o esposti nei NOTCH3 mutati guidano il malripiegamento dannoso, e dove il “capping” di questi siti reattivi può ripristinare un ripiegamento e una secrezione più normali della proteina. Sebbene questi risultati provengano da modelli cellulari e non ancora da studi su pazienti o animali, gettano le basi per sviluppare o riutilizzare farmaci che mirano la cisteina come potenziali terapie per CADASIL e disordini correlati dei piccoli vasi cerebrali.
Citazione: Cartee, N.M.P., Zhang, X., Lee, S.J. et al. Cysteine-reactive mitigators of small vessel disease-related NOTCH3 mutants. Sci Rep 16, 14300 (2026). https://doi.org/10.1038/s41598-026-45103-1
Parole chiave: CADASIL, mutazioni NOTCH3, malattia dei piccoli vasi, farmaci che mirano la cisteina, malripiegamento proteico