Clear Sky Science · ar
مخففات تفاعلية مع السيستئين لِطفرات NOTCH3 المرتبطة بمرض الأوعية الدموية الصغيرة
لماذا تهم هذه الدراسة لأوعية الدماغ الصغيرة
يعد مرض الأوعية الدموية الدماغية الصغيرة سببًا رئيسيًا للسكتة الدماغية والخَرَف، ومع ذلك لا تتوفر علاجات للعديد من الأشكال الوراثية منه. أحد هذه الاضطرابات، المسمى CADASIL، ينتج عن تغييرات في بروتين واحد في جدران الشرايين الدماغية الدقيقة، مما يؤدي إلى تلف تدريجي على مدى عقود. تستقصي هذه الدراسة ما إذا كانت بعض الجزيئات الصغيرة الشبيهة بالأدوية يمكنها دفع ذلك البروتين المعيب نحو شكل أكثر صحة، مما يوحي بطريقة جديدة لإبطاء المرض أو منعه لدى الأشخاص الحاملين لمتغيرات جينية عالية المخاطر.
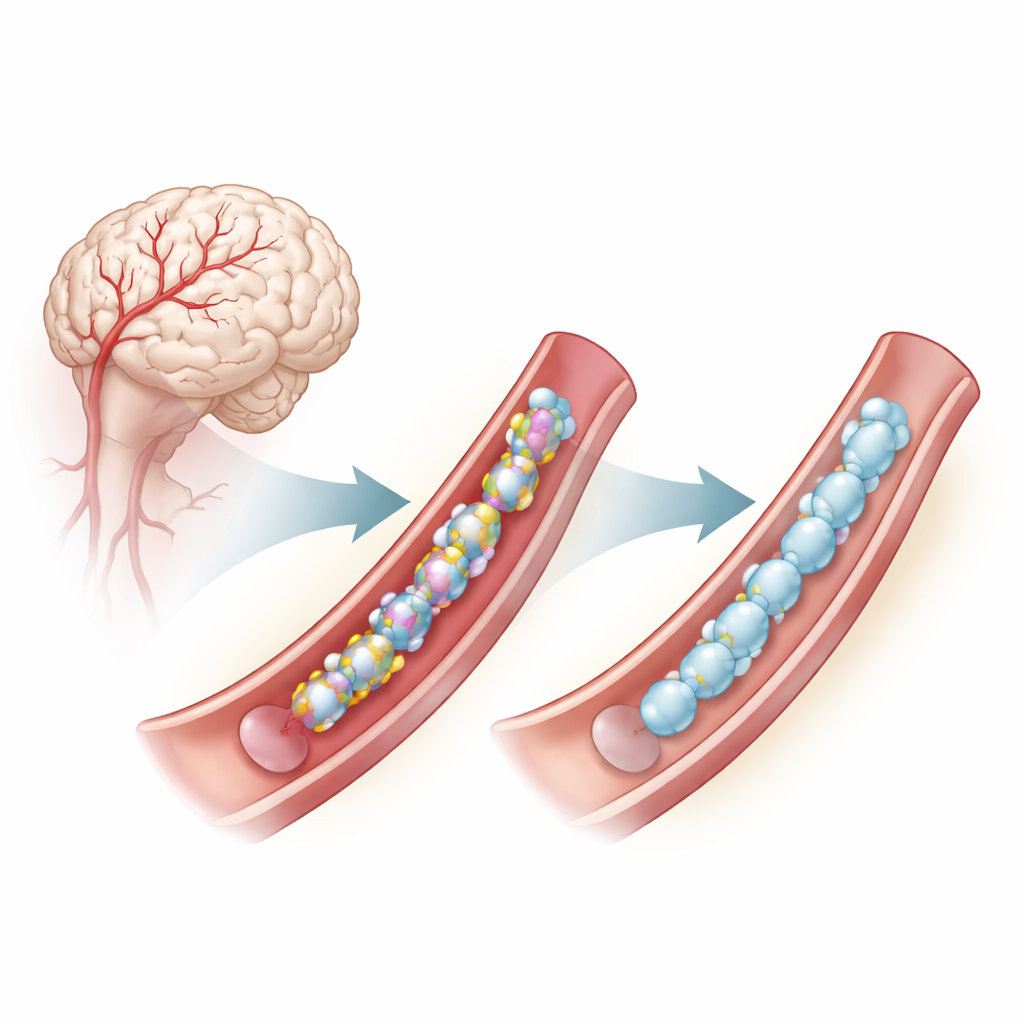
مشكلة عميقة داخل جدران أوعية الدماغ
ينجم CADASIL عن طفرات في جين يُدعى NOTCH3، وهو نشط في خلايا العضلات الملساء التي تبطن الشرايين الدماغية الصغيرة. غالبًا ما تغير هذه الطفرات عدد أو موضع وحدة بناء معينة هي السيستئين داخل مقاطع مكررة من بروتين NOTCH3. عادةً ما تتزاوج وحدات السيستئين لتكوّن روابط كبريتيدية (روابط ثنائي الكبريت)، وهي جسور كيميائية صغيرة تساعد البروتين على الطي الصحيح. عندما يكون عدد السيستئين غير صحيح، يميل NOTCH3 إلى الطي الخاطئ والتجمع خارج الخلايا وتعطيل وظيفة الأوعية الدموية، مما يسهم في سكتات مبكرة وتراجع إدراكي. حتى بعض الطفرات التي لا تغير السيستئين مباشرة يبدو أنها تخلق مشاكل طي مماثلة تعتمد على هذه الروابط الكبريتيدية.
اختبار قائم على الضوء للكشف عن البروتينات المشوهة
للبحث عن طرق لإنقاذ NOTCH3 المعيب، استخدم الباحثون أداة مختبرية حساسة طوروها سابقًا: نظام مراسل لوسيفيراز مقسوم يسمى LSL-NOTCH3. في هذا الإعداد، تُدمَج أجزاء من بروتين NOTCH3 بين نصفَي إنزيم باعث للضوء. عندما يُنتَج NOTCH3 ويُطوى ويُفرَز بشكل صحيح من الخلايا، تعود أنصاف الإنزيم لتتحد وتنتج إشارة ضوئية قوية في السائل المحيط. عند طي البروتين بشكل خاطئ، ينخفض الإنتاج والإفراز، وتنخفض شدة الضوء. يقيس القياس الثاني في نفس الفحص مقدار البروتين الذي يحمل الروابط الكبريتيدية الصحيحة بمقارنة الضوء قبل وبعد "فتح" الروابط غير الطبيعية كيميائيًا. معًا، توفر هذه القراءات وسيلة سريعة لمعرفة ما إذا كان أي علاج يجعل NOTCH3 الطافر يتصرف بشكل أقرب إلى نظيره السليم.
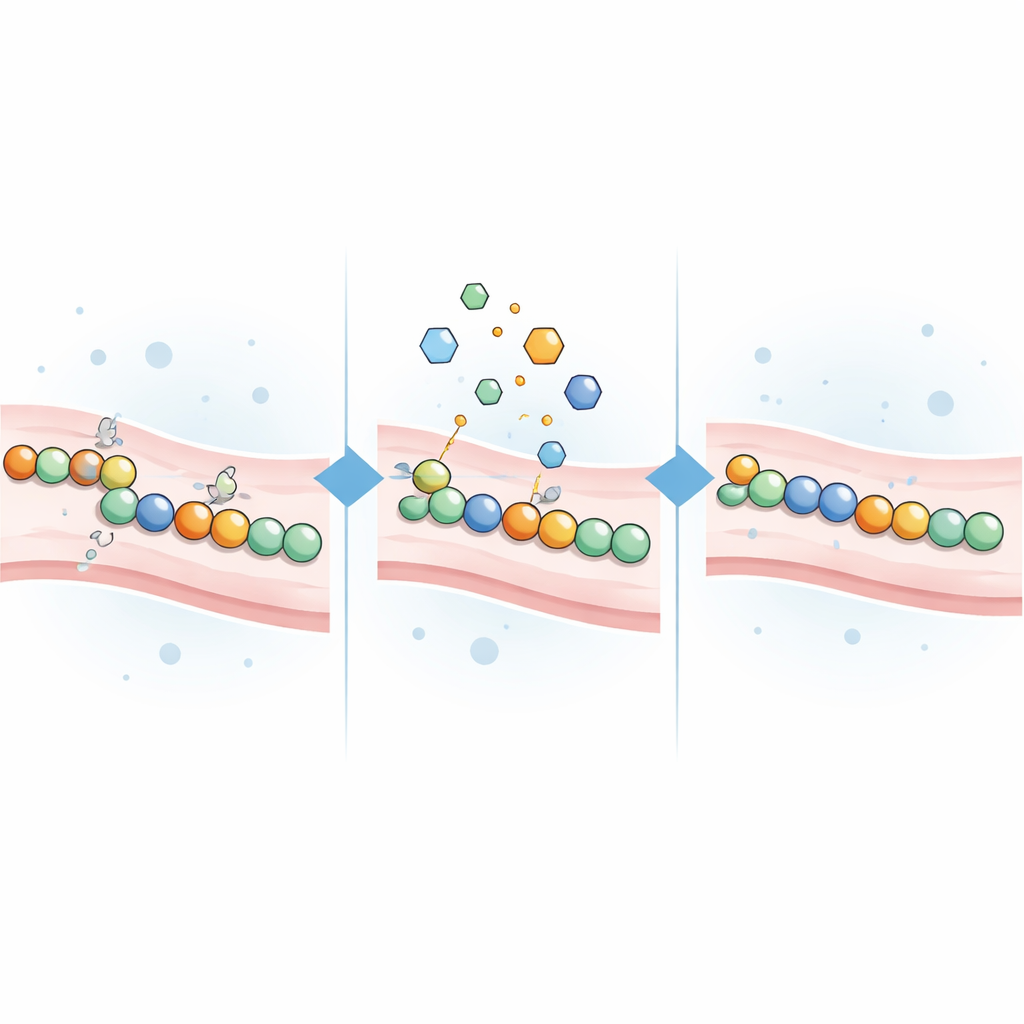
اختبار مركبات تتجه إلى السيستئين كعلاجات محتملة
نظرًا لأن طفرات CADASIL غالبًا ما تترك مجموعات سيستئين غير متزاوجة، افترض الفريق أن جزيئات صغيرة تتفاعل مع السيستئين قد تساعد. جمعوا 21 مركبًا تفاعليًا مع السيستئين، بما في ذلك كواشف مختبرية تقليدية وعدة أدوية مرخَّصة أو تجريبية طورت في الأصل لعلاج السرطان أو اضطرابات حموضة المعدة أو حالات أخرى. أُضيف كل مركب إلى خلايا تعبر عن أحد 16 متغيرًا ممرضًا مختلفًا من NOTCH3 تمتد عبر مناطق مرتبطة بالمخاطر في البروتين، وكذلك إلى خلايا تعبر عن متغيرات طبيعية أو حميدة. ثم قاس العلماء مقدار تغير إشارة الضوء استجابةً لكل علاج.
ظهور مذيّلين ذوي تأثير واسع من الفحص
حسّن أكثر من نصف المركبات المختبرة على الأقل أحد متغيرات NOTCH3 الممرضة، وعزَّز خمسة من هذه المواد الإشارة الضوئية الأساسية في نصف المتغيرات أو أكثر. من بين هذه، جاءت أقوى وأوسع التأثيرات من ديسلفرام، وهو دواء معروف لمُعالجة الاعتماد على الكحول، وأورانوفين، دواء يحتوي على الذهب ويستخدم في التهاب المفاصل الروماتويدي. لم تزد هذه المركبات فقط من إجمالي خرج الضوء، ما يوحي بتحسن الإنتاج والإفراز البروتيني، بل حسَّنت أيضًا نسبة البروتين الحاملة لروابط كبريتيدية مواتية. ومن المهم أنها لم تؤثر على NOTCH3 الطبيعي، مما يوحي بوجود انتقائية معينة للأشكال المطوية بشكل خاطئ. أظهرت تجارب إضافية أن المركبات يجب أن تكون موجودة أثناء تصنيع الخلايا للبروتين، ولم تعمل على البروتين المفرَز وحده، مما يشير إلى أنها تعمل على الأرجح أثناء الطي داخل الخلية.
أبعد من جين واحد وطفرَة واحدة
سأل الباحثون ما إذا كانت فائدة المركبات التفاعلية مع السيستئين تعتمد على الحمض الأميني الذي استبدل السيستئين في الطفرة. من خلال استبدال منظّم للعديد من البقايا عند مواقع رئيسية بشكل منهجي، وجدوا أن ديسلفرام ومركبًا ذا صلة لا يزالان يحسنان نشاط المراسل في جميع الحالات تقريبًا. يدعم هذا الفكرة القائلة بأن الأدوية تستهدف المشكلة المشتركة المتمثلة في أزواج السيستئين المفقودة، بدل أن تكون مرتبطة باستبدال معين. اختبروا أيضًا نظام مراسل مستقل ثانٍ قائم على تصميم لوسيفيراز مقسوم مختلف وأكدوا أن ديسلفرام عزَّز كذلك إفراز شظايا NOTCH3 الطافرة لكن ليس الشكل الطبيعي. عندما توجهوا إلى بروتين غني بالسيستئين آخر مشارك في متلازمة مارفان، FBN1، ساعد ديسلفرام بعض الطفرات فقط ولم يساعد أورانوفين أيًا منها، مما يوحي بأن NOTCH3 في CADASIL قد يكون عرضة بشكل خاص لهذه الاستراتيجية.
ماذا قد يعني هذا للعلاجات المستقبلية
تُظهر هذه الدراسة أنه من الممكن تصحيح سلوك العديد من طفرات NOTCH3 جزئيًا باستخدام جزيئات صغيرة تفاعلية مع السيستئين على نطاق واسع، بما في ذلك أدوية مستخدمة سريريًا بالفعل لأمراض أخرى. تشير النتائج إلى آلية موحدة حيث تقود مجموعات السيستئين الزائدة أو المكشوفة في NOTCH3 الطافر إلى طي ضار، وأن تغطية هذه المواقع التفاعلية يمكن أن تستعيد طي البروتين وإفرازه إلى نمط أقرب للطبيعي. بينما تستند هذه النتائج إلى نماذج خلوية وليس إلى مرضى أو دراسات حيوانية بعد، فإنها تمهد الطريق لتطوير أو إعادة توظيف أدوية تستهدف السيستئين كعلاجات محتملة لـ CADASIL واضطرابات ذات صلة في أوعية الدماغ الصغيرة.
الاستشهاد: Cartee, N.M.P., Zhang, X., Lee, S.J. et al. Cysteine-reactive mitigators of small vessel disease-related NOTCH3 mutants. Sci Rep 16, 14300 (2026). https://doi.org/10.1038/s41598-026-45103-1
الكلمات المفتاحية: CADASIL, طفرات NOTCH3, مرض الأوعية الدموية الصغيرة, أدوية تستهدف السيستئين, طي البروتين الخاطئ