Clear Sky Science · ru
Реактивные к цистеину препараты, смягчающие эффект мутантов NOTCH3, связанных с заболеванием мелких сосудов
Почему это исследование кровеносных сосудов мозга важно
Церебральное заболевание мелких сосудов — одна из основных причин инсульта и деменции, однако для множества наследственных форм нет лечения. Одна из таких болезней, известная как CADASIL, вызывается изменениями в одном белке в стенках крошечных артерий мозга и приводит к прогрессирующему повреждению на протяжении десятилетий. В этом исследовании выясняют, могут ли небольшие лекарственно-подобные молекулы подтолкнуть дефектный белок к более здоровой форме, что открывает перспективу нового способа замедлить или предотвратить болезнь у носителей рискованных вариантов гена.
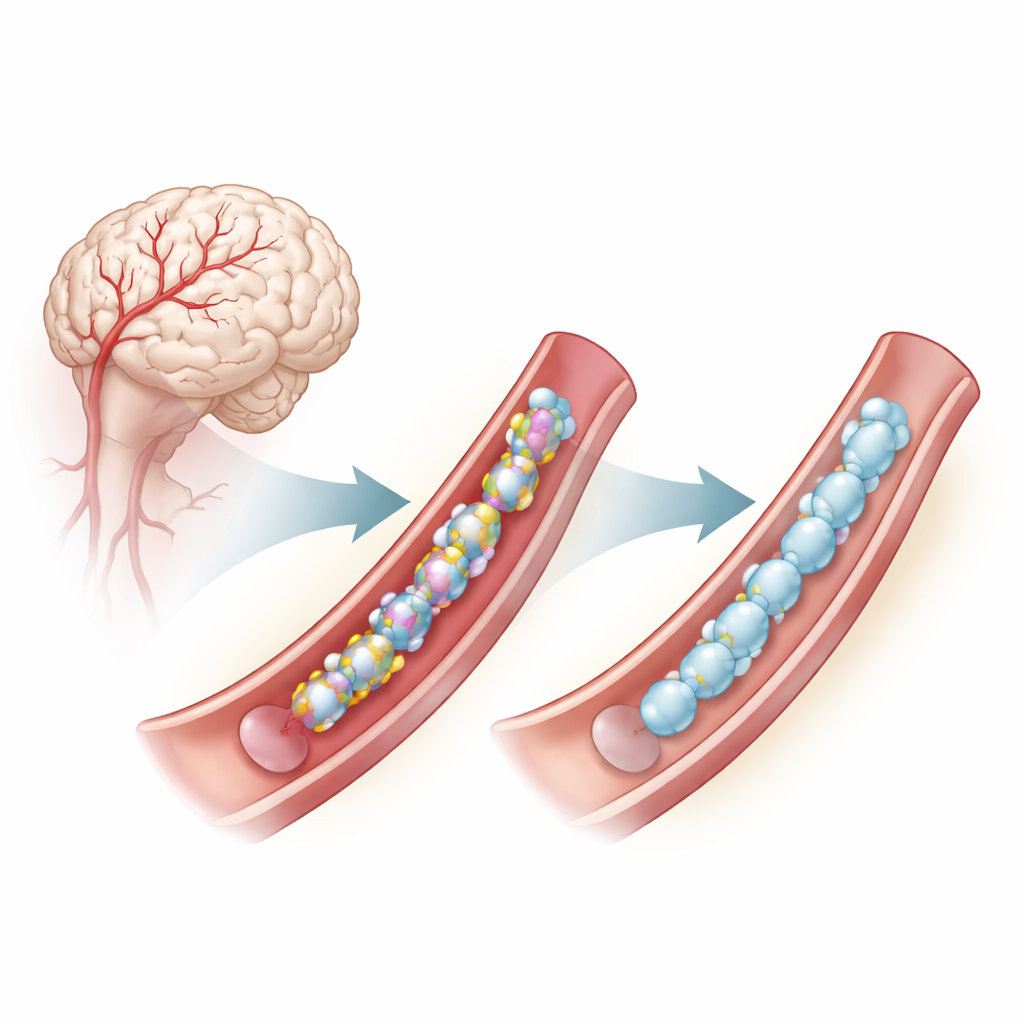
Проблема глубоко в стенках сосудов мозга
CADASIL вызван мутациями в гене NOTCH3, который активен в гладкомышечных клетках, выстилающих мелкие артерии мозга. Часто эти мутации изменяют количество или расположение одного из аминокислотных компонентов — цистеина — в повторяющихся сегментах белка NOTCH3. Мономеры цистеина обычно образуют пары и дисульфидные мостики, небольшие химические связи, помогающие белку правильно сворачиваться. Когда количество цистеинов нарушено, NOTCH3 склонен к неправильному сворачиванию, образованию агрегатов вне клеток и нарушению функции сосудов, что способствует ранним инсультам и когнитивному снижению. Даже некоторые мутации, которые напрямую не меняют цистеин, похоже, вызывают схожие проблемы со сворачиванием, зависящие от дисульфидных связей.
Световой тест для деформированных белков
Чтобы найти способы восстановить нормальное поведение NOTCH3, исследователи использовали чувствительный лабораторный инструмент, ранее разработанный ими: систему сплит-люциферазного репортера LSL-NOTCH3. В этой схеме фрагменты белка NOTCH3 сращены между двумя половинками светопротеина. Когда NOTCH3 синтезируется, правильно сворачивается и секретируется из клетки, половинки фермента соединяются и дают сильный световой сигнал в окружающей среде. При неправильном сворачивании продуцирование и секреция снижаются, и светоотдача падает. Второй показатель в том же анализе фиксирует долю белка с правильными дисульфидными связями, сравнивая свет до и после химического «отмыкания» скрытых, аномальных связей. Вместе эти измерения дают быстрый способ увидеть, делает ли какое-либо лечение мутантный NOTCH3 более похожим на здоровый вариант.
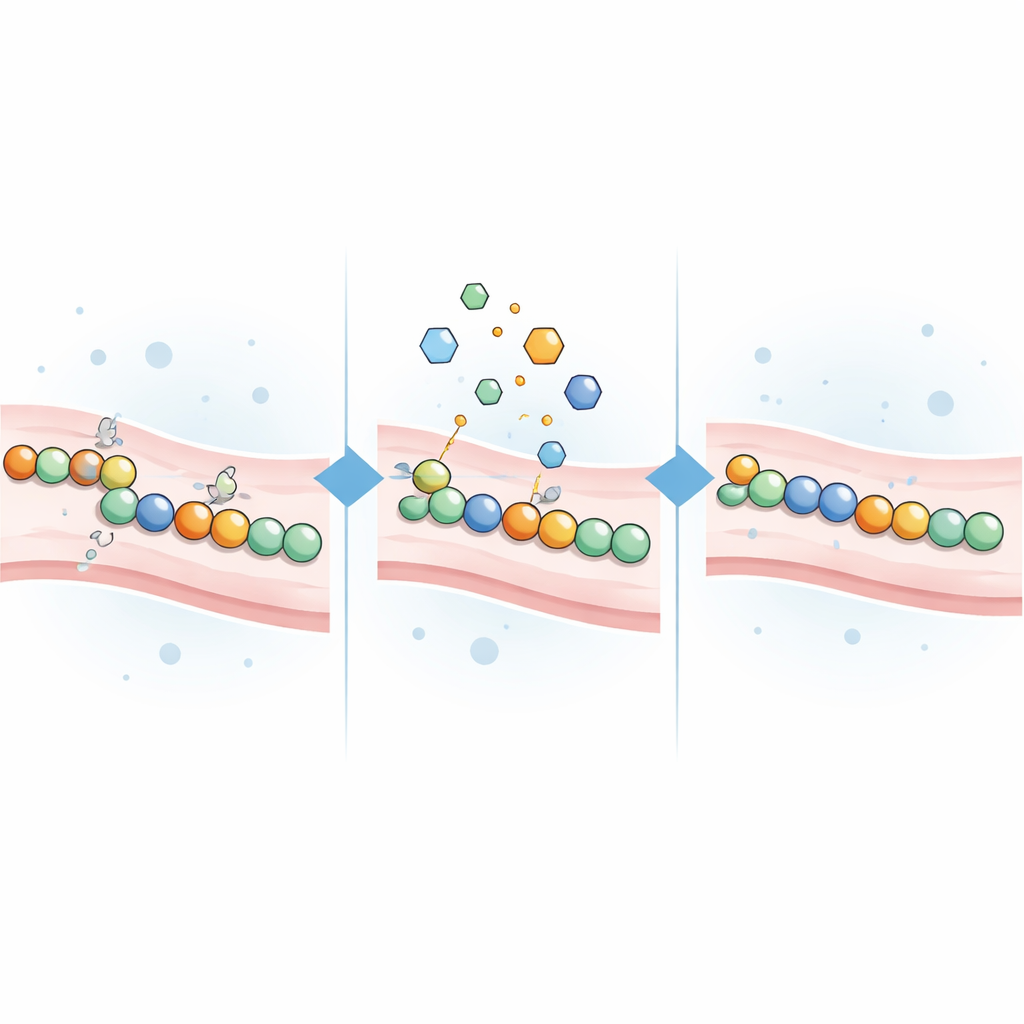
Проверка реагентов, ищущих цистеин, как исправителей
Поскольку мутации при CADASIL часто оставляют цистеиновые группы несопряжёнными, команда предположила, что малые молекулы, реагирующие с цистеином, могут помочь. Они собрали коллекцию из 21 цистеин-реактивного соединения, включая классические лабораторные реагенты и несколько одобренных или исследуемых препаратов, изначально разработанных для лечения рака, нарушений желудочной кислотности и других состояний. Каждый соединение добавляли в клетки, экспрессирующие один из 16 различных патогенных вариантов NOTCH3, охватывающих несколько областей, связанных с риском, а также в клетки, экспрессирующие нормальные или безвредные варианты. Затем учёные измеряли, насколько изменялся световой сигнал в ответ на каждое лечение.
В скрининге выявились широкодействующие помощники
Более половины протестированных соединений улучшили по крайней мере один патогенный вариант NOTCH3, а пять химикатов повысили основной световой сигнал в половине или более мутантов. Среди них наиболее сильные и широкие эффекты были от дисульфирама — проверенного препарата для лечения алкогольной зависимости — и аурофина — содержащего золото препарата, применявшегося при ревматоидном артрите. Эти соединения не только увеличивали общий световой сигнал, что указывает на улучшение синтеза и секреции белка, но и повышали долю белка с благоприятным рисунком дисульфидных связей. Важно, что они не оказывали эффекта на нормальный NOTCH3, что подразумевает некоторую селективность по отношению к неправильно свернувшимся формам. Дополнительные эксперименты показали, что химикаты должны присутствовать в период синтеза белка в клетке и не действовали на уже секретированный белок, что указывает на их действие в процессе сворачивания внутри клетки.
Не ограничиваясь одним геном и одной мутацией
Исследователи поинтересовались, зависит ли польза от цистеин-реактивных соединений от той аминокислоты, которая замещает цистеин в мутации. Путём систематической замены множества различных остатков в ключевых позициях они обнаружили, что дисульфирам и родственное соединение по-прежнему улучшали активность репортера во почти всех случаях. Это подтверждает идею, что препараты нацелены на общую проблему отсутствия пар цистеинов, а не на конкретную замену. Они также проверили вторую, независимую систему репортера на основе другой конструкции сплит-люциферазы и подтвердили, что дисульфирам аналогично усиливал секрецию фрагментов мутантного NOTCH3, но не нормальной формы. Когда же исследователи обратились к другому цистеин-обогащённому белку, вовлечённому в синдром Марфана — FBN1, — дисульфирам помог лишь нескольким мутантам, а аурофин не помог вовсе, что предполагает, что NOTCH3 при CADASIL может быть особенно уязвим для этой стратегии.
Что это может значить для будущего лечения
Эта работа показывает, что возможно частично восстановить поведение многих различных мутантов NOTCH3 с помощью широкодействующих цистеин-реактивных малых молекул, включая препараты, уже применяемые при других заболеваниях. Результаты указывают на объединяющий механизм, в котором лишние или экспонированные группы цистеина в мутантном NOTCH3 приводят к вредному неправильному сворачиванию, а «запирание» этих реактивных сайтов способно восстановить более нормальное сворачивание и секрецию белка. Хотя эти данные получены в клеточных моделях, а не у пациентов или на животных, они прокладывают путь к разработке или переназначению препаратов, нацеленных на цистеин, как потенциальной терапии CADASIL и связанных расстройств мелких сосудов мозга.
Цитирование: Cartee, N.M.P., Zhang, X., Lee, S.J. et al. Cysteine-reactive mitigators of small vessel disease-related NOTCH3 mutants. Sci Rep 16, 14300 (2026). https://doi.org/10.1038/s41598-026-45103-1
Ключевые слова: CADASIL, мутации NOTCH3, заболевание мелких сосудов, препараты, нацеленные на цистеин, свёртывание белка