Clear Sky Science · pt
Mitigadores reativos à cisteína de mutantes NOTCH3 relacionados à doença dos pequenos vasos
Por que este estudo sobre vasos sanguíneos cerebrais é importante
A doença cerebral dos pequenos vasos é uma causa importante de AVC e demência, e muitas formas hereditárias ainda não têm tratamento. Uma dessas condições, chamada CADASIL, é causada por alterações em uma única proteína nas paredes de pequenas artérias cerebrais, levando a danos progressivos ao longo de décadas. Este estudo investiga se certos pequenos compostos semelhantes a fármacos podem orientar essa proteína defeituosa de volta a uma conformação mais saudável, sugerindo uma nova forma de retardar ou prevenir a doença em pessoas que carregam variantes genéticas de risco.
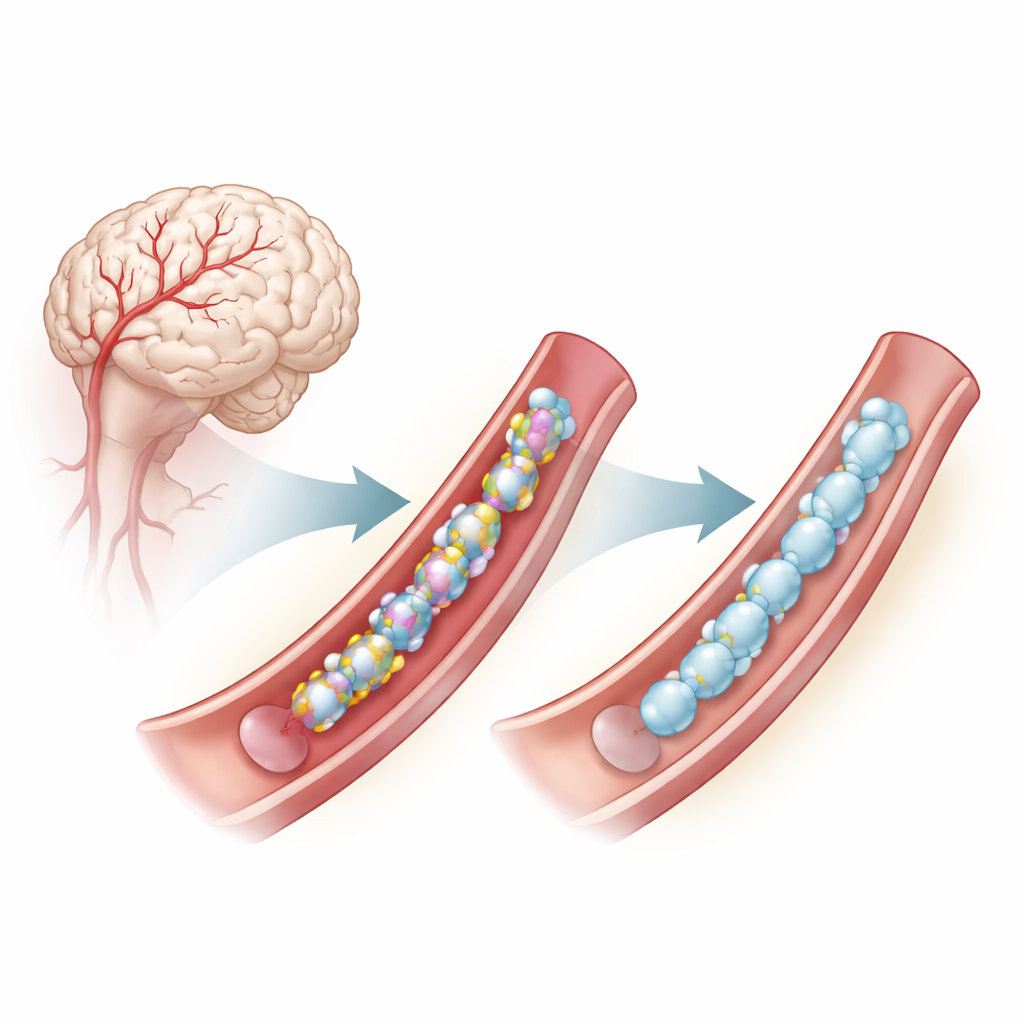
Um problema no interior das paredes dos vasos cerebrais
CADASIL é causado por mutações em um gene chamado NOTCH3, que é ativo nas células musculares lisas que revestem pequenas artérias cerebrais. Essas mutações frequentemente alteram o número ou a posição de um determinado bloco de construção, a cisteína, dentro de segmentos repetidos da proteína NOTCH3. As unidades de cisteína normalmente se emparelham para formar ligações dissulfeto, pequenas pontes químicas que ajudam a proteína a se dobrar corretamente. Quando o número de cisteínas está errado, o NOTCH3 tende a se desnaturar, aglutinar-se fora das células e prejudicar a função dos vasos sanguíneos, contribuindo para AVCs precoces e declínio cognitivo. Mesmo algumas mutações que não alteram diretamente a cisteína parecem gerar problemas semelhantes de desnaturação dependentes dessas pontes dissulfeto.
Um teste baseado em luz para proteínas deformadas
Para buscar formas de resgatar o NOTCH3 defeituoso, os pesquisadores usaram uma ferramenta laboratorial sensível que haviam desenvolvido anteriormente: um sistema repórter de luciferase dividido chamado LSL-NOTCH3. Nesse arranjo, fragmentos da proteína NOTCH3 são fundidos entre duas metades de uma enzima que emite luz. Quando o NOTCH3 é produzido, dobrado e secretado corretamente pelas células, as metades da enzima se recombinam e produzem um forte sinal luminoso no meio líquido. Quando a proteína se desnatura, a produção e secreção caem, e a emissão de luz diminui. Uma segunda medida no mesmo ensaio avalia quanto da proteína tem as ligações dissulfeto corretas, comparando a luz antes e depois de “destrancar” quimicamente ligações anormais e ocultas. Juntos, esses sinais fornecem uma maneira rápida de ver se algum tratamento faz com que o NOTCH3 mutante se comporte mais como sua versão saudável.
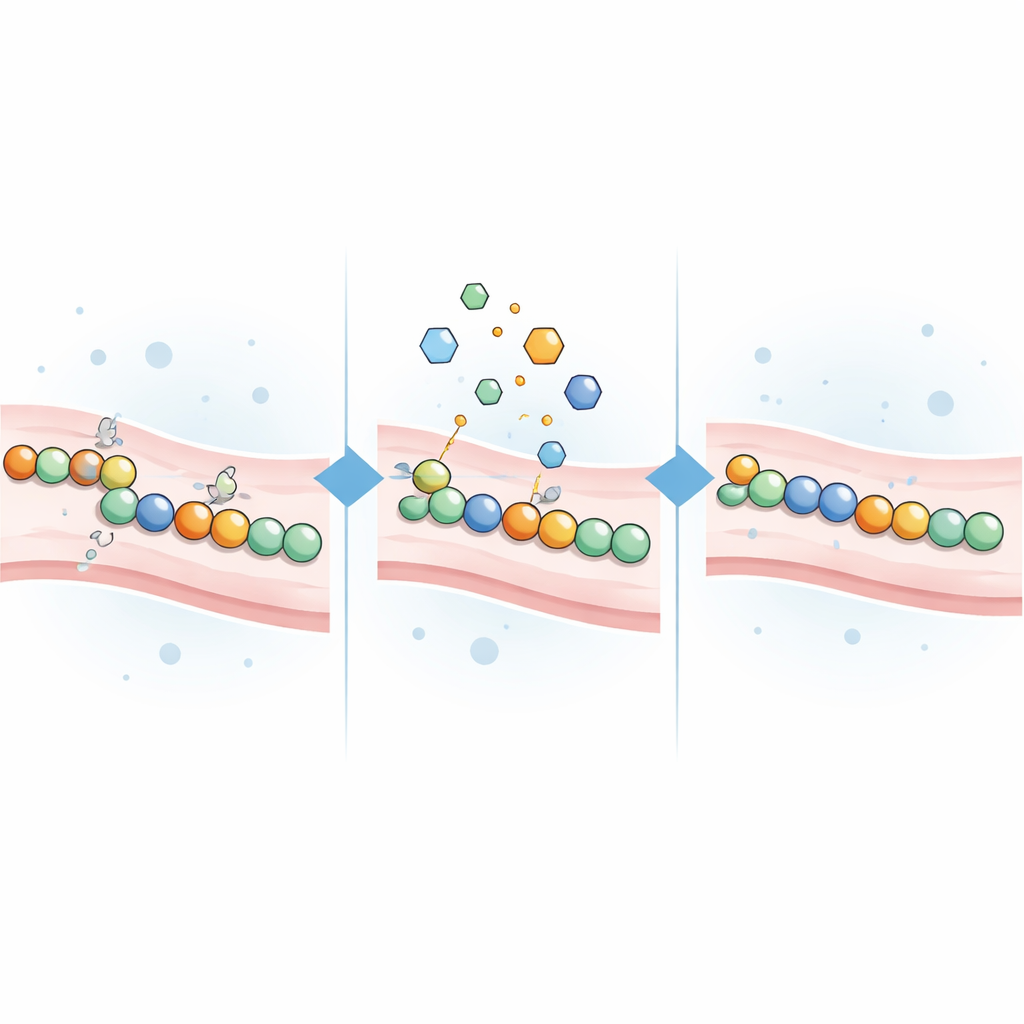
Testando químicos que buscam cisteína como reparadores
Porque as mutações de CADASIL frequentemente deixam grupos de cisteína desemparelhados, a equipe raciocinou que pequenas moléculas que reagem com cisteína poderiam ajudar. Eles reuniram 21 compostos reativos à cisteína, incluindo reagentes clássicos de laboratório e vários fármacos aprovados ou em investigação originalmente desenvolvidos para câncer, distúrbios de ácido estomacal ou outras condições. Cada composto foi adicionado a células que expressavam uma de 16 variantes diferentes de NOTCH3 causadoras de doença, abrangendo várias regiões associadas ao risco da proteína, bem como a células que expressavam variantes normais ou inócuas. Os cientistas então mediram quanto o sinal luminoso mudou em resposta a cada tratamento.
Surgem auxiliares de ação ampla a partir da triagem
Mais da metade dos compostos testados melhorou pelo menos uma variante patogênica de NOTCH3, e cinco químicos aumentaram o sinal luminoso primário em metade ou mais dos mutantes. Entre eles, os efeitos mais fortes e abrangentes vieram do dissulfiram, um fármaco estabelecido para dependência alcoólica, e do auranofina, um medicamento contendo ouro usado para artrite reumatoide. Esses compostos não apenas aumentaram a emissão total de luz, sugerindo melhor produção e secreção da proteína, mas também melhoraram a fração de proteína com padrões de ligação dissulfeto favoráveis. Importante, eles não tiveram efeito sobre o NOTCH3 normal, o que implica certa seletividade para as formas desnaturadas. Experimentos adicionais mostraram que os químicos precisavam estar presentes enquanto as células produziam a proteína, e não funcionavam na proteína já secretada, indicando que provavelmente atuam durante o dobramento dentro da célula.
Além de um gene e de uma mutação
Os pesquisadores investigaram se o benefício dos compostos reativos à cisteína dependia do aminoácido específico que substituiu a cisteína na mutação. Ao substituir sistematicamente muitos resíduos diferentes em posições-chave, eles descobriram que o dissulfiram e um composto relacionado ainda aumentavam a atividade do repórter em quase todos os casos. Isso apoia a ideia de que os medicamentos estão atingindo o problema comum das pares de cisteína ausentes, em vez de qualquer substituição particular. Eles também testaram um segundo sistema repórter independente baseado em um design diferente de luciferase dividida e confirmaram que o dissulfiram também aumentou a secreção de fragmentos mutantes de NOTCH3, mas não da forma normal. Ao avaliar outra proteína rica em cisteína envolvida na síndrome de Marfan, FBN1, o dissulfiram ajudou apenas alguns mutantes e o auranofina não ajudou nenhum, sugerindo que o NOTCH3 em CADASIL pode ser especialmente suscetível a essa estratégia.
O que isso pode significar para tratamentos futuros
Este trabalho mostra que é possível corrigir parcialmente o comportamento de muitas variantes diferentes de NOTCH3 usando pequenas moléculas amplamente reativas à cisteína, incluindo fármacos já em uso clínico para outras doenças. As descobertas apontam para um mecanismo unificador em que grupos extras ou expostos de cisteína no NOTCH3 mutante promovem o desenovelamento prejudicial, e onde o bloqueio desses locais reativos pode restaurar um dobramento e secreção mais normais da proteína. Embora esses resultados tenham sido obtidos em modelos celulares e ainda não em pacientes ou estudos animais, eles estabelecem a base para desenvolver ou reproporcionar drogas direcionadas à cisteína como potenciais terapias para CADASIL e distúrbios relacionados dos pequenos vasos cerebrais.
Citação: Cartee, N.M.P., Zhang, X., Lee, S.J. et al. Cysteine-reactive mitigators of small vessel disease-related NOTCH3 mutants. Sci Rep 16, 14300 (2026). https://doi.org/10.1038/s41598-026-45103-1
Palavras-chave: CADASIL, mutações em NOTCH3, doença dos pequenos vasos, fármacos direcionados à cisteína, desenovelamento proteico