Clear Sky Science · es
Mitigadores reactivos a la cisteína de mutantes de NOTCH3 relacionados con la enfermedad de pequeños vasos
Por qué importa este estudio sobre los vasos sanguíneos cerebrales
La enfermedad cerebral de pequeños vasos es una causa principal de ictus y demencia, y muchas formas hereditarias carecen de tratamiento. Una de ellas, denominada CADASIL, está provocada por cambios en una única proteína en las paredes de las pequeñas arterias cerebrales, lo que conduce a un daño progresivo durante décadas. Este estudio explora si ciertos compuestos pequeños con carácter farmacológico pueden empujar esa proteína defectuosa hacia una conformación más saludable, lo que sugiere una nueva vía para frenar o prevenir la enfermedad en personas que portan variantes genéticas de riesgo.
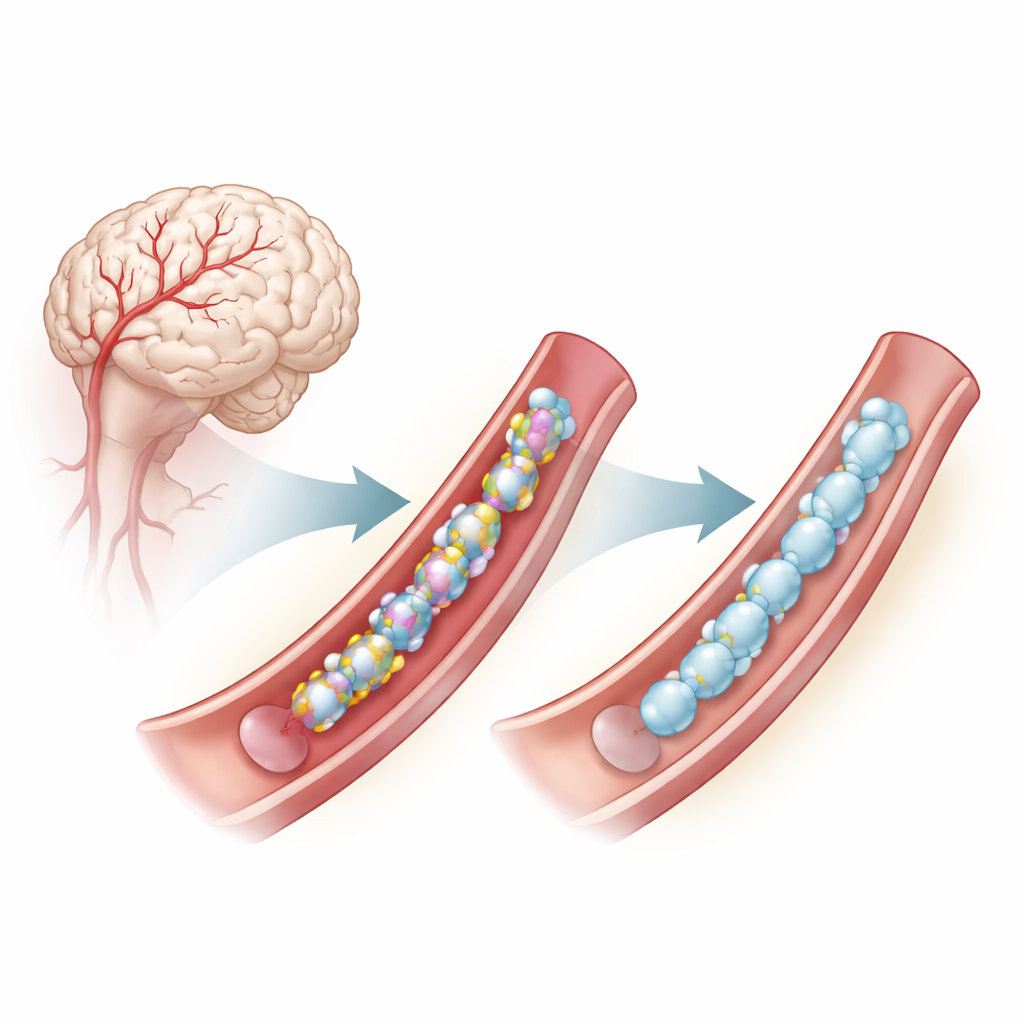
Un problema en lo profundo de las paredes de los vasos cerebrales
CADASIL se debe a mutaciones en un gen llamado NOTCH3, que está activo en las células musculares lisas que recubren las pequeñas arterias cerebrales. Estas mutaciones con frecuencia alteran el número o la posición de un residuo particular, la cisteína, dentro de segmentos repetidos de la proteína NOTCH3. Las unidades de cisteína normalmente se emparejan para formar enlaces disulfuro, pequeños puentes químicos que ayudan a que la proteína se pliegue correctamente. Cuando el número de cisteínas es incorrecto, NOTCH3 tiende a plegarse mal, agregarse fuera de las células y alterar la función vascular, contribuyendo a ictus prematuros y deterioro cognitivo. Incluso algunas mutaciones que no cambian directamente la cisteína parecen provocar problemas de plegamiento similares dependientes de estos enlaces disulfuro.
Una prueba basada en luz para detectar proteínas deformadas
Para buscar formas de rescatar el NOTCH3 defectuoso, los investigadores utilizaron una herramienta de laboratorio sensible que habían desarrollado previamente: un sistema reportero de luciferasa dividida llamado LSL-NOTCH3. En este montaje, fragmentos de la proteína NOTCH3 se fusionan entre dos mitades de una enzima emisora de luz. Cuando NOTCH3 se sintetiza, pliega y secreta correctamente desde las células, las mitades enzimáticas se reúnen y producen una señal lumínica intensa en el líquido circundante. Cuando la proteína se pliega mal, la producción y secreción disminuyen y la emisión de luz cae. Una segunda medición en el mismo ensayo monitoriza cuánta proteína presenta los enlaces disulfuro correctos comparando la luz antes y después de “desbloquear” químicamente enlaces anómalos ocultos. En conjunto, estas lecturas proporcionan una forma rápida de ver si algún tratamiento hace que NOTCH3 mutante se comporte más como su contraparte sana.
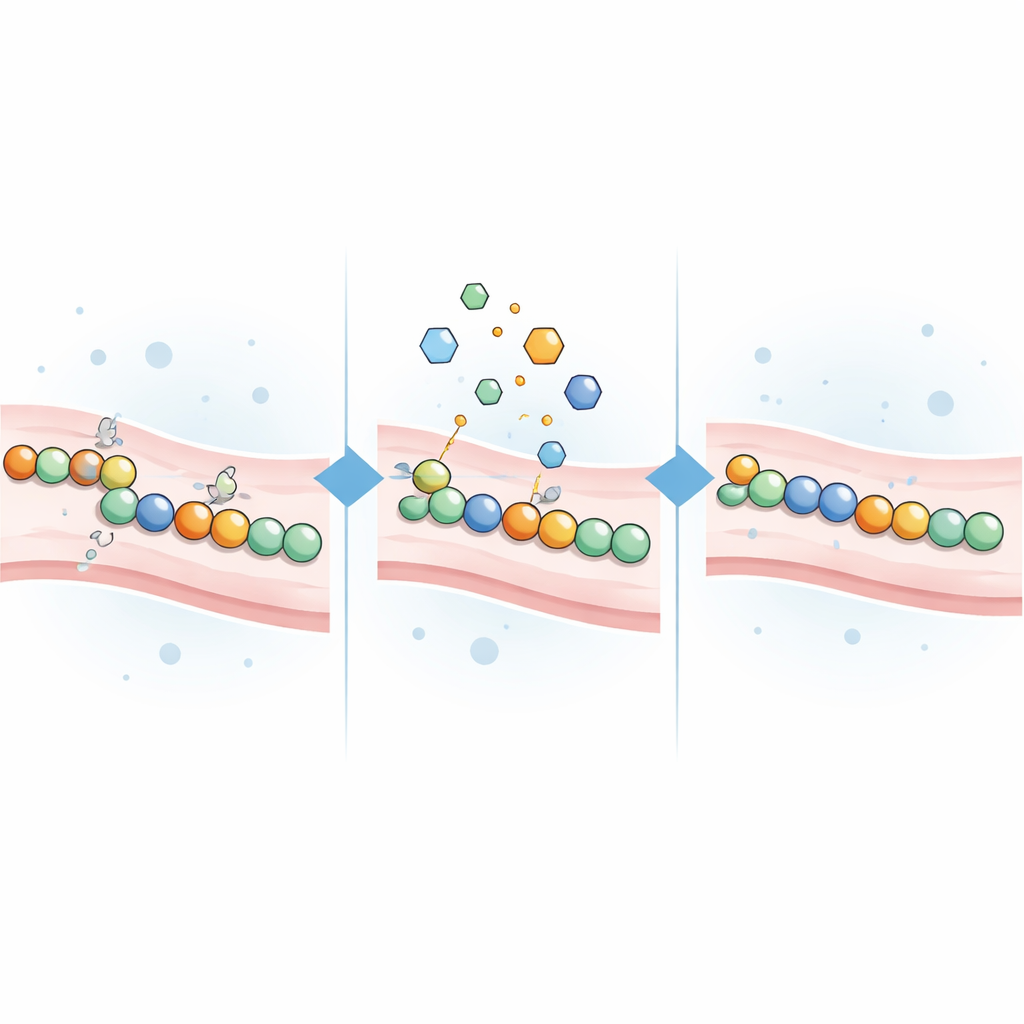
Poniendo a prueba compuestos que buscan cisteínas como reparadores
Puesto que las mutaciones de CADASIL con frecuencia dejan grupos de cisteína sin emparejar, el equipo supuso que pequeñas moléculas reactivas frente a la cisteína podrían ayudar. Reunieron 21 compuestos reactivos a la cisteína, incluidos reactivos clásicos de laboratorio y varios fármacos aprobados o en investigación desarrollados inicialmente para el cáncer, trastornos del ácido gástrico u otras enfermedades. Cada compuesto se añadió a células que expresaban una de 16 variantes diferentes de NOTCH3 causantes de enfermedad, que abarcaban varias regiones vinculadas al riesgo de la proteína, así como a células que expresaban variantes normales o inocuas. Los científicos midieron entonces cuánto cambiaba la señal lumínica en respuesta a cada tratamiento.
Salen a la luz ayudantes de amplio espectro
Más de la mitad de los compuestos probados mejoraron al menos una variante patogénica de NOTCH3, y cinco incrementaron la señal lumínica principal en la mitad o más de las variantes. Entre ellos, los efectos más fuertes y amplios provinieron de disulfiram, un fármaco establecido para la dependencia al alcohol, y auranofín, un medicamento que contiene oro usado en la artritis reumatoide. Estos compuestos no solo aumentaron la emisión lumínica global, lo que sugiere mejor producción y secreción de la proteína, sino que también mejoraron la fracción de proteína con patrones de enlaces disulfuro favorables. Es importante que no afectaron al NOTCH3 normal, lo que implica cierta selectividad por las formas mal plegadas. Experimentos adicionales mostraron que los químicos debían estar presentes mientras las células sintetizaban la proteína y no funcionaban sobre la proteína ya secretada, lo que indica que probablemente actúan durante el plegamiento dentro de la célula.
Más allá de un gen y una mutación
Los investigadores examinaron si el beneficio de los compuestos reactivos a la cisteína dependía del aminoácido específico que reemplazaba a la cisteína en una mutación. Al sustituir sistemáticamente muchos residuos diferentes en posiciones clave, encontraron que disulfiram y un compuesto relacionado seguían mejorando la actividad del reportero en casi todos los casos. Esto respalda la idea de que los fármacos se dirigen al problema común de pares de cisteína faltantes, en lugar de a un reemplazo concreto. También evaluaron un segundo sistema reportero independiente basado en un diseño diferente de luciferasa dividida y confirmaron que disulfiram también aumentaba la secreción de fragmentos mutantes de NOTCH3 pero no del tipo normal. Cuando pasaron a otra proteína rica en cisteína implicada en el síndrome de Marfan, FBN1, disulfiram ayudó solo a unos pocos mutantes y auranofín no ayudó a ninguno, lo que sugiere que NOTCH3 en CADASIL puede ser especialmente susceptible a esta estrategia.
Qué puede significar esto para futuros tratamientos
Este trabajo demuestra que es posible corregir parcialmente el comportamiento de muchas variantes diferentes de NOTCH3 usando pequeñas moléculas de acción amplia reactivas a la cisteína, incluidos fármacos ya en uso clínico para otras enfermedades. Los hallazgos apuntan a un mecanismo unificador en el que grupos de cisteína adicionales o expuestos en NOTCH3 mutante provocan un plegamiento perjudicial, y donde bloquear esos sitios reactivos puede restaurar un plegamiento y secreción más normales. Aunque estos resultados proceden de modelos celulares y aún no de pacientes o estudios en animales, sientan las bases para desarrollar o reutilizar fármacos dirigidos a la cisteína como posibles terapias para CADASIL y trastornos relacionados de los pequeños vasos cerebrales.
Cita: Cartee, N.M.P., Zhang, X., Lee, S.J. et al. Cysteine-reactive mitigators of small vessel disease-related NOTCH3 mutants. Sci Rep 16, 14300 (2026). https://doi.org/10.1038/s41598-026-45103-1
Palabras clave: CADASIL, mutaciones de NOTCH3, enfermedad de pequeños vasos, fármacos dirigidos a la cisteína, desplegamiento proteico