Clear Sky Science · nl
Cysteïne-reactieve mitigatoren van NOTCH3-mutaties gerelateerd aan kleinevatenziekte
Waarom deze studie van hersenbloedvaten ertoe doet
Cerebrale kleinevatenziekte is een belangrijke oorzaak van beroerte en dementie, maar voor veel erfelijke vormen bestaat geen behandeling. Eén aandoening, CADASIL genoemd, wordt veroorzaakt door veranderingen in een enkel eiwit in de wanden van kleine hersenarteriën, wat over tientallen jaren leidt tot progressieve schade. Deze studie onderzoekt of bepaalde kleine, geneesmiddelenachtige chemicaliën het defecte eiwit weer in een gezondere vorm kunnen brengen, wat wijst op een nieuwe manier om ziekte bij dragers van risicovarianten te vertragen of te voorkomen.
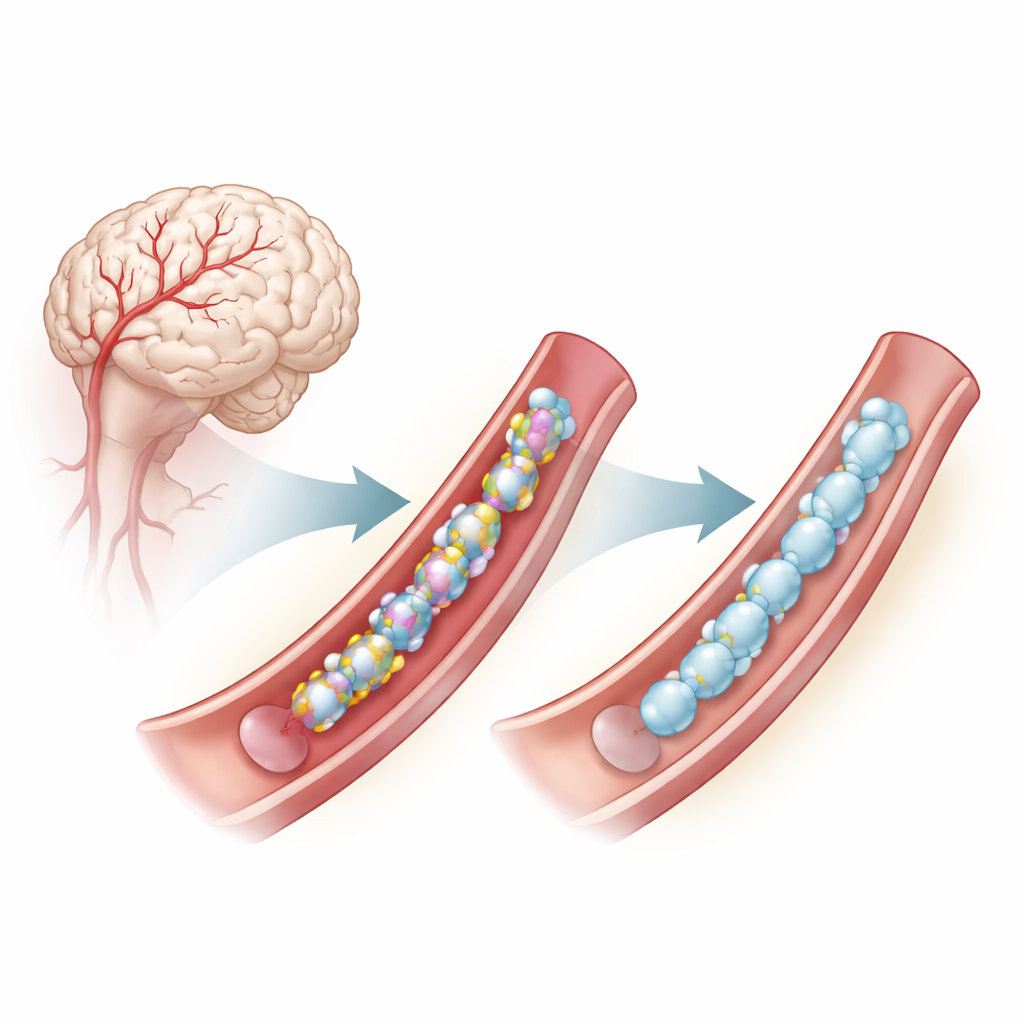
Een probleem diep in de wanden van hersenbloedvaten
CADASIL wordt veroorzaakt door mutaties in een gen dat NOTCH3 heet en dat actief is in de gladde spiercellen die kleine hersenarteriën bekleden. Deze mutaties veranderen vaak het aantal of de plaats van een specifieke bouwsteen, cysteïne, binnen herhaalde segmenten van het NOTCH3-eiwit. Cysteïne-eenheden koppelen zich normaal gesproken om disulfidebruggen te vormen, kleine chemische verbindingen die helpen dat het eiwit correct vouwt. Wanneer het aantal cysteïnes niet klopt, heeft NOTCH3 de neiging fout te vouwen, buiten de cellen te klonteren en de functie van bloedvaten te verstoren, wat bijdraagt aan vroege beroertes en cognitieve achteruitgang. Zelfs sommige mutaties die niet rechtstreeks cysteïne veranderen, lijken vergelijkbare vouwproblemen te veroorzaken die afhankelijk zijn van deze disulfidebruggen.
Een lichtgebaseerde test voor misvormde eiwitten
Om naar manieren te zoeken om defect NOTCH3 te herstellen, gebruikten de onderzoekers een gevoelig laboratoriuminstrument dat ze eerder ontwikkelden: een split-luciferase-rapporteursysteem genaamd LSL-NOTCH3. In dit systeem zijn delen van het NOTCH3-eiwit gefuseerd tussen twee helften van een lichtgevende enzym. Wanneer NOTCH3 correct wordt gemaakt, gevouwen en uitgescheiden door cellen, voegen de enzymhelften zich weer samen en produceren ze een sterk lichtsignaal in het omliggende medium. Wanneer het eiwit fout vouwt, nemen productie en secretie af en daalt de lichtoutput. Een tweede meting in dezelfde assay volgt hoeveel van het eiwit de juiste disulfidebruggen heeft door licht te vergelijken vóór en na het chemisch "ontgrendelen" van verborgen, abnormale bruggen. Samen bieden deze aflezingen een snelle manier om te zien of een behandeling mutant NOTCH3 meer als de gezonde variant doet gedragen.
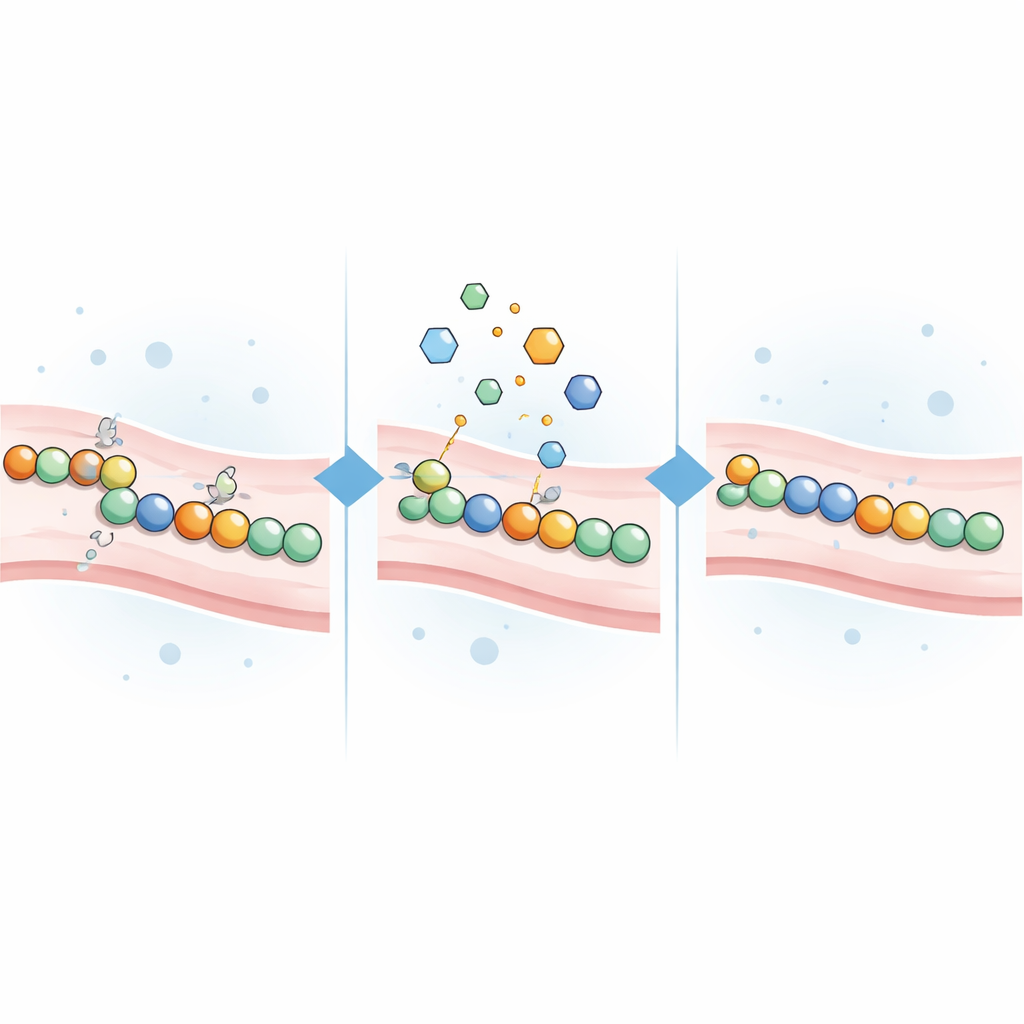
Testen van cysteïne-zoekende chemicaliën als herstelmiddelen
Aangezien CADASIL-mutaties vaak cysteïnegroepen onvervuld achterlaten, veronderstelde het team dat kleine moleculen die met cysteïne reageren, kunnen helpen. Ze stelden 21 cysteïne-reactieve verbindingen samen, waaronder klassieke laboratoriumreagentia en verschillende goedgekeurde of experimentele geneesmiddelen oorspronkelijk ontwikkeld voor kanker, maagzuurgerelateerde aandoeningen of andere indicaties. Elk middel werd toegevoegd aan cellen die één van 16 verschillende ziekteveroorzakende NOTCH3-varianten tot expressie brachten, verspreid over meerdere risicogebieden van het eiwit, evenals aan cellen die normale of onschuldige varianten uitdrukten. De wetenschappers maten vervolgens hoeveel het lichtsignaal veranderde als reactie op elke behandeling.
Breedwerkende hulpverleners komen uit het scherm
Meer dan de helft van de geteste verbindingen verbeterde minstens één ziekteveroorzakende NOTCH3-variant, en vijf chemicaliën verhoogden het primaire lichtsignaal bij de helft of meer van de mutanten. Onder deze middelen waren de sterkste en meest algemene effecten afkomstig van disulfiram, een bekend middel tegen alcoholafhankelijkheid, en auranofin, een goudhoudend geneesmiddel dat wordt gebruikt bij reumatoïde artritis. Deze verbindingen verhoogden niet alleen de totale lichtopbrengst, wat wijst op verbeterde eiwitproductie en secretie, maar verbeterden ook het aandeel eiwit met gunstige disulfidebindingspatronen. Belangrijk is dat ze geen effect hadden op normaal NOTCH3, wat wijst op enige selectiviteit voor de foutgevouwen vormen. Aanvullende experimenten toonden aan dat de chemicaliën aanwezig moesten zijn terwijl cellen het eiwit maakten en niet werkten op reeds uitgescheiden eiwit alleen, wat aangeeft dat ze waarschijnlijk tijdens het vouwen binnen de cel werkzaam zijn.
Voorbij één gen en één mutatie
De onderzoekers vroegen zich af of het voordeel van cysteïne-reactieve verbindingen afhankelijk was van het specifieke aminozuur dat cysteïne in een mutatie verving. Door systematisch veel verschillende restgroepen op sleutelposities te substitueren, vonden ze dat disulfiram en een verwant verbinding de rapportage-activiteit in bijna alle gevallen nog steeds verbeterden. Dit ondersteunt het idee dat de middelen het gedeelde probleem van ontbrekende cysteïneparen aanpakken, in plaats van een specifieke vervanging. Ze testten ook een tweede, onafhankelijk rapportsysteem gebaseerd op een ander split-luciferase-ontwerp en bevestigden dat disulfiram op vergelijkbare wijze de secretie van mutante NOTCH3-fragmenten verbeterde, maar niet van de normale vorm. Toen ze naar een ander cysteïnerijk eiwit betrokken bij het Marfan-syndroom, FBN1, keken, hielp disulfiram slechts een paar mutanten en ondersteunde auranofin er geen, wat suggereert dat NOTCH3 bij CADASIL mogelijk bijzonder vatbaar is voor deze strategie.
Wat dit zou kunnen betekenen voor toekomstige behandelingen
Dit werk toont aan dat het mogelijk is het gedrag van veel verschillende NOTCH3-mutanten gedeeltelijk te corrigeren met breed cysteïne-reactieve kleine moleculen, waaronder middelen die al klinisch worden gebruikt voor andere ziekten. De bevindingen wijzen op een verenigend mechanisme waarin extra of blootgestelde cysteïnegroepen in mutant NOTCH3 schadelijke vouwing aandrijven, en waarin het afdekken van die reactieve plaatsen normaler vouwen en secretie kan herstellen. Hoewel deze resultaten afkomstig zijn uit celgebaseerde modellen en nog niet uit patiënten- of dierstudies, vormen ze de basis voor het ontwikkelen of herbestemmen van cysteïne-richtende geneesmiddelen als potentiële therapieën voor CADASIL en verwante aandoeningen van kleine hersenvaten.
Bronvermelding: Cartee, N.M.P., Zhang, X., Lee, S.J. et al. Cysteine-reactive mitigators of small vessel disease-related NOTCH3 mutants. Sci Rep 16, 14300 (2026). https://doi.org/10.1038/s41598-026-45103-1
Trefwoorden: CADASIL, NOTCH3-mutaties, kleinevatenziekte, cysteïne-richtende geneesmiddelen, eiwitverkeerde vouwing