Clear Sky Science · sv
ITPR3 främjar leverfibros genom att skada hepatocyter via Ca2+/NF-κB/LECT2‑vägen
Varför leverärrbildning spelar roll
Leversjukdom ökar globalt och utvecklas ofta tyst under många år innan symptom visar sig. En viktig vändpunkt är leverfibros — uppbyggnaden av ärrvävnad som så småningom kan leda till cirros och leversvikt. Denna studie ställer en avgörande fråga: vad driver den tidigaste skadan på levercellerna som sätter igång ärrbildningen, och skulle blockering av en enskild molekylär ”strömbrytare” kunna skydda levern mot långsiktig skada?
En närmare titt på hur levern skadas
Fibros börjar när leverns huvudceller, hepatocyterna, skadas upprepade gånger. I denna studie använde forskarna ett väl etablerat kemiskt ämne, tetrachlormetan, för att efterlikna kronisk leverskada hos möss och i odlade musleverceller. De behandlade mössen utvecklade kännetecken för leversjukdom som ses hos människor: förhöjda blodmarkörer för leverskada, störningar i fett- och kolesterolmetabolism, inflammation och omfattande avlagringar av ärrliknande material som förvränger leverns normala arkitektur. Dessa förändringar bekräftar att modellen troget återger kedjan av händelser som förvandlar enkel skada till bestående ärrbildning.
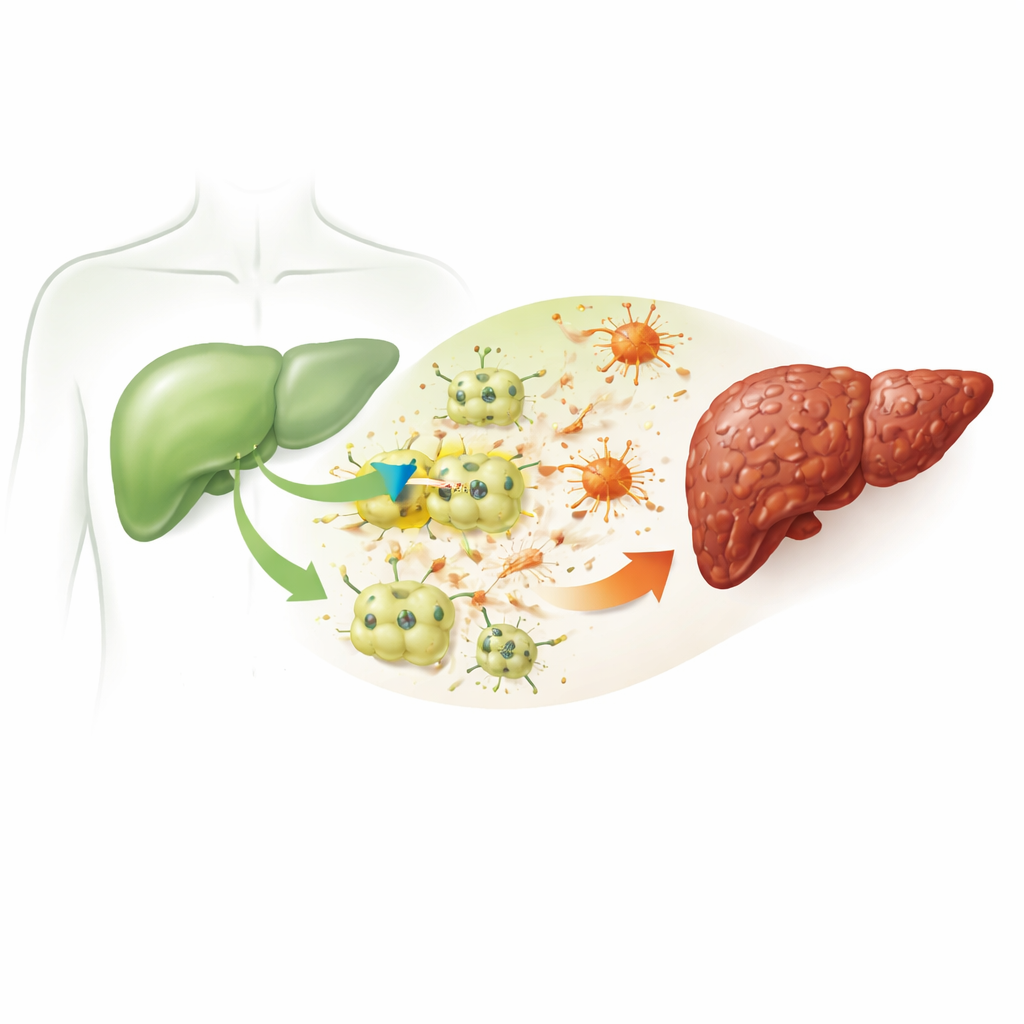
En dold kanal som framträder i sjuka leverceller
Teamet fokuserade på ett protein kallat ITPR3, en kanal som frigör kalcium från intracellulära lagrar. Friska hepatocyter tillverkar vanligen inte denna kanal alls. Men i både de skadade musleverna och de kemiskt stressade levercellerna odlade i labbet fann forskarna en markant ökning av ITPR3‑nivåer. Där ITPR3 dök upp var levercellerna betydligt mer benägna att genomgå programmerad celldöd, en kontrollerad form av självdestruktion. När forskarna använde ett genetiskt verktyg (siRNA) för att dämpa ITPR3 försvann den ökade intracellulära kalciumökningen och dödligheten bland cellerna sjönk kraftigt. Vätskan från dessa skadade hepatocyter kunde också omvandla närliggande stödjeceller, så kallade stellatceller, till ett aktivt, ärrproducerande tillstånd — en förändring som mildrades när ITPR3 undertrycktes.
Från kalciumsignal till inflammatorisk strömbrytare
Kalcium är inte bara ett strukturellt mineral; inne i celler fungerar korta kalciumpulser som signaler som slår på och av vägledningar. Författarna visade att överskott av kalcium som frigörs genom nyskapade ITPR3‑kanaler aktiverar en välkänd inflammatorisk regulator, NF‑κB. I skadade muslever och odlade hepatocyter förflyttade sig NF‑κB från cytoplasman till kärnan, där gener regleras — ett kännetecken för dess aktivering. Minskning av ITPR3‑nivåer förhindrade denna nukleära förflyttning, medan en kemisk NF‑κB‑hämmare minskade celldöd. Dessa experiment kopplar uppkomsten av ITPR3 till en kalciumvåg, aktivering av NF‑κB och i slutändan till förlust av hepatocyter, vilket banar väg för ärrbildning.
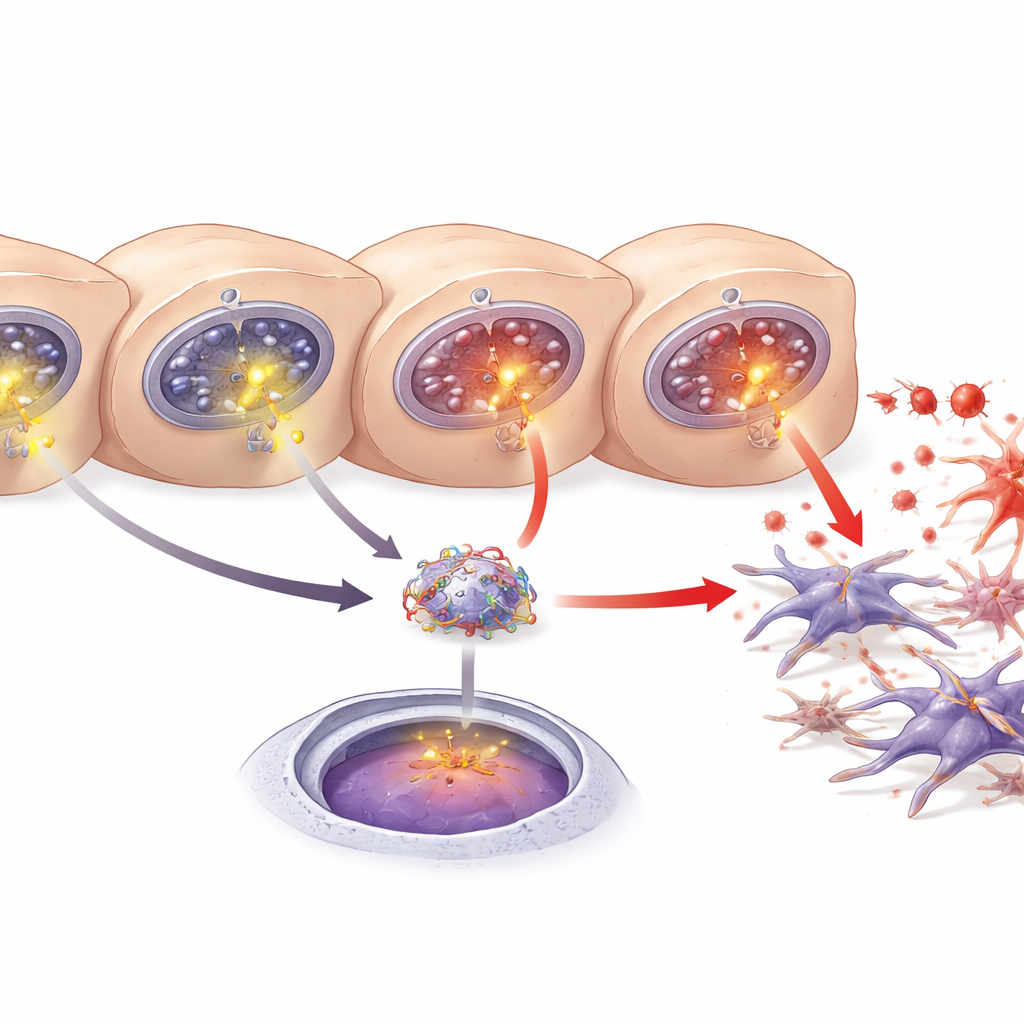
En leverbudbärare som driver ärrbildning
En annan nyckelspelare är ett leverderiverat protein kallat LECT2, tidigare implicerat i fettlever, fibros och levercancer. Forskarna fann ökad mängd LECT2 i blod, levervävnad och odlingsmedia när hepatocyter skadades. Genom databasprediktioner och genetiska rapportörtester visade de att NF‑κB kan binda till ett specifikt DNA‑avsnitt i LECT2‑genens reglerande område och öka dess aktivitet. Blockering av NF‑κB eller nedsättning av ITPR3 minskade båda LECT2‑produktion och utsöndring. Tillsammans beskriver resultaten en kedja: ITPR3 uppträder i stressade hepatocyter, utlöser extra kalciumfrisättning, aktiverar NF‑κB, driver LECT2‑produktion och främjar stellatcellaktivering och fibros.
Vad detta betyder för framtida behandlingar
Enkelt uttryckt identifierar studien en abnorm kalciumkanal, ITPR3, som en tidig ”på‑knapp” som omvandlar pågående leverskada till bestående ärrbildning. Genom att visa att ITPR3 leder till celldöd och fibros via en specifik kalcium–NF‑κB–LECT2‑väg framhäver arbetet flera potentiella läkemedelsmål: själva kanalen, den inflammatoriska strömbrytaren eller den nedströms leverbudbäraren. Även om mer forskning krävs hos människor, särskilt för att bekräfta säkerhet och verkliga nyttor, antyder resultaten att avstängning av ITPR3 skulle kunna hjälpa till att bevara leverceller, dämpa inflammation och sakta eller förhindra att kronisk leversjukdom utvecklas till cirros.
Citering: Zhao, X., Liu, X., Ni, M. et al. ITPR3 promotes liver fibrosis by damaging hepatocytes via the Ca2+/NF-B/LECT2 pathway. Sci Rep 16, 13376 (2026). https://doi.org/10.1038/s41598-026-43866-1
Nyckelord: leverfibros, hepatocytapoptos, calciumsignalering, NF-kappaB‑väg, LECT2