Clear Sky Science · ru
ITPR3 способствует фиброзу печени, повреждая гепатоциты через путь Ca2+/NF-κB/LECT2
Почему рубцевание печени важно
Заболевания печени растут во всем мире и часто развиваются бессимптомно в течение многих лет. Ключевым переломным моментом является фиброз печени — накопление рубцовой ткани, которое в конечном итоге может привести к циррозу и печеночной недостаточности. В этом исследовании задают важный вопрос: что именно вызывает ранние повреждения клеток печени, запускающие процесс рубцевания, и может ли блокирование одного молекулярного «переключателя» помочь защитить печень от долгосрочного вреда?
Взгляд в механизм повреждения печени
Фиброз начинается, когда основные функциональные клетки печени — гепатоциты — подвергаются повторным повреждениям. В исследовании ученые использовали хорошо зарекомендовавшее себя химическое вещество тетрахлорид углерода, чтобы смоделировать хроническое повреждение печени у мышей и в культурах мышиных печеночных клеток. Леченые мыши демонстрировали признаки болезни печени, сходные с человеческими: повышенные кровяные маркеры повреждения печени, нарушения жирового и холестеринового обмена, воспаление и обильные отложения рубцоподобного материала, искажающие нормальную архитектуру печени. Эти изменения подтверждают, что модель достоверно воспроизводит цепочку событий, превращающую простое повреждение в стойкое рубцевание.
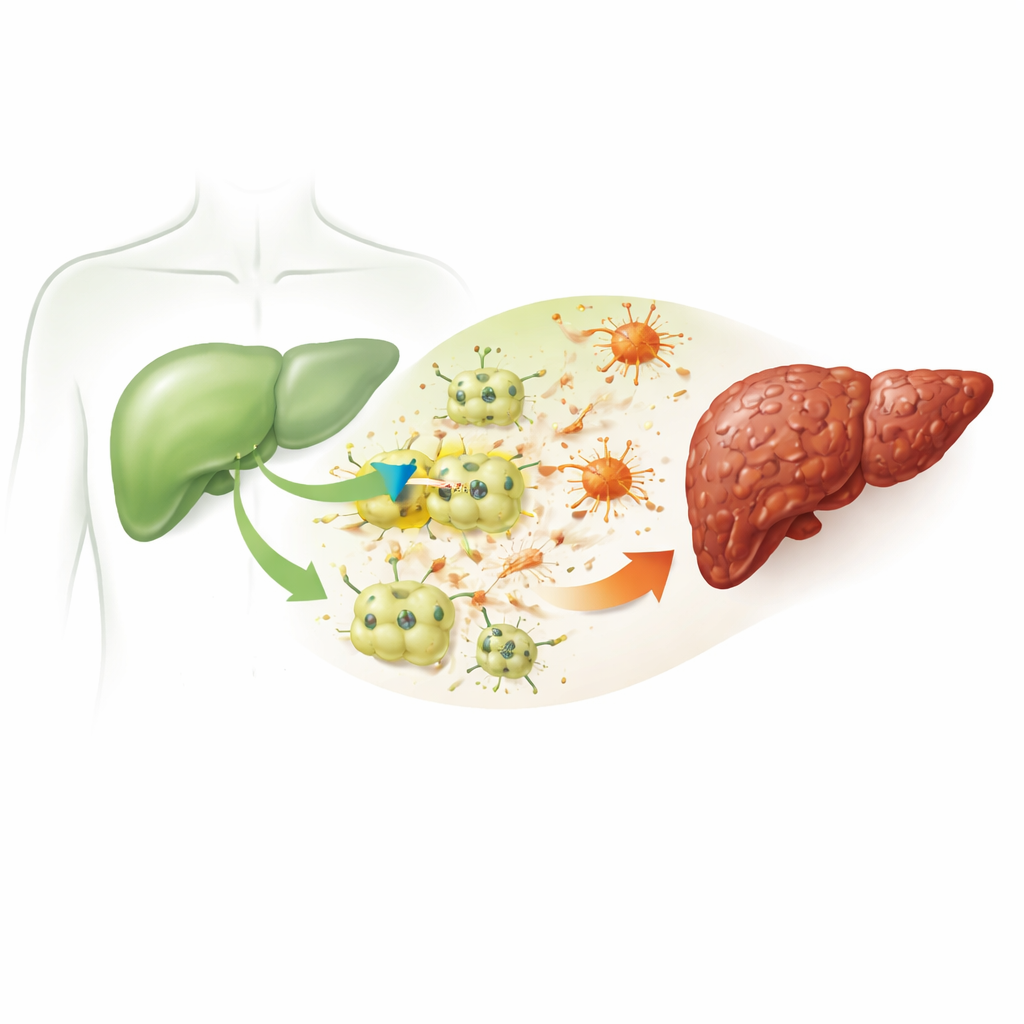
Скрытый канал, появляющийся в больных гепатоцитах
Команда сосредоточилась на белке ITPR3 — канале, который высвобождает кальций из внутриклеточных депо. В здоровых гепатоцитах этот канал обычно не экспрессируется вовсе. Однако и в поврежденных печенях мышей, и в химически стрессированных печеночных клетках in vitro исследователи обнаружили заметное повышение уровня ITPR3. Там, где появлялся ITPR3, гепатоциты значительно чаще проходили программируемую гибель, контролируемую форму самоуничтожения. Когда ученые с помощью генетического инструмента (siRNA) подавляли ITPR3, всплеск внутриклеточного кальция исчезал, и частота гибели клеток резко снижалась. Среда от этих поврежденных гепатоцитов также могла переводить соседние поддерживающие клетки — звездчатые клетки печени — в активное состояние с секрецией рубцеобразующих компонентов; это изменение было ослаблено при подавлении ITPR3.
От кальциевого сигнала к воспалительному переключателю
Кальций — это не только структурный минерал: внутри клеток кратковременные всплески кальция служат сигналами, включающими и выключающими пути. Авторы показали, что избыток кальция, высвобожденный через вновь возникающие каналы ITPR3, активирует хорошо известный регулятор воспаления NF-κB. В поврежденных печенях мышей и в культивируемых гепатоцитах NF-κB перемещался из цитоплазмы в ядро — признак его активации. Снижение уровней ITPR3 предотвращало это ядерное перемещение, тогда как химический блокатор NF-κB уменьшал гибель клеток. Эти эксперименты связывают появление ITPR3 с всплеском кальция, активацией NF-κB и в конечном счете с потерей гепатоцитов, создавая основу для формирования рубцов.
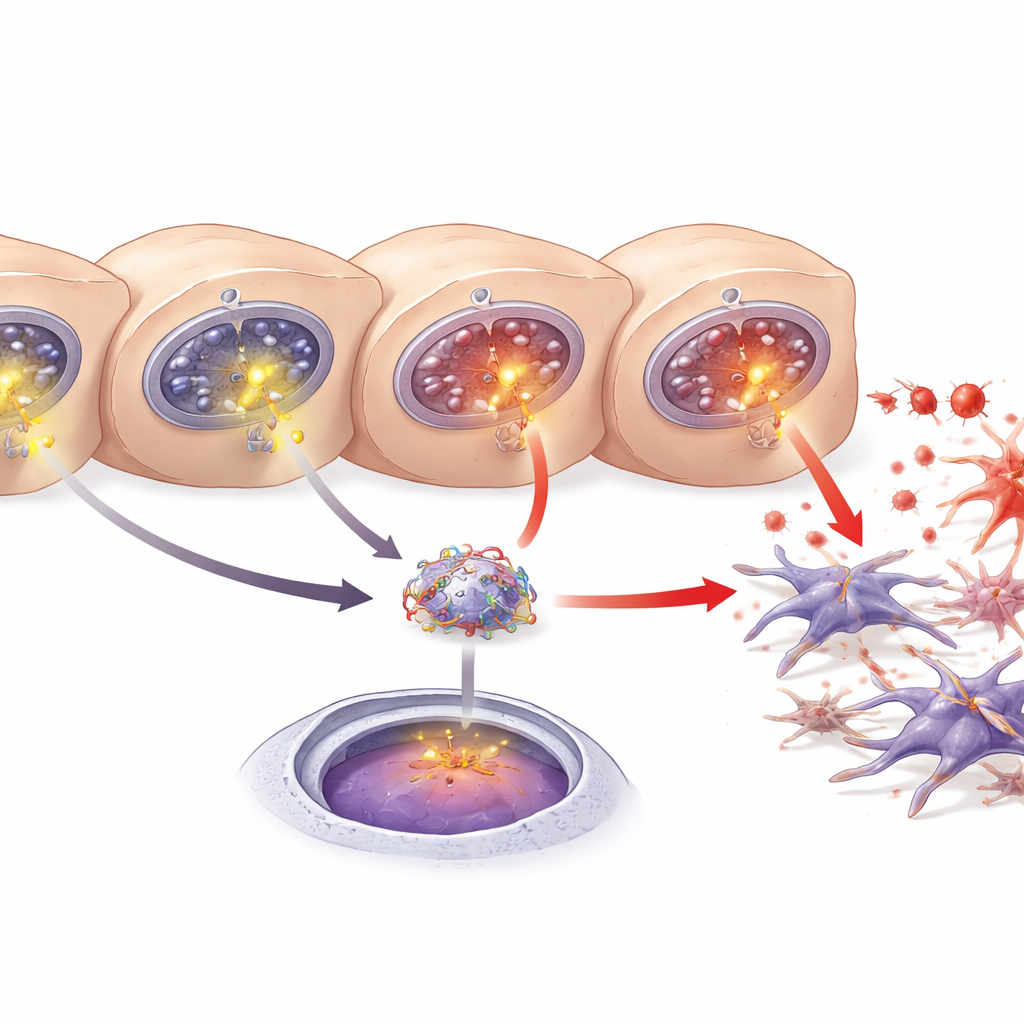
Печеночный мессенджер, подпитывающий рубцевание
Еще один ключевой участник — белок, происходящий из печени, LECT2, ранее связанный с жировой болезнью печени, фиброзом и раком печени. Исследователи обнаружили больше LECT2 в крови, печеночной ткани и в среде культивирования при повреждении гепатоцитов. Используя базы данных предсказаний и генетические репортерные тесты, они показали, что NF-κB может присоединяться к определенному фрагменту ДНК в регуляторной области гена LECT2 и усиливать его активность. Блокирование NF-κB или понижение ITPR3 снижало продукцию и выделение LECT2. В совокупности результаты описывают цепочку: ITPR3 появляется в стрессированных гепатоцитах, вызывает дополнительное высвобождение кальция, активирует NF-κB, стимулирует синтез LECT2 и способствует активации звездчатых клеток и фиброзу.
Что это значит для будущих терапий
Проще говоря, исследование выявляет аномальный кальциевый канал ITPR3 как верхний «включатель», который превращает продолжающееся повреждение печени в стойкое рубцевание. Показав, что ITPR3 приводит к гибели клеток и фиброзу через конкретный путь кальций–NF-κB–LECT2, работа выделяет несколько потенциальных мишеней для лекарств: сам канал, воспалительный переключатель или его нисходящий печеночный мессенджер. Хотя для подтверждения безопасности и эффективности у людей потребуется дополнительная работа, результаты говорят о том, что отключение ITPR3 может помочь сохранить гепатоциты, уменьшить воспаление и замедлить или предотвратить прогрессирование хронического заболевания печени к циррозу.
Цитирование: Zhao, X., Liu, X., Ni, M. et al. ITPR3 promotes liver fibrosis by damaging hepatocytes via the Ca2+/NF-B/LECT2 pathway. Sci Rep 16, 13376 (2026). https://doi.org/10.1038/s41598-026-43866-1
Ключевые слова: фиброз печени, апоптоз гепатоцитов, кальциевые сигналы, путь NF-kappaB, LECT2