Clear Sky Science · he
ITPR3 מקדם פיברוזיס בכבד על‑ידי פגיעה בהפטוציטים דרך מסלול Ca2+/NF‑κB/LECT2
למה הצלקת בכבד חשובה
מחלות כבד נמצאות בעלייה ברחבי העולם ולעתים קרובות מתקדמות באופן שקט במשך שנים לפני שהסימפטומים מופיעים. נקודת מפנה מרכזית היא הפיברוזיס של הכבד, הצטברות רקמת צלקת שיכולה בסופו של דבר להוביל לצירוזיס ולכשל כבד. מחקר זה שואל שאלה קריטית: מה בדיוק מובל לנזק המוקדם לתאי הכבד שמפעיל את תהליך ההצטלקות הזה, והאם חסימה של "מתג" מולקולרי יחיד יכולה להגן על הכבד מפגיעה לטווח ארוך?
מבט מקרוב על האופן שבו הכבד ניזוק
הפיברוזיס מתחיל כאשר תאי הכבד העיקריים, המכונים הפטוציטים, נפגעים שוב ושוב. במחקר זה השתמשו החוקרים בכימיקל ידוע היטב, פחמן‑טטרהכלוריד, כדי לחקות נזק כרוני לכבד בעכברים ובתאים כבדיים של עכבר בתרבית. בעכברים המטופלים הופיעו סימני היכר של מחלת כבד הנצפים בבני אדם: עלייה בסמנים בדם המעידים על פגיעה בכבד, הפרעות שומניות וכולסטרוליות, דלקת והצטברויות כבידות של חומר דמוי צלקת שמעוותות את הארכיטקטורה הנורמלית של הכבד. שינויים אלה מאשרים שהמודל משכפל בנאמנות את שרשרת האירועים שממירה פגיעה פשוטה לצלקת מתמשכת.
ערוץ מוסתר שמופיע בתאי כבד חולים
הצוות התרכז בחלבון בשם ITPR3, תעלה שמשחררת סידן ממאגרי פנימיים בתוך התאים. בהפטוציטים בריאים התעלה הזו בדרך כלל אינה מיוצרת כלל. אולם גם בכבדות העכבר הפגועות וגם בתאים הכבדיים המצופים בכימיקל במעבדה מצאו החוקרים עלייה בולטת ברמות ITPR3. במקום שבו הופיעה ITPR3, תאי הכבד היו בסבירות גבוהה יותר לעבור מוות תאי מתוכנן (אפטוזיס), צורת השמדה עצמית מבוקרת. כאשר המדענים השתמשו בכלי גנטי (siRNA) כדי לדכא את ITPR3, גל הסידן הפנימי נעלם ושיעור המוות התאי ירד באופן חד. גם הנוזל מהפטוציטים הפגועים הללו יכול היה להפוך תאים תומכים סמוכים, הנקראים תאי סטלת הכבד (hepatic stellate cells), למצב פעיל המייצר צלקת — שינוי שהצטמצם כאשר ITPR3 הושתקה.
אות הסידן למתג דלקתי
סידן אינו רק מינרל מבני; בתוך התאים, פולסים קצרים של סידן משמשים כאותות שמשתקים או מדליקים מסלולים. המחברים הראו שסידן עודף שמשתחרר דרך תעלות ITPR3 שנוצרו מפעיל רגולטור דלקתי ידוע, NF‑κB. בכבדות העכבר הפגועות ובהפטוציטים בתרבית, NF‑κB זז מתוך הציטופלזמה אל הגרעין, שם מבוקרים גנים — סימן אופייני להפעלתו. הקטנת רמות ITPR3 מנעה את ההזזה הזאת לגרעין, בעוד שחוסם כימי של NF‑κB צימצם את המוות התאי. ניסויים אלה מקשרים את הופעת ITPR3 לגל סידן, להפעלת NF‑κB ולבסוף לאובדן הפטוציטים, וכך מכינים את הבסיס להיווצרות צלקת.
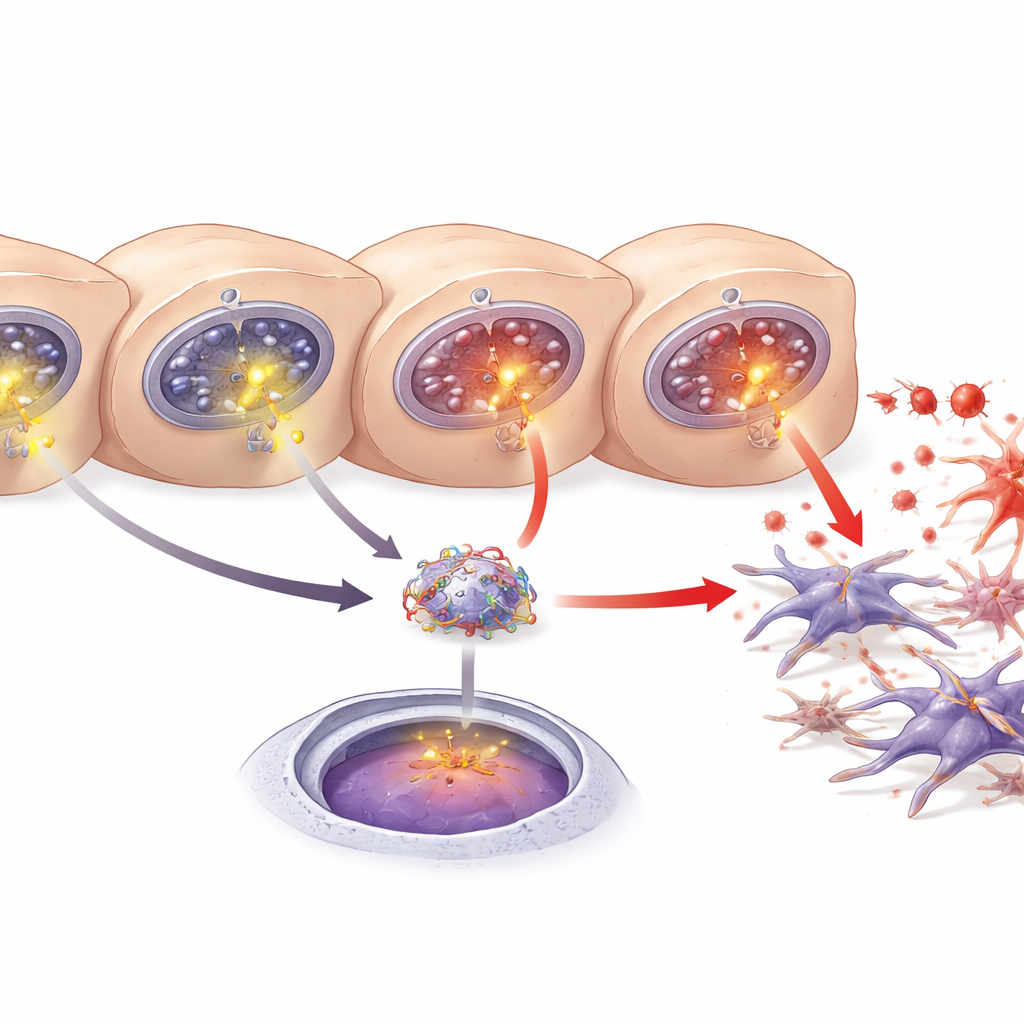
שליח כבד שמזין את ההצטלקות
שחקן מרכזי נוסף הוא חלבון שמקורו בכבד בשם LECT2, שהיה מעורב בעבר בכבד שומני, פיברוזיס וסרטן הכבד. החוקרים מצאו יותר LECT2 בדם, ברקמת הכבד ובמדיות התרבית כאשר הפטוציטים ניזוקו. בעזרת תחזיות ממסדי נתונים ובדיקות מדד גנטיות הם הראו ש‑NF‑κB יכול להיקשר למקטע DNA ספציפי באזור הבקרה של גן LECT2 ולהגביר את פעילותו. חסימת NF‑κB או השתקת ITPR3 שניהם הפחיתו את ייצור ושחרור ה‑LECT2. יחד, הממצאים מתארים שרשרת: ITPR3 מופיעה בהפטוציטים הלחוצים, גורמת לשחרור סידן נוסף, מפעילה את NF‑κB, מגרה ייצור LECT2 ומקדמת את הפעלת תאי הסטלת ואת הפיברוזיס.
מה משמעות הדבר לטיפולים עתידיים
במילים פשוטות, המחקר מזהה תעלת סידן חריגה, ITPR3, כ"מתג" על‑זרימה שממירה פגיעה ממושכת בכבד לצלקת מתמשכת. על‑ידי הוכחה ש‑ITPR3 מובילה למוות תאי ולפיברוזיס דרך מסלול ספציפי של סידן–NF‑κB–LECT2, העבודה מדגישה מספר מטרות תרופתיות פוטנציאליות: התעלה עצמה, המתג הדלקתי או השליח הכבד ההורד. למרות שיש צורך במחקר נוסף בבני אדם, ובמיוחד לאמת בטיחות ותועלת במציאות הקלינית, התוצאות מרמזות שכיבוי ITPR3 עשוי לסייע בשימור תאי הכבד, בהרגעת דלקת ובהאטה או מניעה של התקדמות מחלת כבד כרונית לכיוון צירוזיס.
ציטוט: Zhao, X., Liu, X., Ni, M. et al. ITPR3 promotes liver fibrosis by damaging hepatocytes via the Ca2+/NF-B/LECT2 pathway. Sci Rep 16, 13376 (2026). https://doi.org/10.1038/s41598-026-43866-1
מילות מפתח: פיברוזיס של הכבד, אפטוזיס של הפטוציטים, אותות סידן, מסלול NF‑kappaB, LECT2