Clear Sky Science · fr
ITPR3 favorise la fibrose hépatique en endommageant les hépatocytes via la voie Ca2+/NF-κB/LECT2
Pourquoi la cicatrisation du foie importe
Les maladies du foie augmentent dans le monde et évoluent souvent de façon silencieuse pendant des années avant l’apparition de symptômes. Un tournant clé est la fibrose hépatique, l’accumulation de tissu cicatriciel qui peut finalement conduire à la cirrhose et à l’insuffisance hépatique. Cette étude pose une question cruciale : qu’est‑ce qui provoque exactement les premiers dommages aux cellules hépatiques qui déclenchent ce processus de cicatrisation, et l’inhibition d’un seul « interrupteur » moléculaire pourrait‑elle protéger le foie contre des dégâts à long terme ?
Un examen approfondi des mécanismes de dommage du foie
La fibrose débute lorsque les principales cellules fonctionnelles du foie, les hépatocytes, sont blessées de manière répétée. Dans cette étude, les chercheurs ont utilisé un produit chimique bien établi, le tétrachlorure de carbone, pour reproduire un dommage hépatique chronique chez la souris et dans des cultures de cellules hépatiques murines. Les souris traitées ont développé des signes caractéristiques de maladie hépatique observés chez l’humain : des marqueurs sanguins d’atteinte hépatique élevés, des perturbations du métabolisme des lipides et du cholestérol, une inflammation et d’importants dépôts de matière ressemblant à du tissu cicatriciel qui déforment l’architecture normale du foie. Ces changements confirment que le modèle reproduit fidèlement la chaîne d’événements qui transforme une lésion simple en cicatrisation durable.
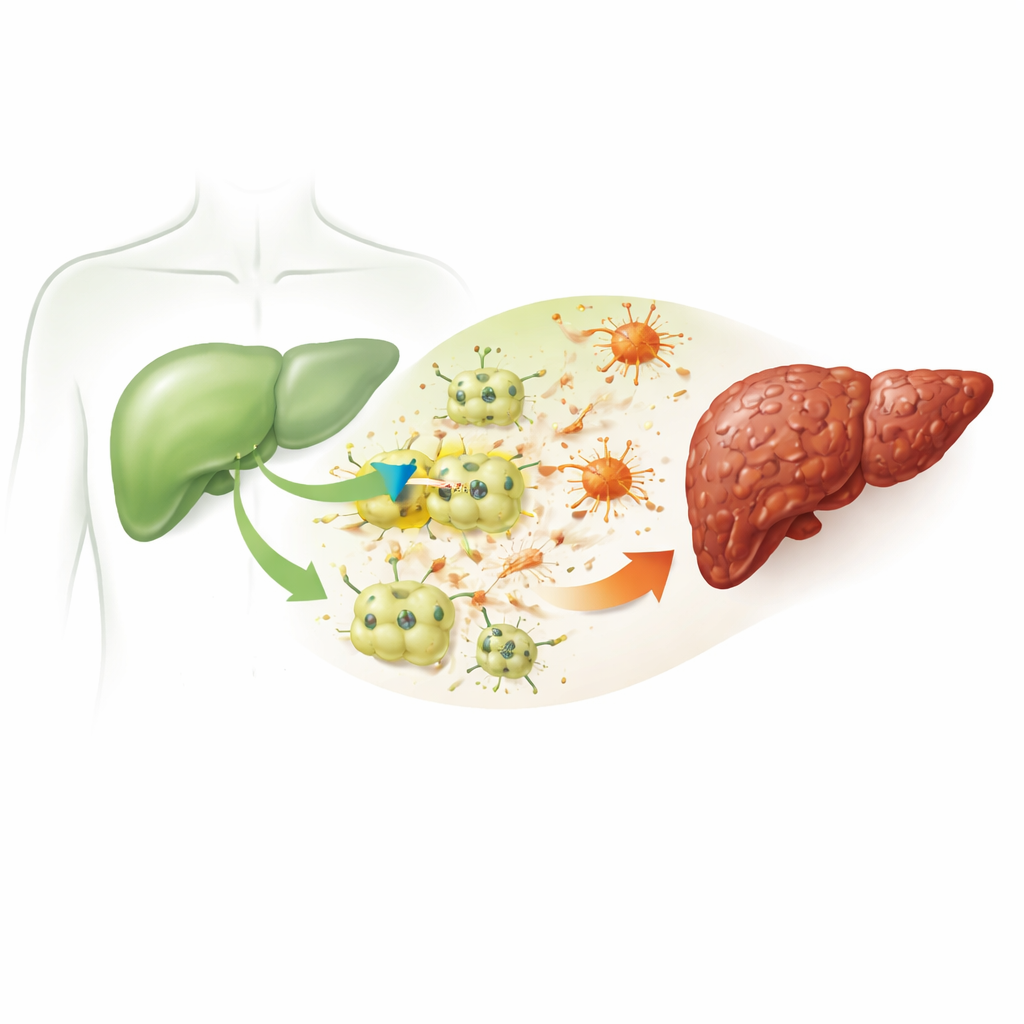
Un canal caché qui apparaît dans les hépatocytes malades
L’équipe s’est concentrée sur une protéine nommée ITPR3, un canal qui libère du calcium depuis les réserves internes des cellules. Les hépatocytes sains ne produisent normalement pas ce canal. Cependant, dans les foies de souris endommagés et dans les cellules hépatiques soumises au stress chimique en culture, les chercheurs ont observé une augmentation marquée des niveaux d’ITPR3. Là où l’ITPR3 apparaissait, les cellules hépatiques avaient beaucoup plus de chances de subir une mort cellulaire programmée, une forme contrôlée d’autodestruction. Lorsque les scientifiques ont utilisé un outil génétique (siRNA) pour réduire l’expression d’ITPR3, la hausse du calcium intracytoplasmique a disparu et le taux de mort cellulaire a fortement diminué. Le liquide provenant de ces hépatocytes endommagés pouvait aussi transformer des cellules de soutien voisines, appelées cellules étoilées hépatiques, en un état actif producteur de cicatrices — un changement atténué lorsque l’ITPR3 était supprimée.
Du signal calcique à l’interrupteur inflammatoire
Le calcium n’est pas qu’un minéral structurel ; à l’intérieur des cellules, de brefs pics calciques servent de signaux qui activent ou désactivent des voies. Les auteurs ont montré que le calcium en excès libéré via les canaux ITPR3 nouvellement exprimés active un régulateur inflammatoire bien connu, NF‑κB. Dans les foies de souris endommagés et dans les hépatocytes en culture, NF‑κB migrait du cytosol vers le noyau, où sont contrôlés les gènes, signe de son activation. La réduction des niveaux d’ITPR3 empêchait cette translocation nucléaire, tandis qu’un inhibiteur chimique de NF‑κB diminuait la mort cellulaire. Ces expériences relient l’apparition d’ITPR3 à une poussée calcique, à l’activation de NF‑κB et, en fin de compte, à la perte d’hépatocytes, préparant le terrain pour la formation de cicatrices.
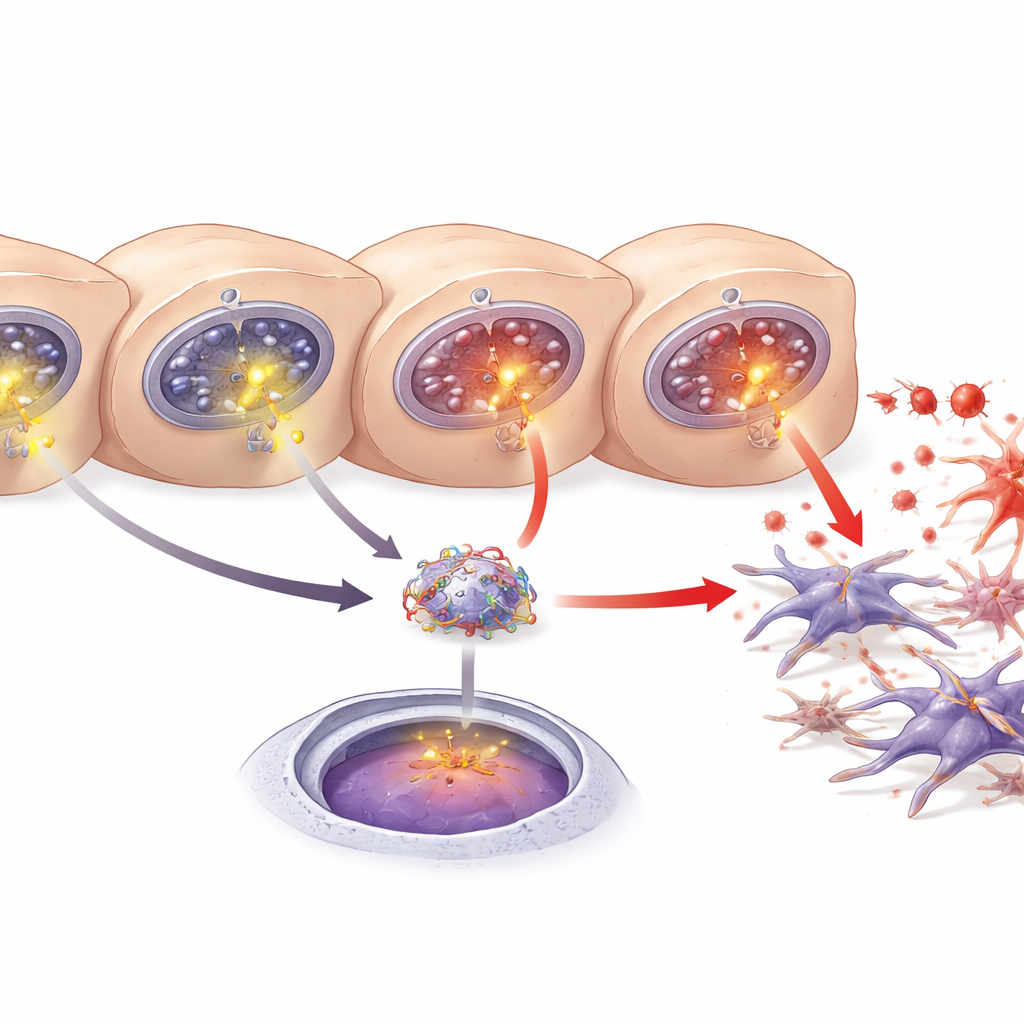
Un messager hépatique qui alimente la fibrose
Un autre acteur clé est une protéine d’origine hépatique appelée LECT2, déjà impliquée dans la stéatose hépatique, la fibrose et le cancer du foie. Les chercheurs ont trouvé davantage de LECT2 dans le sang, le tissu hépatique et le milieu de culture lorsque les hépatocytes étaient endommagés. À partir de prédictions de bases de données et de tests de gènes rapporteurs, ils ont montré que NF‑κB peut se lier à une séquence spécifique d’ADN dans la région régulatrice du gène LECT2, augmentant ainsi son activité. Le blocage de NF‑κB ou l’abaissement d’ITPR3 réduisaient tous deux la production et la libération de LECT2. Ensemble, ces résultats décrivent une chaîne d’événements : ITPR3 apparaît dans les hépatocytes stressés, déclenche une libération de calcium supplémentaire, active NF‑κB, stimule la production de LECT2 et favorise l’activation des cellules étoilées et la fibrose.
Ce que cela signifie pour les traitements futurs
En termes simples, l’étude identifie un canal calcique anormal, ITPR3, comme un « interrupteur » en amont qui transforme une lésion hépatique continue en cicatrisation durable. En montrant qu’ITPR3 conduit à la mort cellulaire et à la fibrose via une voie spécifique calcium–NF‑κB–LECT2, le travail met en évidence plusieurs cibles médicamenteuses potentielles : le canal lui‑même, l’interrupteur inflammatoire ou le messager hépatique en aval. Si des recherches supplémentaires sont nécessaires chez l’humain, notamment pour confirmer la sécurité et l’efficacité en conditions réelles, les résultats suggèrent que l’inhibition d’ITPR3 pourrait aider à préserver les hépatocytes, à calmer l’inflammation et à ralentir ou prévenir la progression des maladies hépatiques chroniques vers la cirrhose.
Citation: Zhao, X., Liu, X., Ni, M. et al. ITPR3 promotes liver fibrosis by damaging hepatocytes via the Ca2+/NF-B/LECT2 pathway. Sci Rep 16, 13376 (2026). https://doi.org/10.1038/s41598-026-43866-1
Mots-clés: fibrose hépatique, apoptose des hépatocytes, signalisation calcique, voie NF-kappaB, LECT2