Clear Sky Science · nl
ITPR3 bevordert leverfibrose door hepatocyten te beschadigen via de Ca2+/NF-κB/LECT2-route
Waarom littekens in de lever ertoe doen
Leveraandoeningen nemen wereldwijd toe en verlopen vaak jarenlang sluipend zonder symptomen. Een cruciaal kantelpunt is leverfibrose, de ophoping van littekenweefsel die uiteindelijk kan leiden tot cirrose en leverfalen. Deze studie stelt een belangrijke vraag: wat veroorzaakt precies de vroegste beschadiging van levercellen die dit littekenproces in gang zet, en zou het blokkeren van één moleculaire "schakelaar" de lever tegen langdurige schade kunnen beschermen?
Een nadere blik op hoe de lever beschadigt
Fibrose begint wanneer de belangrijkste werkcellen van de lever, hepatocyten genoemd, herhaaldelijk worden beschadigd. In deze studie gebruikten de onderzoekers een goed bekend chemisch middel, tetrachloorkoolstof, om chronische leverschade na te bootsen bij muizen en in gekweekte muizenlevercellen. De behandelde muizen ontwikkelden kenmerkende tekenen van leverziekte die ook bij mensen voorkomen: verhoogde bloedwaarden van leverbeschadiging, verstoring van vet- en cholesterolhuishouding, ontsteking en zware afzettingen van littekenachtig materiaal die de normale leverarchitectuur vervormen. Deze veranderingen bevestigen dat het model de keten van gebeurtenissen die eenvoudige beschadiging in blijvend littekenweefsel omzet, getrouw nabootst.
Een verborgen kanaal dat verschijnt in zieke levercellen
Het team richtte zich op een eiwit genaamd ITPR3, een kanaal dat calcium uit interne opslagplaatsen in de cel vrijgeeft. Gezonde hepatocyten produceren dit kanaal normaal gesproken niet. In zowel de beschadigde muizenlevers als de chemisch gestreste levercellen in het laboratorium vonden de onderzoekers echter een opvallende toename van ITPR3-niveaus. Waar ITPR3 opdook, liepen levercellen veel eerder het risico geprogrammeerde celdood te ondergaan, een gecontroleerde vorm van zelfdestructie. Toen de wetenschappers een genetisch middel (siRNA) gebruikten om ITPR3 te verminderen, verdween de piek in intern calcium en daalde het celdoodpercentage scherp. Vloeistof uit deze beschadigde hepatocyten kon ook nabijgelegen steuncellen, zogeheten stellate-cellen, omzetten in een actieve, littekenproducerende staat — een verandering die werd afgezwakt wanneer ITPR3 werd onderdrukt.
Van calciumsignaal naar ontstekingsschakelaar
Calcium is niet alleen een structureel mineraal; binnen cellen fungeren korte calciumpulses als signalen die routes aan- en uitzetten. De auteurs lieten zien dat overtollig calcium dat via nieuw gevormde ITPR3-kanalen vrijkomt, een bekende ontstekingsregelaar, NF-κB, activeert. In beschadigde muizenlevers en gekweekte hepatocyten verschoof NF-κB van het celvocht naar de kern, waar genen worden gereguleerd — een kenmerk van activering. Het verlagen van ITPR3-niveaus verhinderde deze verschuiving naar de kern, terwijl een chemische NF-κB-remmer celdood verminderde. Deze experimenten koppelen het verschijnen van ITPR3 aan een calciumpiek, activatie van NF-κB en uiteindelijk verlies van hepatocyten, waarmee het toneel wordt gezet voor littekenvorming.
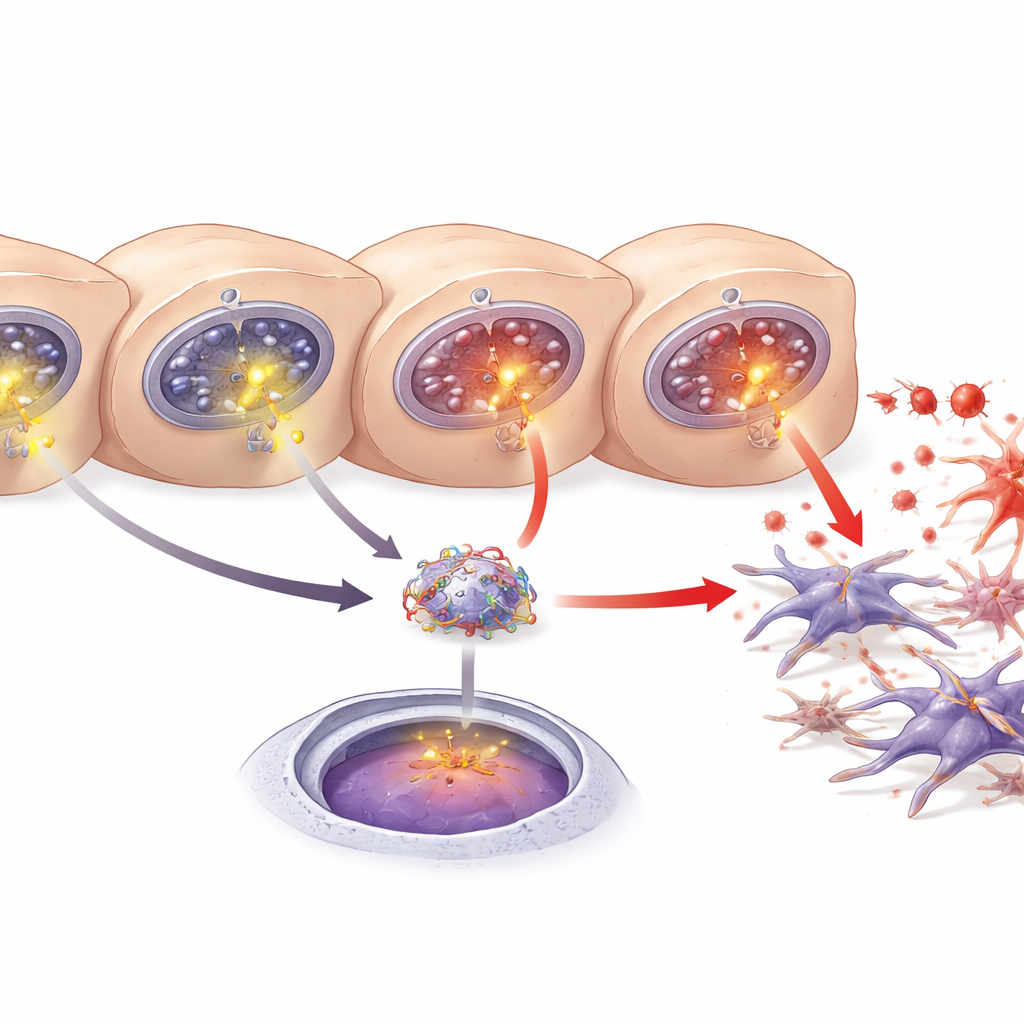
Een leverboodschapper die littekenvorming aanjaagt
Een andere belangrijke speler is een leverafgeleid eiwit genaamd LECT2, eerder in verband gebracht met leververvetting, fibrose en leverkanker. De onderzoekers vonden meer LECT2 in het bloed, leverweefsel en kweekmedium wanneer hepatocyten beschadigd waren. Met behulp van databankvoorspellingen en genetische reporter-testen toonden ze aan dat NF-κB zich kan binden aan een specifieke DNA-sequentie in het regulerende gebied van het LECT2-gen en zo de activiteit ervan verhoogt. Het blokkeren van NF-κB of het naar beneden brengen van ITPR3 verminderde zowel de productie als de afgifte van LECT2. Gezamenlijk schetsen de bevindingen een keten: ITPR3 verschijnt in gestreste hepatocyten, veroorzaakt extra calciumvrijgave, activeert NF-κB, stimuleert LECT2-productie en bevordert activatie van stellate-cellen en fibrose.
Wat dit betekent voor toekomstige behandelingen
Concreet identificeert de studie een abnormaal calciumkanaal, ITPR3, als een upstream "aan-schakelaar" die aanhoudende leverschade omzet in blijvend littekenweefsel. Door aan te tonen dat ITPR3 via een specifieke calcium–NF-κB–LECT2-route leidt tot celdood en fibrose, benadrukt het werk meerdere potentiële medicinale aanvalsdoelen: het kanaal zelf, de ontstekingsschakelaar of de downstream leverboodschapper. Hoewel meer onderzoek bij mensen nodig is, vooral om veiligheid en echte klinische voordelen te bevestigen, suggereren de resultaten dat het uitschakelen van ITPR3 kan helpen hepatocyten te bewaren, ontsteking te verminderen en het verloop van chronische leverziekte naar cirrose te vertragen of voorkomen.
Bronvermelding: Zhao, X., Liu, X., Ni, M. et al. ITPR3 promotes liver fibrosis by damaging hepatocytes via the Ca2+/NF-B/LECT2 pathway. Sci Rep 16, 13376 (2026). https://doi.org/10.1038/s41598-026-43866-1
Trefwoorden: leverfibrose, apoptose van hepatocyten, calciumsignaal, NF-kappaB-route, LECT2