Clear Sky Science · pt
ITPR3 promove fibrose hepática ao danificar hepatócitos via a via Ca2+/NF-κB/LECT2
Por que a cicatrização do fígado é importante
Doenças hepáticas estão aumentando no mundo todo e frequentemente progridem de forma silenciosa por anos antes que surjam sintomas. Um ponto de virada crucial é a fibrose hepática, o acúmulo de tecido cicatricial que pode eventualmente levar à cirrose e à falência do fígado. Este estudo faz uma pergunta central: o que exatamente provoca os primeiros danos às células do fígado que desencadeiam esse processo de cicatrização, e seria possível proteger o fígado do dano a longo prazo bloqueando um único “interruptor” molecular?
Um olhar mais atento sobre como o fígado é lesionado
A fibrose começa quando as principais células funcionais do fígado, chamadas hepatócitos, são repetidamente lesionadas. Neste estudo, os pesquisadores usaram um composto bem estabelecido, o tetracloreto de carbono, para mimetizar dano hepático crônico em camundongos e em células hepáticas de camundongo cultivadas. Os animais tratados desenvolveram sinais característicos de doença hepática observados em humanos: elevação de marcadores sanguíneos de lesão hepática, alterações no metabolismo de gorduras e colesterol, inflamação e depósitos intensos de material semelhante a cicatriz que distorcem a arquitetura normal do fígado. Essas alterações confirmam que o modelo reproduz fielmente a cadeia de eventos que transforma uma lesão simples em uma cicatrização duradoura.
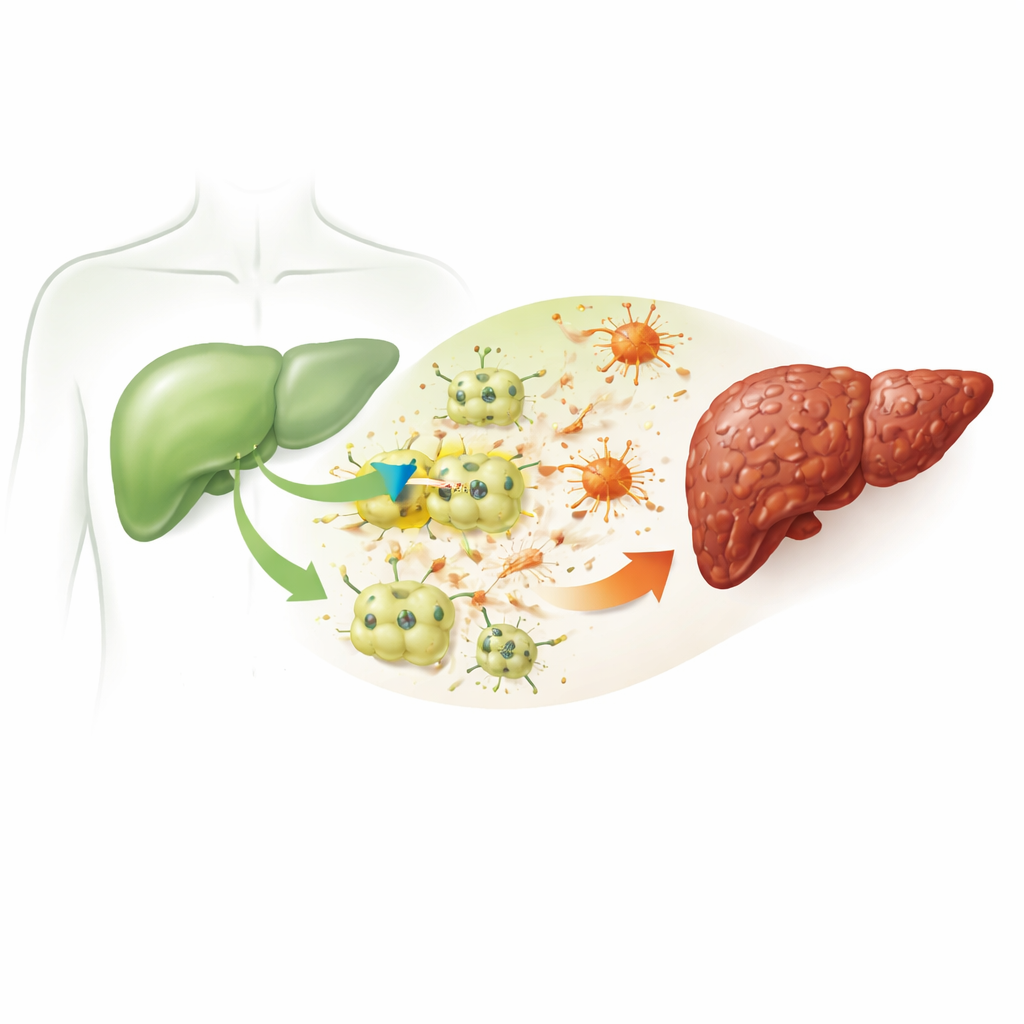
Um canal oculto que aparece em hepatócitos doentes
A equipe concentrou‑se em uma proteína chamada ITPR3, um canal que libera cálcio de reservatórios internos dentro das células. Hepatócitos saudáveis normalmente não produzem esse canal. Contudo, tanto nos fígados de camundongos lesionados quanto nas células hepáticas quimicamente estressadas cultivadas em laboratório, os pesquisadores observaram um aumento marcante nos níveis de ITPR3. Onde o ITPR3 apareceu, as células hepáticas tinham muito mais probabilidade de estar em processo de morte programada, uma forma controlada de autodestruição. Quando os cientistas usaram uma ferramenta genética (siRNA) para reduzir o ITPR3, o pico de cálcio intracelular desapareceu e a taxa de morte celular caiu acentuadamente. O fluido proveniente desses hepatócitos danificados também podia ativar células de suporte próximas, chamadas células estreladas hepáticas, levando‑as a um estado ativo produtor de cicatriz — mudança que foi atenuada quando o ITPR3 foi suprimido.
Do sinal de cálcio ao interruptor inflamatório
O cálcio não é apenas um mineral estrutural; dentro das células, pulsos breves de cálcio funcionam como sinais que ligam e desligam vias. Os autores mostraram que o excesso de cálcio liberado por canais ITPR3 recém‑formados ativa um regulador inflamatório bem conhecido, o NF‑κB. Em fígados de camundongos lesionados e em hepatócitos cultivados, o NF‑κB deslocou‑se do citoplasma para o núcleo, onde os genes são controlados — um marco de sua ativação. Reduzir os níveis de ITPR3 impediu esse movimento nuclear, enquanto um bloqueador químico do NF‑κB reduziu a morte celular. Esses experimentos conectam o aparecimento do ITPR3 a um surto de cálcio, ativação do NF‑κB e, em última instância, à perda de hepatócitos, preparando o terreno para a formação de cicatriz.
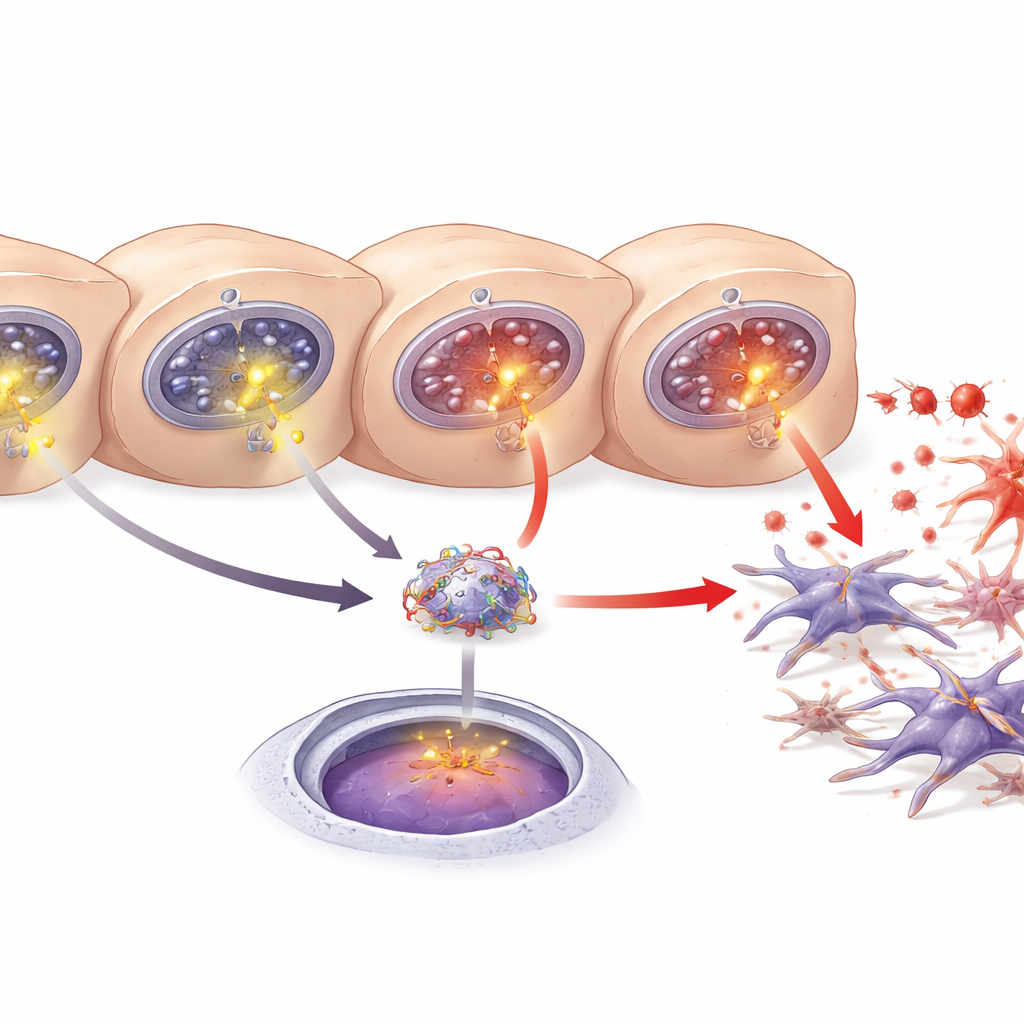
Um mensageiro hepático que alimenta a cicatrização
Outro ator-chave é uma proteína derivada do fígado chamada LECT2, previamente implicada em doença hepática gordurosa, fibrose e câncer de fígado. Os pesquisadores encontraram mais LECT2 no sangue, no tecido hepático e no meio de cultura quando os hepatócitos estavam lesionados. Usando previsões de bancos de dados e testes com repórteres genéticos, mostraram que o NF‑κB pode se ligar a um trecho específico de DNA na região reguladora do gene LECT2, aumentando sua atividade. Bloquear o NF‑κB ou reduzir o ITPR3 diminuiu tanto a produção quanto a liberação de LECT2. Em conjunto, os achados delineiam uma sequência: ITPR3 aparece em hepatócitos estressados, desencadeia liberação extra de cálcio, ativa o NF‑κB, impulsiona a produção de LECT2 e promove a ativação de células estreladas e a fibrose.
O que isso significa para tratamentos futuros
Em termos simples, o estudo identifica um canal de cálcio anômalo, o ITPR3, como um “interruptor” a montante que converte lesão hepática contínua em cicatrização duradoura. Ao mostrar que o ITPR3 leva à morte celular e à fibrose por meio de uma rota específica cálcio–NF‑κB–LECT2, o trabalho destaca vários alvos farmacológicos potenciais: o próprio canal, o interruptor inflamatório ou o mensageiro hepático a jusante. Embora sejam necessárias mais pesquisas em humanos, especialmente para confirmar segurança e benefícios na prática clínica, os resultados sugerem que desligar o ITPR3 poderia ajudar a preservar hepatócitos, reduzir a inflamação e desacelerar ou prevenir a progressão da doença hepática crônica para cirrose.
Citação: Zhao, X., Liu, X., Ni, M. et al. ITPR3 promotes liver fibrosis by damaging hepatocytes via the Ca2+/NF-B/LECT2 pathway. Sci Rep 16, 13376 (2026). https://doi.org/10.1038/s41598-026-43866-1
Palavras-chave: fibrose hepática, apoptose de hepatócitos, sinalização do cálcio, via NF-kappaB, LECT2