Clear Sky Science · pl
ITPR3 promuje włóknienie wątroby, uszkadzając hepatocyty przez szlak Ca2+/NF-κB/LECT2
Dlaczego bliznowacenie wątroby ma znaczenie
Choroby wątroby rosną na całym świecie i często rozwijają się cicho przez lata, zanim pojawią się objawy. Kluczowym momentem jest włóknienie wątroby, czyli odkładanie się tkanki bliznowatej, które ostatecznie może prowadzić do marskości i niewydolności wątroby. W tym badaniu postawiono ważne pytanie: co dokładnie powoduje najwcześniejsze uszkodzenie komórek wątroby, które inicjuje ten proces bliznowacenia, i czy zablokowanie jednego molekularnego „wyłącznika” mogłoby chronić wątrobę przed długotrwałą szkodą?
Bliższe spojrzenie na mechanizmy uszkodzenia wątroby
Włóknienie zaczyna się, gdy główne komórki czynnościowe wątroby, zwane hepatocytami, są wielokrotnie uszkadzane. W badaniu użyto dobrze znanego związku chemicznego, czterochlorku węgla, by naśladować przewlekłe uszkodzenie wątroby u myszy i w hodowlach komórek wątrobowych myszy. Leczone myszy wykazały cechy choroby wątroby obserwowane u ludzi: podwyższone markery uszkodzenia wątrobowego we krwi, zaburzenia metabolizmu tłuszczów i cholesterolu, zapalenie oraz obfite depozyty materiału przypominającego bliznę, które zaburzają normalną architekturę wątroby. Te zmiany potwierdzają, że model wiernie odtwarza łańcuch zdarzeń prowadzący od prostego uszkodzenia do trwałego bliznowacenia.
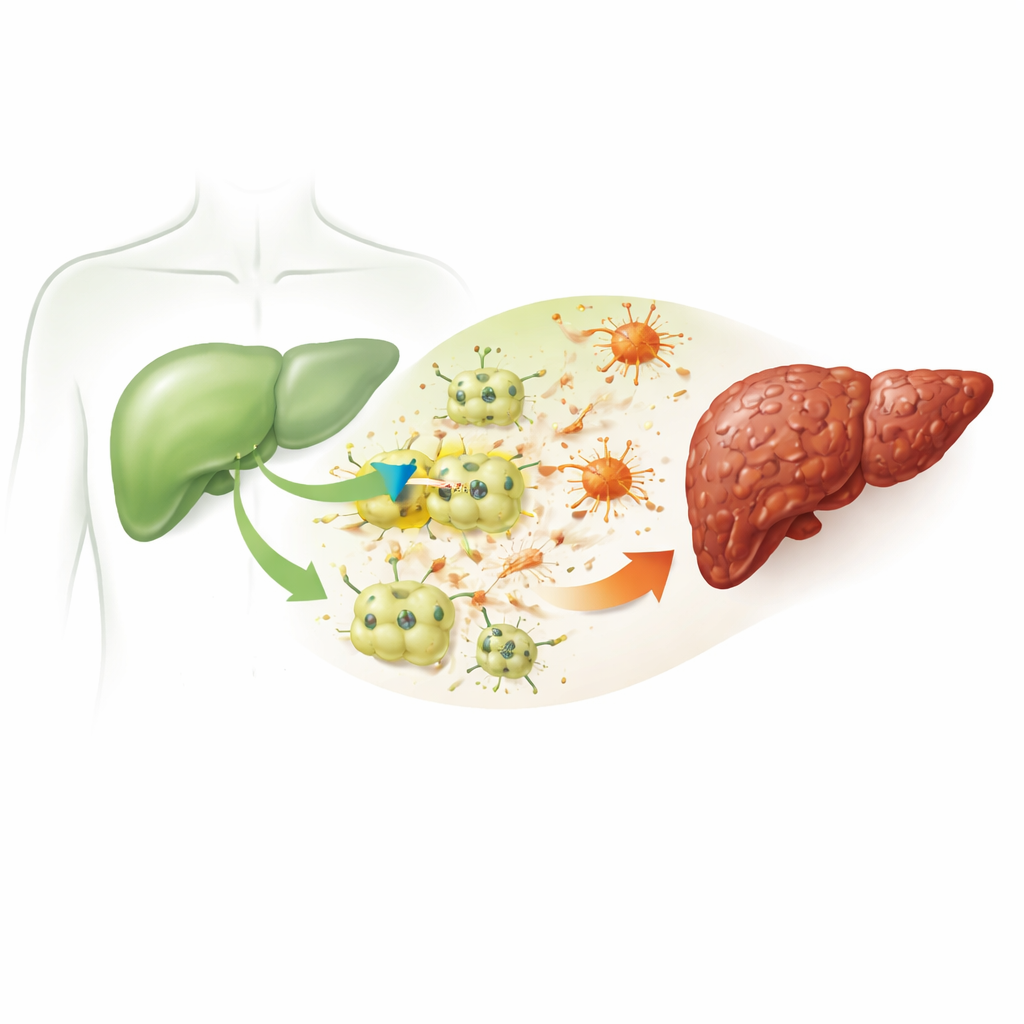
Ukryty kanał, który pojawia się w chorych komórkach wątroby
Zespół skoncentrował się na białku o nazwie ITPR3, kanale uwalniającym wapń z wewnętrznych zbiorników komórkowych. Zdrowe hepatocyty normalnie w ogóle nie wytwarzają tego kanału. Jednak zarówno w uszkodzonych wątrobach myszy, jak i w chemicznie obciążonych komórkach wątroby hodowanych w laboratorium, badacze stwierdzili wyraźny wzrost poziomu ITPR3. Tam, gdzie pojawiał się ITPR3, komórki wątroby znacznie częściej przechodziły programowaną śmierć komórkową, formę kontrolowanej autodestrukcji. Kiedy naukowcy użyli narzędzia genetycznego (siRNA) do zmniejszenia ekspresji ITPR3, fala wewnętrznego wapnia zniknęła, a częstość śmierci komórek spadła gwałtownie. Płyn z tych uszkodzonych hepatocytów mógł także przekształcić pobliskie komórki podporowe, zwane komórkami gwiaździstymi wątroby, w aktywny stan produkujący bliznę — zmiana ta była osłabiona, gdy ITPR3 zostało stłumione.
Od sygnału wapniowego do zapalnego przełącznika
Wapń to nie tylko minerał budulcowy; wewnątrz komórek krótkie impulsy wapniowe działają jako sygnały włączające i wyłączające szlaki. Autorzy pokazali, że nadmiar wapnia uwolniony przez nowo pojawiające się kanały ITPR3 uruchamia dobrze znany regulator zapalny, NF‑κB. W uszkodzonych wątrbach myszy i w hodowlach hepatocytów NF‑κB przemieścił się z cytoplazmy do jądra komórkowego, gdzie kontrolowane są geny — to klasyczny znak jego aktywacji. Redukcja poziomu ITPR3 zapobiegała temu przemieszczeniu do jądra, natomiast chemiczny inhibitor NF‑κB zmniejszał śmierć komórek. Te eksperymenty łączą pojawienie się ITPR3 z falą wapnia, aktywacją NF‑κB i w konsekwencji z utratą hepatocytów, co stwarza warunki do tworzenia blizn.
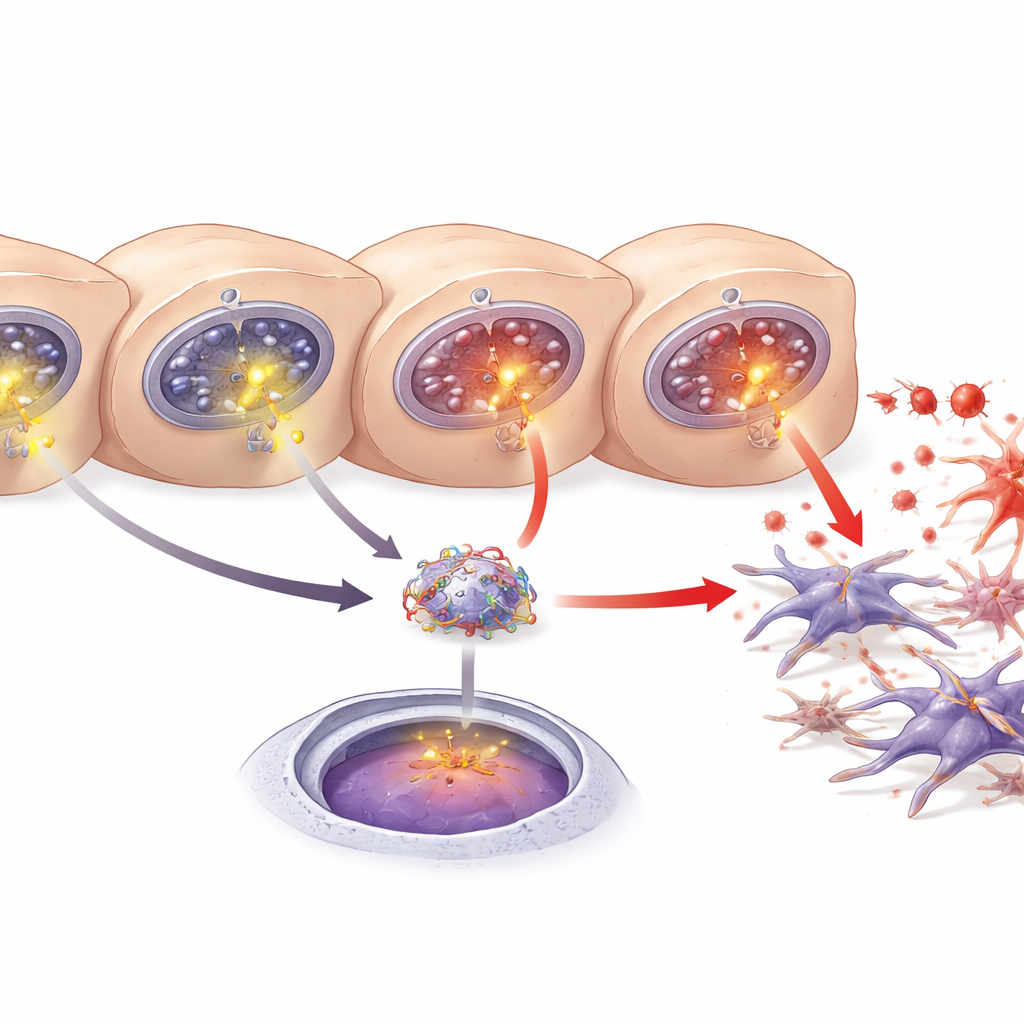
Wiadomość z wątroby, która napędza bliznowacenie
Innym kluczowym graczem jest białko pochodzące z wątroby o nazwie LECT2, wcześniej powiązane z chorobą stłuszczeniową wątroby, włóknieniem i rakiem wątroby. Naukowcy stwierdzili zwiększone stężenia LECT2 we krwi, tkance wątroby i w pożywce hodowlanej, gdy hepatocyty były uszkodzone. Wykorzystując predykcje z baz danych i genetyczne testy reporterowe, wykazali, że NF‑κB może wiązać się z konkretnym fragmentem DNA w regionie kontrolnym genu LECT2, zwiększając jego aktywność. Blokowanie NF‑κB lub redukcja ITPR3 obniżały zarówno produkcję, jak i wydzielanie LECT2. Razem wyniki opisują ciąg zdarzeń: ITPR3 pojawia się w zestresowanych hepatocytach, wywołuje dodatkowe uwalnianie wapnia, aktywuje NF‑κB, napędza produkcję LECT2 i sprzyja aktywacji komórek gwiaździstych oraz włóknieniu.
Co to oznacza dla przyszłych terapii
Mówiąc wprost, badanie identyfikuje nieprawidłowy kanał wapniowy, ITPR3, jako wstępny „wyłącznik”, który przekształca trwające uszkodzenie wątroby w trwałe bliznowacenie. Pokazując, że ITPR3 prowadzi do śmierci komórek i włóknienia poprzez konkretną ścieżkę wapń–NF‑κB–LECT2, praca wskazuje kilka potencjalnych celów terapeutycznych: sam kanał, zapalny przełącznik lub downstreamowy posłaniec wątroby. Chociaż potrzeba więcej badań u ludzi, zwłaszcza aby potwierdzić bezpieczeństwo i realne korzyści, wyniki sugerują, że wyłączenie ITPR3 mogłoby pomóc zachować hepatocyty, złagodzić stan zapalny i spowolnić lub zapobiec postępowi przewlekłej choroby wątroby w kierunku marskości.
Cytowanie: Zhao, X., Liu, X., Ni, M. et al. ITPR3 promotes liver fibrosis by damaging hepatocytes via the Ca2+/NF-B/LECT2 pathway. Sci Rep 16, 13376 (2026). https://doi.org/10.1038/s41598-026-43866-1
Słowa kluczowe: włóknienie wątroby, apoptoza hepatocytów, sygnalizacja wapniowa, szlak NF-kappaB, LECT2