Clear Sky Science · sv
STHELAR, en mångvävnadsdatamängd som länkar rumslig transkriptomik och histologi för celltypannotering
Varför mikroskopisk granskning av cancer inte räcker
Cancerläkare förlitar sig fortfarande mycket på vad de ser i mikroskopet: tunt skivade, rosafärgade och lila vävnader färgade med hematoxylin och eosin (H&E). Dessa bilder avslöjar former och mönster, men kan inte direkt visa vilka gener som är aktiva i varje cell. En ny resurs kallad STHELAR förenar dessa två världar genom att koppla den välbekanta bilden av vävnadssnitt till toppmoderna ”rumsliga” mätningar av genaktivitet. För läsare är detta viktigt eftersom det öppnar dörren för snabbare, billigare verktyg som en dag kan avläsa tumörers molekylära sammansättning från vanliga digitala bilder.
Att se tumören som ett trångt kvarter
Tumörer är mer än avvikande cancerceller; de är trånga kvarter fyllda med immunceller, blodkärl, stödjeceller och normal vävnad. Blandningen och ordningen av dessa invånare — tumörens mikromiljö — kan påverka hur en cancer växer och hur den svarar på behandling. Rumslig transkriptomik, en ny teknik, kan kartlägga vilka gener som är påslagna i individuella celler samtidigt som deras exakta position i vävnaden bevaras. Dessa experiment är dock kostsamma och tekniskt krävande, så de ingår ännu inte i rutinvården. Däremot är högupplösta skanningar av H&E‑preparat numera vanliga, billiga att lagra och redan i global användning. Den centrala idén bakom STHELAR är att använda ett begränsat antal rumsliga transkriptomikexperiment som en ”lärare” för miljoner celler som syns i standard‑H&E‑bilder.
Bygga ett stort bibliotek av märkta celler
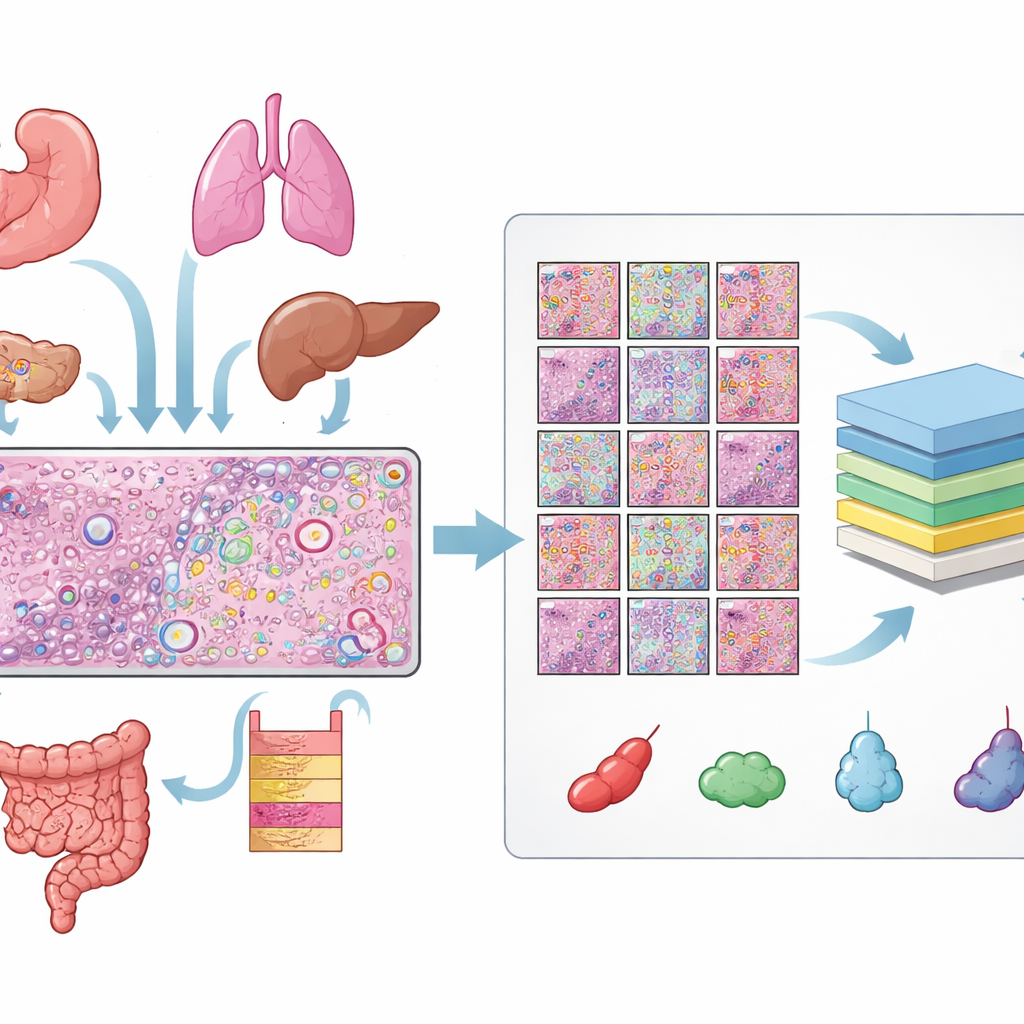
Författarna samlade data från 31 vävnadssnitt mätta med 10x Genomics Xenium‑plattform för rumslig transkriptomik, som täcker 16 typer av mänsklig vävnad samt 22 cancerprover och 9 icke‑cancerprover. För varje snitt fanns tre matchade vyer: ett H&E‑preparat, en fluorescerande bild som visar cellkärnor, och en karta över individuella RNA‑molekyler. Att alignera dessa vyer krävde noggranna kvalitetskontroller och, för många preparat, manuell finjustering så att varje kärna i den fluorescerande bilden överensstämde med motsvarande struktur i H&E‑bilden. Från dessa alineerade bilder erhöll de över 11 miljoner distinkta celler och mer än en halv miljon små H&E‑lappar, var och en med precisa konturer för varje kärna.
Lära datorn vad varje celltyp är
Att veta var varje cell sitter räcker inte; det avgörande steget är att bestämma vilken typ av cell det är. För detta kombinerade teamet rumslig transkriptomik med stora befintliga kataloger av single‑cell RNA‑profiler. Med en metod kallad Tangram överförde de först sannolika cellidentiteter från dessa referensatlaser till de rumsliga data. De förbättrade sedan dessa preliminära etiketter genom att gruppera celler i kluster baserat på deras genaktivitet och undersöka vilka gener som särskiljde varje kluster. När markörgener och Tangram var överens accepterades etiketterna; när de skilde sig åt prioriterades de lokala genmönstren i vävnaden. Slutligen harmoniserade de resultaten över alla preparat till tio breda kategorier såsom epitel, blodkärl, immuncellsgrupper, fibroblaster, melanocyter och en fång‑allt‑kategori ”övrigt”. En patolog inspekterade visuellt resultaten på H&E‑bilderna för att säkerställa att etiketterna var biologiskt rimliga.
Förvandla rika molekylkartor till träningsmaterial
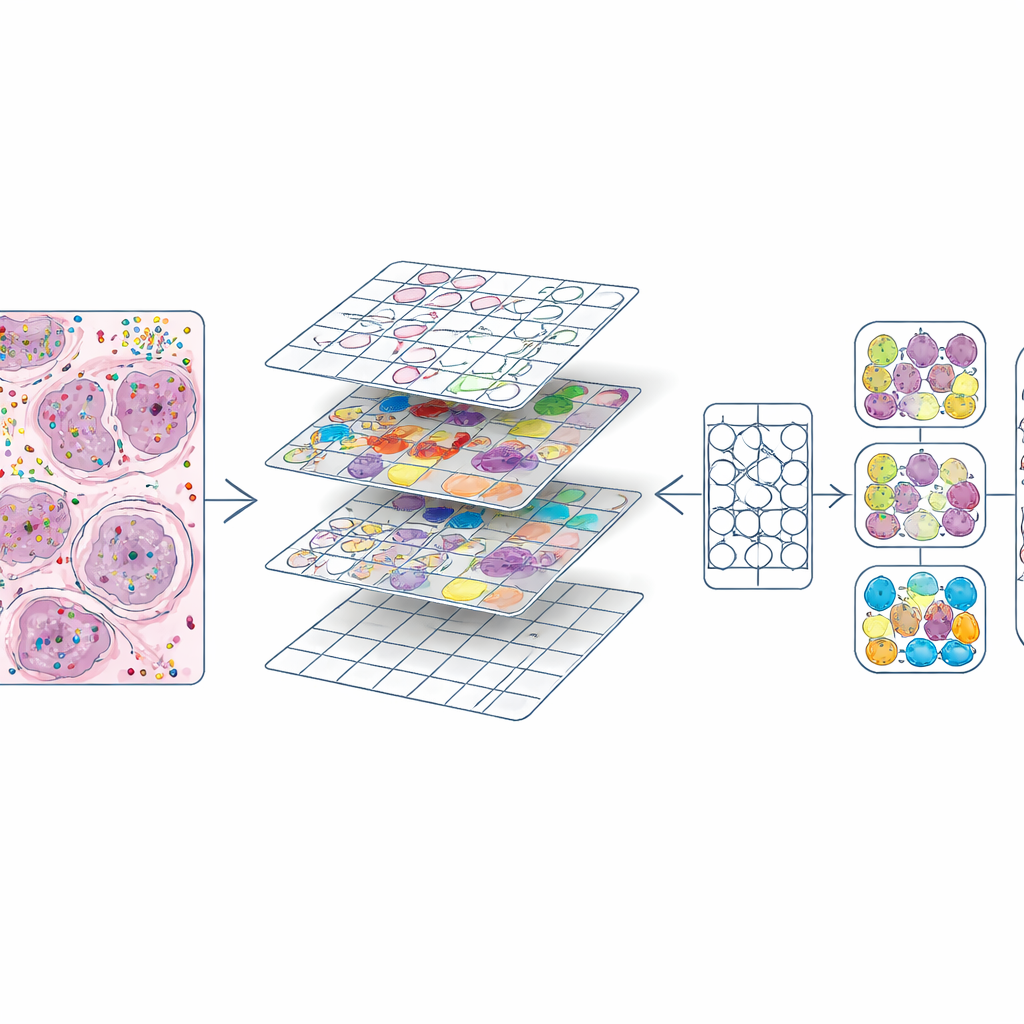
När varje cell hade både position och typ skar författarna varje H&E‑preparat i små rutor, liknande bildbrickor i ett fotoredigeringsprogram. För varje bricka producerade de två nyckelkomponenter: en mask som avgränsade varje kärna och en färgkod som angav dess celltyp. Detta skapade cirka 587 000 brickor vid hög förstoring och en något mindre mängd vid lägre förstoring. De jämförde också sina kärnkonturer med de som automatiskt producerats av en befintlig djupinlärningsmodell (CellViT) och beräknade överensstämmelsespoäng, vilket gör det möjligt för framtida användare att filtrera bort regioner av lägre kvalitet. All denna information — bilder, masker, genräkningar, cellettiketter och kvalitetsmått — paketades i standardiserade dataobjekt så att forskare enkelt kan utforska eller återanvända datamängden.
Visar att datorer kan lära av den nya atlasen
För att demonstrera vad STHELAR möjliggör finjusterade teamet CellViT‑modellen, en kraftfull vision‑transformer utformad för segmentering och klassificering av celler i H&E‑bilder. Med STHELARs etiketter som sanning tränade de modellen att känna igen nio detaljerade cellklasser och, i ett andra experiment, fem bredare grupper (till exempel genom att kombinera flera immuncellstyper). Den finjusterade modellen behöll god prestanda vid detektering och avgränsning av kärnor och uppnådde bra noggrannhet för visuellt distinkta celler såsom epitelceller och melanocyter, medan mer subtila immunsubtyper förblev utmanande. De kontrollerade också sina annoteringar mot en oberoende märkmetod (SingleR) och alternativa RNA‑baserade modeller och fann i allmänhet god överensstämmelse.
Vad detta betyder för framtida cancerdiagnostik
STHELAR är mindre en enskild algoritm än en referensatlas: en öppen, storskalig länk mellan vad patologer ser på standard‑H&E‑preparat och vad rumslig transkriptomik avslöjar om genaktivitet i varje cell. För icke‑specialister är slutsatsen att denna resurs gör det mycket enklare att träna och testa datorbaserade modeller som kan härleda tumörers cellulära sammansättning direkt från rutinbilder, utan att för varje patient behöva utföra dyra molekylära analyser. I takt med att sådana modeller förbättras kan de hjälpa läkare att läsa den osynliga molekylära ”konversationen” inne i tumörer från vanliga preparat och därigenom stödja mer precisa diagnoser och bättre riktade behandlingar.
Citering: Giraud-Sauveur, F., Blampey, Q., Benkirane, H. et al. STHELAR, a multi-tissue dataset linking spatial transcriptomics and histology for cell type annotation. Sci Data 13, 665 (2026). https://doi.org/10.1038/s41597-026-06937-6
Nyckelord: tumörmikromiljö, rumslig transkriptomik, histopatologisk avbildning, celltypannotering, djupinlärning vid cancer