Clear Sky Science · he
STHELAR, מאגר מולטי‑רקמות שמקשר בין טרנסקрипטומיקה מרחבית והיסטולוגיה לזיהוי סוגי תאים
למה המבט במיקרוסקופ לא מספיק
רופאי סרטן עדיין מסתמכים במידה רבה על מה שהם רואים דרך המיקרוסקופ: חתכים דקים של רקמות בצבעי הורוד‑סגול צבועים עם המטוקסילין ואאוזין (H&E). תמונות אלו מגלות צורות ותבניות, אך אינן יכולות להראות ישירות אילו גנים פעילים בתוך כל תא. משאב חדש בשם STHELAR מחבר בין שני העולמות הללו, ומקשר את המבט המוכר על פרוסות רקמה עם מדידות מרחביות מתקדמות של פעילות גנטית. עבור הקוראים, העבודה הזו חשובה כי היא פותחת את הדלת לכלים מהירים וזולים יותר שעשויים יום אחד לקרוא את המאפיין המולקולרי של גידולים מתוך תמונות דיגיטליות רגילות בלבד.
לראות את הגידול כשכונה צפופה
גידולים הם יותר מתאי סרטן מתרעמים; הם שכונות צפופות מלאות תאי חיסון, כלי דם, תאים תומכים ורקמה נורמלית. התערובת והסידור של התושבים האלה — מיקרו‑הסביבה של הגידול — יכולים לעצב כיצד הסרטן גדל וכיצד הוא מגיב לטיפול. טרנסקריפטומיקה מרחבית, טכנולוגיה חדשה יחסית, יכולה למפות אילו גנים נדלקים בתאים בודדים תוך שמירה על מיקומם המדויק ברקמה. עם זאת, ניסויים אלה יקרים ומורכבים טכנית, ולכן הם עדיין אינם חלק מהטיפול השגרתי. לעומת זאת, סריקות ברזולוציה גבוהה של פרוסות H&E נפוצות כיום, זולות לאחסון ומשמשות כבר ברחבי העולם. הרעיון המרכזי מאחורי STHELAR הוא להשתמש בערכת ניסויי טרנסקריפטומיקה מרחבית מוגבלת כמורה עבור מיליוני תאים הנראים בתמונות H&E סטנדרטיות.
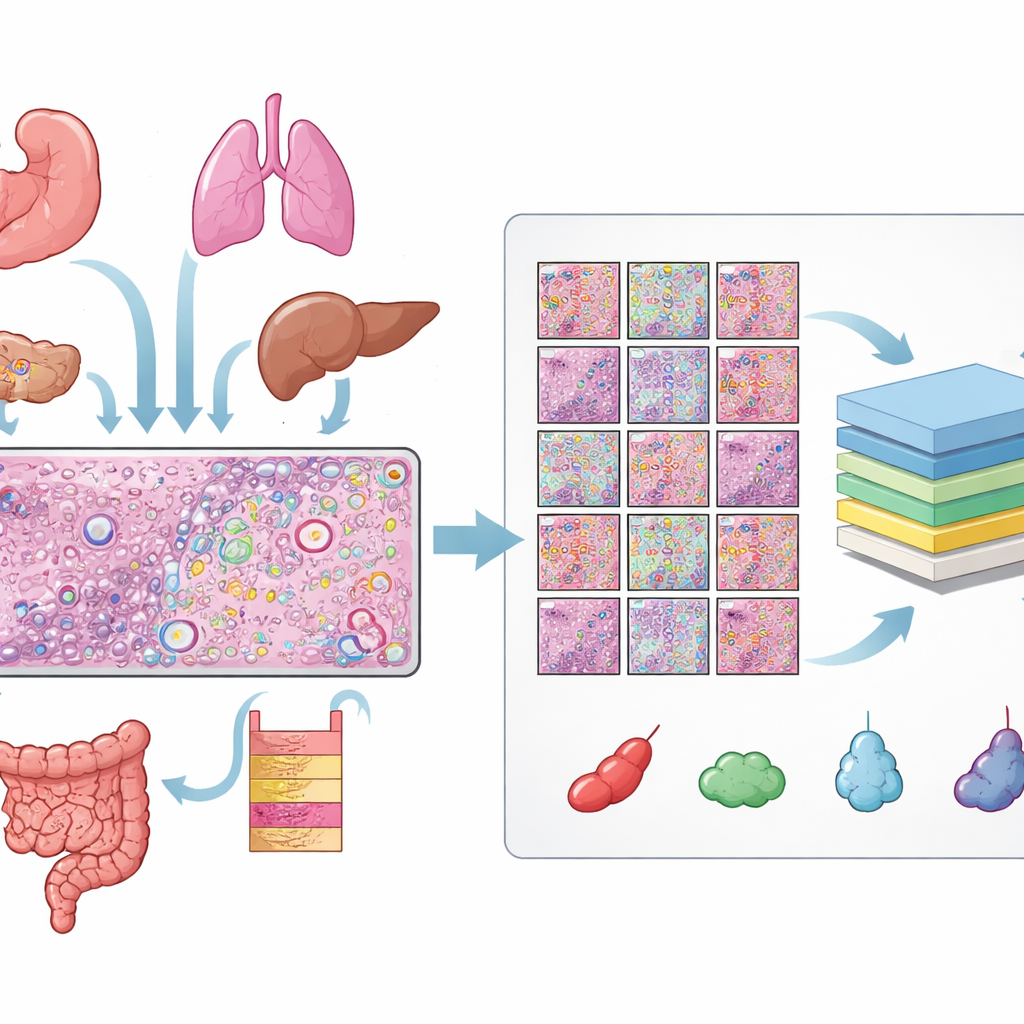
בניית ספרייה עצומה של תאים מתויגים
החוקרים אספו נתונים מ‑31 פרוסות רקמה שנמדדו עם פלטפורמת הטרנסקריפטומיקה המרחבית Xenium של 10x Genomics, הכוללות 16 סוגי רקמות אנושיות ו‑22 דגימות סרטניות ו‑9 שאינן סרטניות. לכל פרוסה היו שלוש תצפיות מותאמות: פרוסת H&E, תמונה פלואורסצנטית המציגה את גרעיני התאים, ומפה של מולקולות RNA אינדיבידואליות. יישור התצפיות הללו דרש בדיקות איכות קפדניות ולרבים מהפרוסות התאמות עדינות ידניות כך שכל גרעין בתמונה הפלואורסצנטית יתחבר למבנה המתאים בפרוסת H&E. מהתמונות המיושרות הללו הם קיבלו מעל 11 מיליון תאים מובדלים ויותר מחצי מיליון חתיכות H&E קטנות, כל אחת עם מתארים מדויקים של כל גרעין.
ללמד את המחשב מהו כל סוג תא
לדעת היכן כל תא יושב זה לא מספיק; השלב הקריטי הוא להחליט איזה סוג תא זה. לשם כך הצוות שילב את הטרנסקריפטומיקה המרחבית עם קטלוגים רחבי היקף של פרופילים של RNA בתא יחיד. באמצעות שיטה בשם Tangram הם העבירו תחילה זהויות תא סבירות מאטלסים אלה אל הנתונים המרחביים. לאחר מכן שיפרו תוויות ראשוניות אלו על‑ידי קיבוץ תאים לצבצים על בסיס פעילות הגנים ובחינת אילו גנים מבדילים כל אשכול. כאשר גני סימון ו‑Tangram הסכימו, התוויות התקבלו; כאשר הם סתרו, דפוסי הגנים המקומיים ברקמה קיבלו עדיפות. לבסוף, הם הרמוניזו את התוצאות על פני כל הפרוסות לעשר קטגוריות רחבות כגון תאים אפיתליאליים, כלי דם, קבוצות תאי חיסון, פיברובלסטים, מלנוציטים, וקבוצת "אחר" מקיפה. פתולוג בחן חזותית את התוצאות בתמונות H&E כדי לוודא שהתוויות הגיוניות ביולוגית.
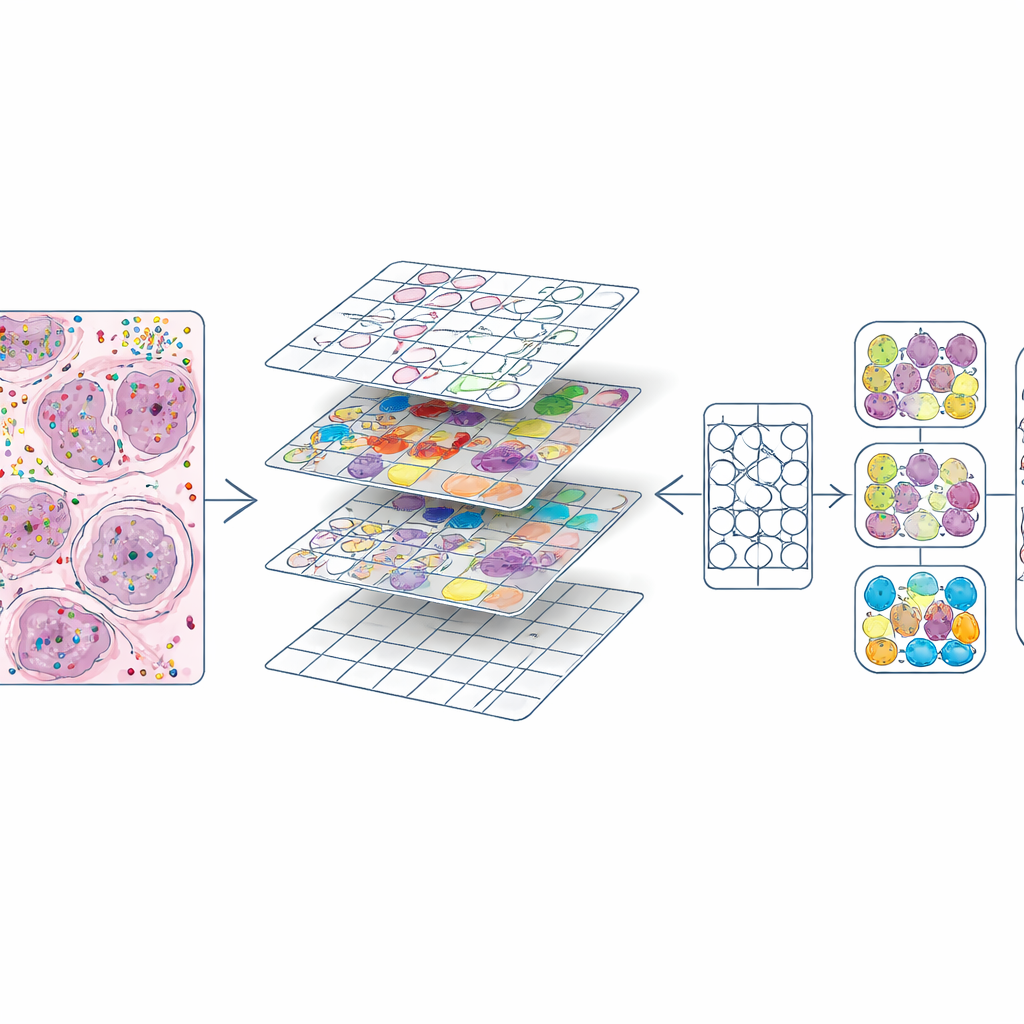
הפיכת מפות מולקולריות עשירות לחומר אימון
ברגע שלכל תא היה גם מיקום וגם סוג, המחברים חתכו כל פרוסת H&E לריבועים קטנים, בדומה לפסי תמונה בתוכנת עריכת תמונות. עבור כל ריבוע הם יצרו שני מרכיבים מרכזיים: מסכה המתארת כל גרעין וקוד צבע המציין את סוג התא. זה יצר כ‑587,000 ריבועים ברזולוציה גבוהה וקבוצה מעט קטנה יותר ברזולוציה נמוכה. הם גם השוו את מתארי הגרעין שלהם לאלה שיוצרו אוטומטית על‑ידי מודל למידה עמוקה קיים (CellViT) וחישבו ציוני הסכמה, מה שאפשר למשתמשים בעתיד לסנן אזורים באיכות נמוכה. כל המידע הזה — תמונות, מסכות, ספירות גנים, תוויות תאים וציוני איכות — נארז לאובייקטי נתונים סטנדרטיים כך שחוקרים יוכלו בקלות לחקור או להשתמש מחדש במאגר.
הפגנת יכולת הלמידה של המחשב מהאטלס החדש
כדי להדגים מה STHELAR מאפשר, הצוות כיוונן מחדש את מודל CellViT, טרנספורמר חזותי חזק המיועד לסגמנטציה ולמיון של תאים בתמונות H&E. באמצעות תוויות STHELAR כאמת‑יסודית, הם אימנו את המודל לזהות תשע קטגוריות תא מדויקות ובניסוי שני חמש קבוצות רחבות יותר (לדוגמה, שילוב מספר סוגי תאי חיסון). המודל המכוון היטב שמר על ביצועים טובים בזיהוי ומתאר הגרעינים והשיג דיוק גבוה עבור תאים בעלי מראה מובחן כמו תאים אפיתליאליים ומלנוציטים, בעוד שתת‑סוגים חיסוניים דקים יותר נותרו מאתגרים. הם גם השוו את התוויות שלהם לשיטה עצמאית (SingleR) ולמודלים מבוססי RNA חלופיים, ובאופן כללי מצאו הסכמה טובה.
מה זה אומר לאבחון סרטן בעתיד
STHELAR היא פחות אלגוריתם יחיד ויותר אטלס ייחוס: קישור פתוח, בקנה מידה רחב, בין מה שפתולוגים רואים בפרוסות H&E סטנדרטיות לבין מה שטרנסקריפטומיקה מרחבית חושפת על פעילות הגנים בכל תא. עבור לא‑מומחים, המסקנה היא שמשאב זה מקל משמעותית על אימון ובדיקת מודלים ממוחשבים שיכולים להסיק את הרכב התאים של גידולים ישירות מתמונות שגרתיות, בלי צורך לבצע מבחנים מולקולריים יקרים לכל מטופל. ככל שמודלים כאלה ישתפרו, הם עשויים לעזור לרופאים לקרוא את ה"שיחה" המולקולרית הבלתי נראית בתוך הגידולים מתוך פרוסות רגילות, ולתמוך באבחונים מדויקים יותר ובטיפולים המותאמים טוב יותר.
ציטוט: Giraud-Sauveur, F., Blampey, Q., Benkirane, H. et al. STHELAR, a multi-tissue dataset linking spatial transcriptomics and histology for cell type annotation. Sci Data 13, 665 (2026). https://doi.org/10.1038/s41597-026-06937-6
מילות מפתח: מיקרו‑סביבת הגידול, טרנסקריפטומיקה מרחבית, דימות היסטופתולוגי, תיעוד סוגי תאים, למידה עמוקה בסרטן