Clear Sky Science · sv
2′-O-metylation‑beroende införande av N2‑metylguanosin i U6:s interna stam‑öga underlättar effektiv spliceosom‑sammansättning
Varför små RNA‑justeringar spelar roll
Inne i varje mänsklig cell redigerar en intrikat molekylär maskin kallad spliceosomen råa RNA‑budskap så att de kan bli fungerande proteiner. Denna redigering måste vara både snabb och noggrann, och den förlitar sig på små RNA‑molekyler som är kraftigt "fininställda" med kemiska märkningar. Denna artikel avslöjar hur en specifik följd av kemiska modifieringar på ett sådant RNA, kallat U6, hjälper spliceosomen att monteras korrekt och hantera särskilt svåra RNA‑segment, med potentiella implikationer för sjukdomar där splitsningen går fel.
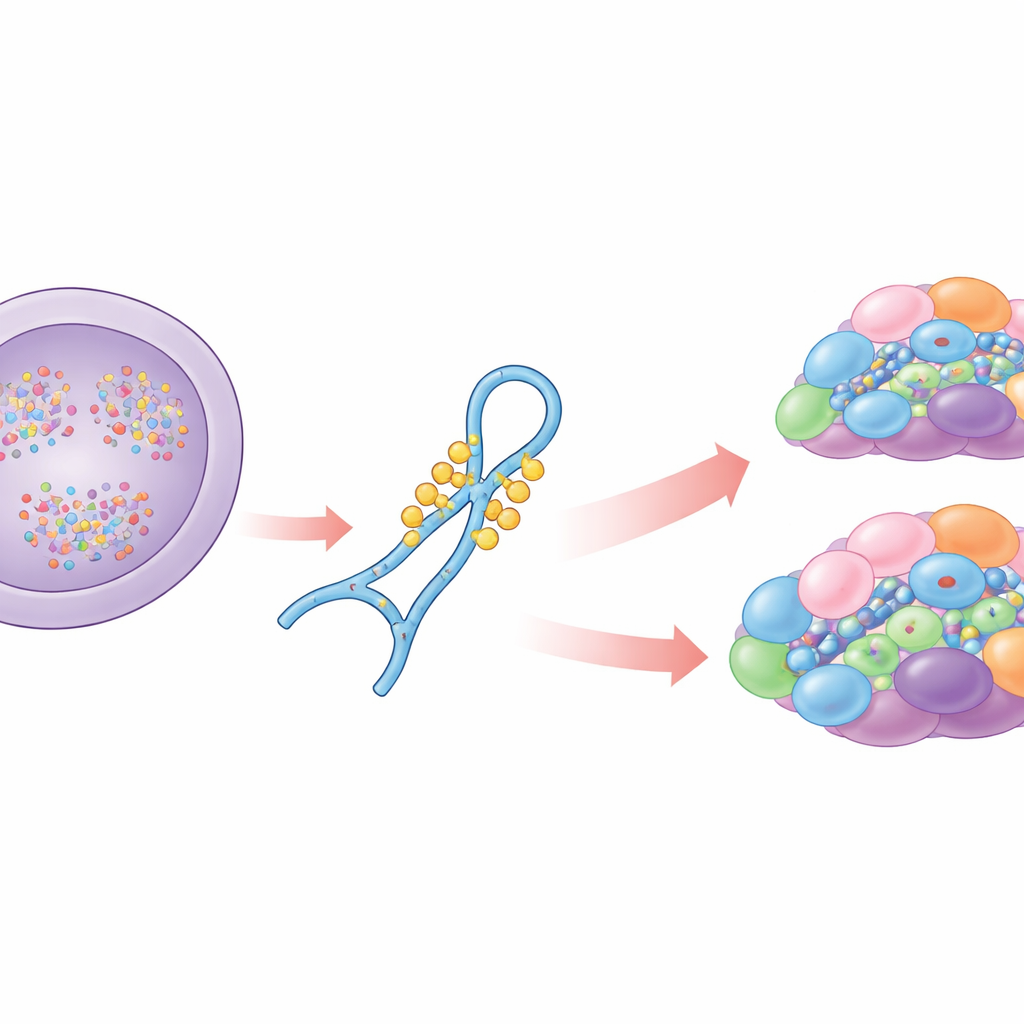
En nyckelhjälpare i RNA‑redigering
De flesta humana gener innehåller icke‑kodande avsnitt som måste tas bort från RNA innan proteiner kan tillverkas. Spliceosomen utför detta klipp‑och‑klistra‑arbete med hjälp av flera små RNA, däribland U6, som utgör en del av maskinens katalytiska kärna. U6 verkar inte ensam: det samarbetar med proteiner och andra RNA i en stegvis monteringsprocess. Under denna process modifieras U6 kemiskt på många positioner. Författarna fokuserar på en intern loop‑region i U6 som bär flera socker‑metylgrupper och en särskild modifiering på en guanosinbas. Tidigare arbete visade att basmetyleringen, känd som N2‑metylguanosin på position 72, krävs för att splitsa svaga platser och att enzymet THUMPD2 installerar denna markering. Vad som återstod att klargöra var när denna mark läggs till, hur enzymet känner igen U6 och hur dessa kemiska förändringar påverkar spliceosom‑montering och splitsning.
Sista handen tillsätts sent i U6:s liv
Genom att använda UV‑crosslinking och höggenomströmning‑sekvensering visade forskarna att THUMPD2 binder U6‑RNA mycket mer än något annat RNA i cellerna, vilket bekräftar U6 som dess huvudsakliga mål. Genom att analysera 3′‑ändarna av U6‑molekyler associerade med THUMPD2 fann de att enzymet engagerar U6 först efter att dess 3′‑ände har blivit fullständigt processad, vilket innebär att metyleringen vid position 72 är ett sent steg i U6‑mognaden. Kartläggning av proteininteraktioner visade att THUMPD2 associerar med U6‑innehållande komplex och tidiga splitsningsfaktorer, men inte med de allra tidigaste biogenesfaktorerna. Fluorescensmikroskopi placerade sedan THUMPD2 i Cajal‑kroppar—nukleära substrukturer där sena steg i spliceosom‑monteringen sker—vilket stöder idén att guanosinmetyleringen är en av de slutliga kvalitetskontroll‑markörerna innan U6 går med i större spliceosomala komplex.
Tvärspel mellan socker‑ och basmodifieringar
För att förstå hur THUMPD2 känner igen U6 kombinerade teamet strukturell modellering, crosslinking‑masspektrometri och mutanalys. De byggde en modell där U6:s interna stam‑öga vilar mot både THUMP RNA‑bindande domän och THUMPD2:s katalytiska metyltransferasdomän, vilket placerar målbasen nära enzymets aktiva yta. De visade sedan att båda domänerna krävs för att greppa U6 stabilt, medan ett litet partnerprotein, TRMT112, är nödvändigt för THUMPD2:s katalytiska aktivitet. Slående nog visade test‑rörsmetyleringsassay att THUMPD2 knappt modifierar en omodifierad U6‑loop men arbetar mer än tio gånger effektivare när två närliggande ribossockrar i motsatt sträng redan är 2′‑O‑metylade. I celler minskade utarmning av LARP7—en faktor som behövs för att installera dessa socker‑metylgrupper—både socker‑märkena och guanosinmetyleringen. Ändå var bindningsstyrkan mellan THUMPD2 och U6 likartad med eller utan socker‑metylering, vilket indikerar att dessa föregående märken justerar själva reaktionssteget snarare än den initiala igenkänningen.
Påverkan på splitsningsmönster och spliceosom‑montering
Författarna undersökte därefter hur dessa kemiska märken påverkar faktisk gen‑splitsning. Genom att jämföra RNA‑sekvenseringsdata från celler som saknar THUMPD2, celler där LARP7 är utarmat, och celler som saknar båda fann de att varje störning subtilt men signifikant ändrade alternativa splitsningsval. Förlust av guanosinmetyleringen ensam ledde främst till ökad retention av introner, särskilt i introner som redan splitsas ineffektivt. I kontrast försköt förlust av socker‑metylering användningen av alternativa 3′‑spliceplatser mot mer avlägsna alternativ. När båda typerna av modifieringar var påverkade var antalet berörda splitsningshändelser störst, och de kombinerade effekterna kunde till stor del förklaras som en additiv blandning av de individuella felen. Biokemisk fraktionering av nukleära extrakt avslöjade de bakomliggande monteringsfelen: utan basmetylering ackumulerades U6 i intermediära små RNA–protein‑komplex, vilket tyder på en fördröjd övergång till fullbildade spliceosomer. Utan socker‑metylering gick mycket mindre U6 alls in i små nukleära ribonukleoproteinpartiklar, och viktiga spliceosomala komponenter var fel‑fördelade, vilket pekar på ett mer grundläggande monteringsproblem.
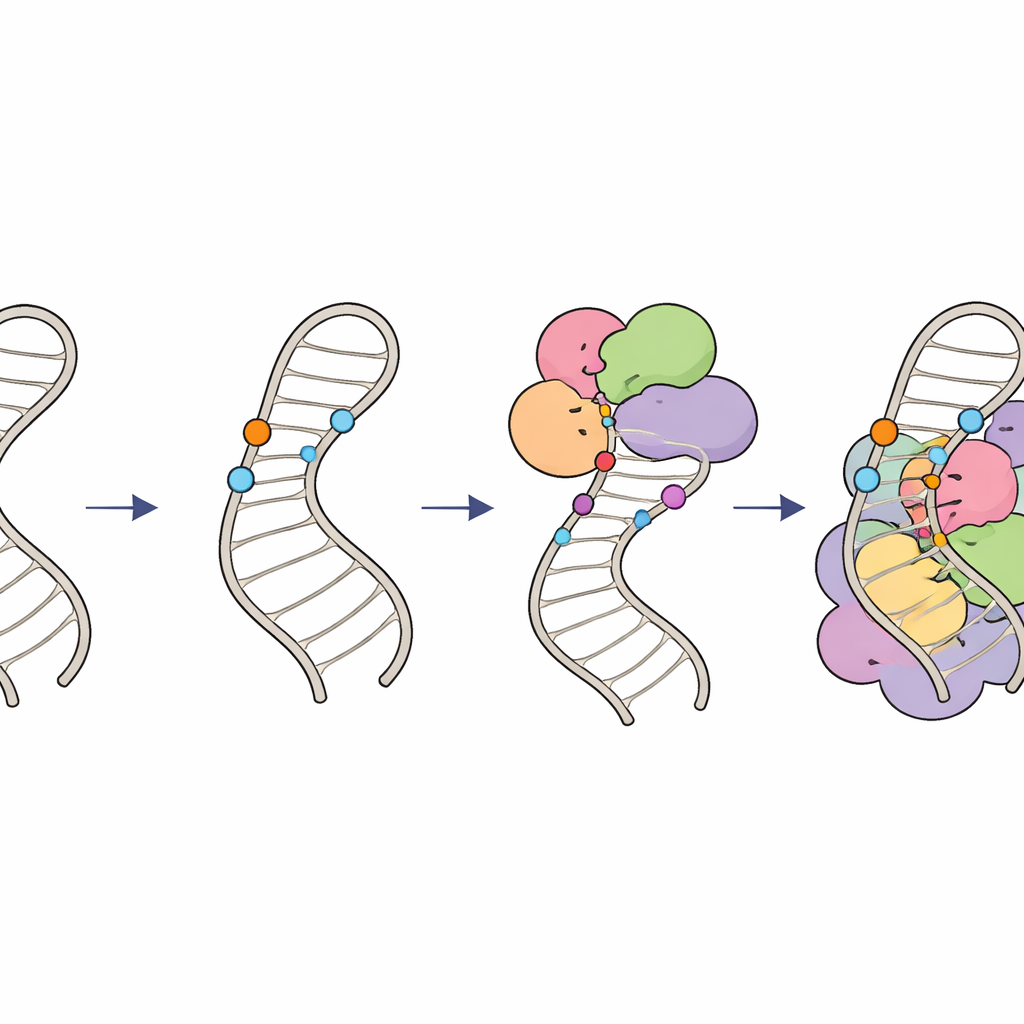
Hur kemiska märken håller RNA‑redigeringen på rätt spår
Tillsammans beskriver dessa fynd en hierarkisk "modifieringskrets" på U6‑RNA. Först placerar specialiserade guide‑RNA och faktorn LARP7 2′‑O‑metylgrupper på socker inom den interna stam‑loopen, vilket formar dess struktur och skapar ett optimalt substrat. Därefter lägger THUMPD2–TRMT112‑enzymkomplexet till en avslutande metylgrupp på en specifik bas, sannolikt fungerande som en sista licens för att U6 ska kunna gå vidare in i högre ordningens spliceosomala komplex. Genom att samordna när och var dessa små kemiska märken uppträder säkerställer cellerna att U6 är korrekt veckad och insatt i spliceosomen med precis rätt timing, vilket upprätthåller noggrann och effektiv RNA‑splitsning. Subtila fel i detta system kan sprida sig och ändra splitsningsmönster över genomet och kan bidra till mänskliga sjukdomar kopplade till splitsningsfel.
Citering: Kleiber, N., Petrosyan, J., Greve, M. et al. 2′-O-methylation-dependent installation of N2-methylguanosine in the U6 internal stem loop facilitates efficient spliceosome assembly. Nat Commun 17, 3793 (2026). https://doi.org/10.1038/s41467-026-72355-2
Nyckelord: RNA-splitsning, U6 snRNA, RNA‑modifieringar, spliceosom‑sammansättning, THUMPD2