Clear Sky Science · ru
Зависимая от 2′-O‑метилирования установка N2‑метилгуанозина во внутренней петле U6 облегчает эффективную сборку сплайсосомы
Почему важны крошечные модификации РНК
В каждой человеческой клетке сложный молекулярный аппарат — сплайсосома — правит «сырые» РНК‑сообщения, чтобы их можно было превратить в работающие белки. Эта редакция должна проходить быстро и точно, и за неё отвечают небольшие РНК, сильно «настроенные» химическими метками. В этой работе показано, как определённая последовательность химических изменений на одной из таких РНК, называемой U6, помогает сплайсосоме правильно собираться и справляться с особенно трудными участками РНК; это может иметь значение для болезней, связанных с дефектами сплайсинга.
Ключевой помощник в редактировании РНК
Большинство человеческих генов содержат некодирующие участки, которые нужно удалить из РНК до синтеза белков. Сплайсосома выполняет эту вырезку и склеивание с участием нескольких малых РНК, среди которых U6, входящая в каталитическое ядро комплекса. U6 не действует в одиночку: он взаимодействует с белками и другими РНК в пошаговом процессе сборки. По пути U6 химически модифицируется в нескольких позициях. Авторы сосредоточились на внутренней петле U6, которая несёт несколько 2′‑O‑метильных сахаров и особую модификацию на одном гуанозиновом нуклеотиде. Ранее показали, что метилирование основания, известное как N2‑метилгуанозин в позиции 72, необходимо для сплайсинга слабых сайтов, и что фермент THUMPD2 устанавливает эту метку. Оставалось неясным, когда добавляется эта метка, как фермент распознаёт U6 и как эти химические изменения влияют на сборку сплайсосомы и сам сплайсинг.
Финальная правка, вносимая на позднем этапе жизни U6
С помощью УФ‑скрещивания и высокопроизводительного секвенирования исследователи показали, что THUMPD2 связывается с U6 РНК значительно сильнее, чем с любой другой РНК в клетке, подтвердив U6 как основной мишень фермента. Анализ концов молекул U6, ассоциированных с THUMPD2, показал, что фермент взаимодействует с U6 только после полной обработки его 3′‑конца, то есть метилирование в позиции 72 — позднее событие в созревании U6. Карты взаимодействий белков выявили, что THUMPD2 ассоциирует с комплексами, содержащими U6, и с ранними факторами сплайсинга, но не с самыми ранними биогенетическими факторами. Флуоресцентная микроскопия поместила THUMPD2 в тела Кахаля — ядерные субструктуры, где происходят поздние этапы сборки сплайсосомы — что поддерживает идею о том, что метилирование гуанозина является одним из финальных контрольных знаков прежде, чем U6 войдёт в более крупные сплайсосомные комплексы.
Взаимодействие между модификациями сахара и основания
Чтобы понять, как THUMPD2 узнаёт U6, команда сочетала структурное моделирование, масс‑спектрометрию скрещивающих пептидных связей и мутационный анализ. Они построили модель, в которой внутренняя стеблевая петля U6 размещается между THUMP‑доменом отдачи РНК и каталитическим метилтрансферазным доменом THUMPD2, приближая целевое основание к активному центру фермента. Затем показали, что оба домена необходимы для стабильного захвата U6, а небольшой партнёр‑белок TRMT112 обязателен для каталитической активности THUMPD2. Поразительно, что in vitro‑ассай показал: THUMPD2 почти не модифицирует немодифицированную петлю U6, но работает более чем в десять раз эффективнее, когда два соседних рибозных сахара в противоположной цепи уже 2′‑O‑метилированы. В клетках истощение LARP7 — фактора, необходимого для установки этих сахарных меток — уменьшало как метилирование сахаров, так и метилирование гуанозина. При этом прочность связывания THUMPD2 с U6 была схожей с метками или без них, что указывает на то, что предварительные метки регулируют сам реакционный шаг, а не начальное распознавание.
Влияние на схемы сплайсинга и сборку сплайсосомы
Далее авторы изучили, как эти химические метки влияют на фактический сплайсинг генов. Сравнивая данные РНК‑секвенирования из клеток, лишённых THUMPD2, клеток с истощённым LARP7 и клеток, в которых отсутствовали оба фактора, они обнаружили, что каждое нарушение тонко, но существенно меняет выбор альтернативного сплайсинга. Потеря лишь метилирования основания в основном приводила к увеличению удержания интронов, особенно в интронах, которые и так слабо сплайсятся. Напротив, потеря сахарных меток сдвигала использование альтернативных 3′‑сайтов в сторону более удалённых вариантов. Когда страдали оба типа модификаций, число затронутых событий сплайсинга было наибольшим, и комбинированные эффекты в целом объяснялись как аддитивная сумма отдельных дефектов. Биохимическая фракционизация ядерных экстрактов выявила базовые дефекты сборки: без метилирования основания U6 накапливался в промежуточных малых РНК‑белковых комплексах, что указывает на замедление перехода к полностью сформированным сплайсосомам. Без сахарных меток гораздо меньше U6 попадало в малые нуклеопротеины вообще, и ключевые компоненты сплайсосомы были неправильно распределены, что указывает на более фундаментальную проблему сборки.
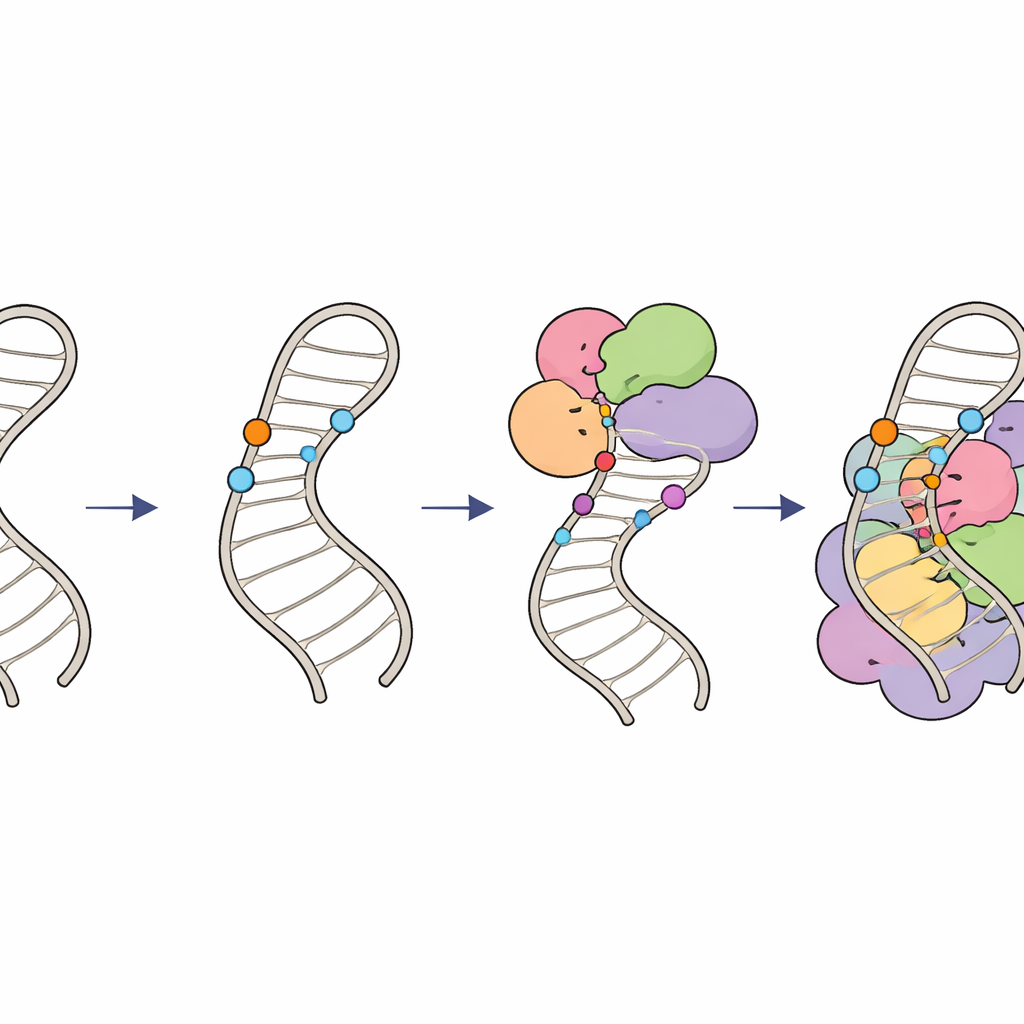
Как химические метки удерживают редакцию РНК в нужном русле
Вместе эти результаты описывают иерархическую «схему модификаций» на молекуле U6. Сначала специализированные направляющие РНК и фактор LARP7 устанавливают 2′‑O‑метильные группы на сахарах внутри внутренней стеблевой петли, формируя её структуру и создавая оптимальный субстрат. Затем ферментный комплекс THUMPD2–TRMT112 добавляет завершающую метильную группу к конкретному основанию, вероятно выступая в роли поздней лицензии, позволяющей U6 перейти в комплексы более высокого порядка сплайсосомы. Координируя время и место появления этих крошечных химических меток, клетки обеспечивают правильное сворачивание U6 и его подключение к сплайсосоме в нужный момент, сохраняя точность и эффективность РНК‑сплайсинга. Незначительные дефекты в этой системе могут распространяться и менять схемы сплайсинга по всему геному и способствовать заболеваниям человека, связанным с ошибками сплайсинга.
Цитирование: Kleiber, N., Petrosyan, J., Greve, M. et al. 2′-O-methylation-dependent installation of N2-methylguanosine in the U6 internal stem loop facilitates efficient spliceosome assembly. Nat Commun 17, 3793 (2026). https://doi.org/10.1038/s41467-026-72355-2
Ключевые слова: РНК‑сплайсинг, U6 snRNA, модификации РНК, сборка сплайсосомы, THUMPD2