Clear Sky Science · es
Instalación dependiente de 2′-O-metilación de N2-metilguanosina en el bucle interno de U6 facilita el ensamblaje eficiente del espliceosoma
Por qué importan los pequeños ajustes en el ARN
Dentro de cada célula humana, una compleja máquina molecular llamada espliceosoma edita los mensajes de ARN crudo para que puedan convertirse en proteínas funcionales. Esta edición debe ser tanto rápida como precisa, y depende de pequeños ARN que están fuertemente “afinados” con etiquetas químicas. Este artículo revela cómo una secuencia específica de ajustes químicos en uno de esos ARN, denominado U6, ayuda al espliceosoma a ensamblarse correctamente y a procesar segmentos de ARN especialmente difíciles, con posibles implicaciones para enfermedades en las que el empalme falla.
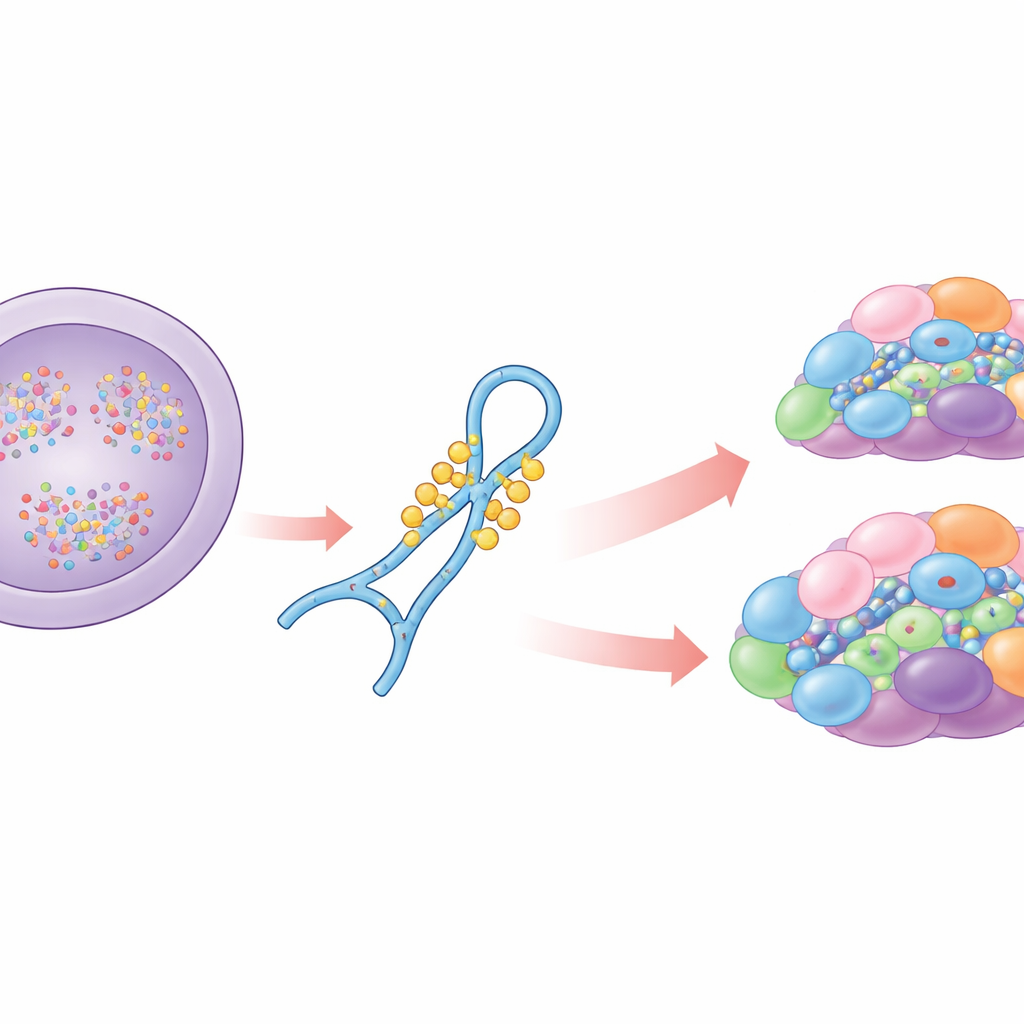
Un ayudante clave en la edición del ARN
La mayoría de los genes humanos contienen tramos no codificantes que deben eliminarse del ARN antes de que se sinteticen las proteínas. El espliceosoma realiza este recorte y pegado usando varios pequeños ARN, entre ellos U6, que forma parte del núcleo catalítico de la máquina. U6 no actúa solo: se asocia con proteínas y otros ARN en un proceso de ensamblaje por etapas. En ese recorrido, U6 se modifica químicamente en muchas posiciones. Los autores se centran en una región de bucle interno de U6 que lleva varios grupos metilo en azúcares y una modificación especial en una base guanosina. Trabajos anteriores mostraron que la metilación de la base, conocida como N2-metilguanosina en la posición 72, es necesaria para empalmar sitios débiles y que la enzima THUMPD2 instala esta marca. Lo que permanecía desconocido era cuándo se añade esta marca, cómo la enzima reconoce U6 y cómo estos cambios químicos afectan el ensamblaje del espliceosoma y el empalme.
Toque final añadido tarde en la vida de U6
Mediante entrecruzamiento UV y secuenciación de alto rendimiento, los investigadores mostraron que THUMPD2 se une al ARN U6 mucho más que a cualquier otro ARN en las células, confirmando a U6 como su principal objetivo. Al analizar los extremos 3′ de las moléculas de U6 asociadas con THUMPD2, encontraron que la enzima interactúa con U6 solo después de que su extremo 3′ ha sido completamente procesado, lo que significa que la metilación en la posición 72 es un evento tardío en la maduración de U6. El mapeo de interacciones proteicas reveló que THUMPD2 se asocia con complejos que contienen U6 y con factores tempranos de empalme, pero no con los factores de biogénesis más precoces. La microscopía de fluorescencia situó a THUMPD2 en los cuerpos de Cajal —subestructuras nucleares donde ocurren los pasos finales del ensamblaje del espliceosoma—, apoyando la idea de que la metilación de la guanosina es una de las marcas finales de control de calidad antes de que U6 se incorpore a ensamblajes espliceosomales mayores.
Interacción entre modificaciones en azúcar y en base
Para entender cómo THUMPD2 reconoce U6, el equipo combinó modelado estructural, espectrometría de masas tras entrecruzamiento y análisis mutacional. Construyeron un modelo en el que el bucle interno de U6 se acopla contra el dominio THUMP de unión al ARN y el dominio metiltransferasa catalítico de THUMPD2, situando la base objetivo cerca del sitio activo de la enzima. Luego demostraron que ambos dominios son necesarios para sujetar U6 de forma estable, mientras que una pequeña proteína asociada, TRMT112, es esencial para la actividad catalítica de THUMPD2. De forma destacada, ensayos de metilación in vitro revelaron que THUMPD2 modifica apenas un bucle U6 no modificado, pero actúa más de diez veces con mayor eficiencia cuando dos ribosas cercanas en la hebra opuesta ya están 2′-O-metiladas. En células, la depleción de LARP7 —un factor necesario para instalar estos grupos metilo en azúcares— redujo tanto las marcas en el azúcar como la metilación de la guanosina. Sin embargo, la fuerza de unión entre THUMPD2 y U6 fue similar con o sin metilación en azúcares, lo que indica que estas marcas previas afinan el paso catalítico en sí, no el reconocimiento inicial.
Impacto en los patrones de empalme y en el ensamblaje del espliceosoma
Los autores preguntaron a continuación cómo estas marcas químicas influyen en el empalme génico real. Al comparar datos de secuenciación de ARN de células sin THUMPD2, células con depleción de LARP7 y células que carecían de ambos, encontraron que cada perturbación alteró de forma sutil pero significativa las elecciones de empalme alternativo. La pérdida solo de la metilación de la guanosina condujo principalmente a un aumento de la retención de intrones, en particular en intrones que ya se empalman de manera ineficiente. En contraste, la pérdida de las metilaciones en azúcares desplazó el uso de sitios de empalme 3′ alternativos hacia opciones más distantes. Cuando ambos tipos de modificación estaban perturbados, el número de eventos de empalme afectados fue el mayor, y los efectos combinados podían explicarse en gran medida como una suma aditiva de los defectos individuales. La fraccionación bioquímica de extractos nucleares reveló los defectos de ensamblaje subyacentes: sin la metilación de la base, U6 se acumuló en complejos intermediarios ARN-proteína pequeños, lo que sugiere una progresión ralentizada hacia espliceosomas totalmente formados. Sin las metilaciones en los azúcares, mucho menos U6 ingresó a ribonucleoproteínas nucleares pequeñas en absoluto, y componentes clave del espliceosoma se redistribuyeron incorrectamente, apuntando a un problema de ensamblaje más fundamental.
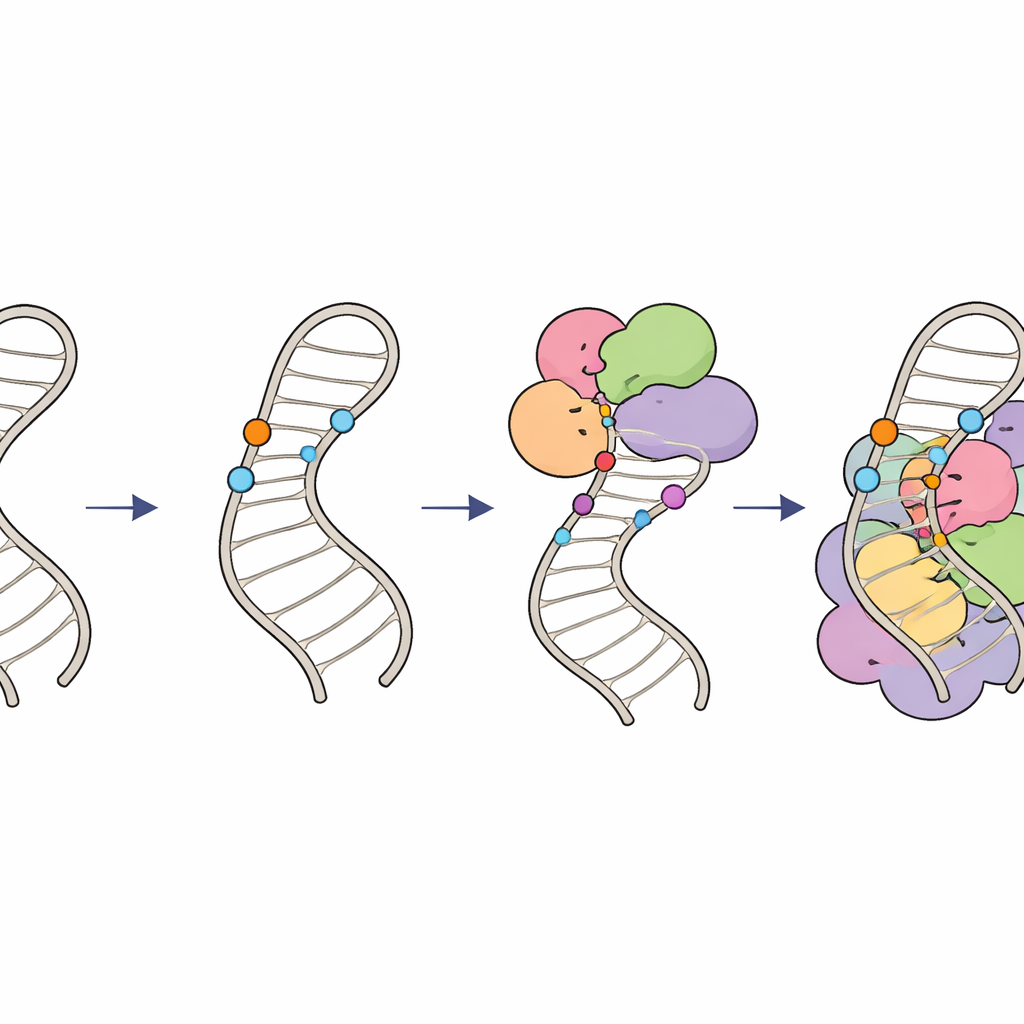
Cómo las marcas químicas mantienen la edición del ARN en rumbo
En conjunto, estos hallazgos describen un “circuito de modificación” jerárquico en el ARN U6. Primero, ARN guía especializados y el factor LARP7 colocan grupos 2′-O-metilo en las ribosas dentro del bucle interno, moldeando su estructura y creando un sustrato óptimo. Luego, el complejo enzimático THUMPD2–TRMT112 añade un grupo metilo final a una base específica, actuando probablemente como una licencia de última etapa para que U6 progrese hacia complejos espliceosomales de orden superior. Al coordinar cuándo y dónde aparecen estas pequeñas marcas químicas, las células aseguran que U6 se pliegue correctamente y se incorpore al espliceosoma con el momento justo, manteniendo un empalme de ARN preciso y eficiente. Defectos sutiles en este sistema pueden propagarse y cambiar los patrones de empalme en todo el genoma y pueden contribuir a enfermedades humanas relacionadas con errores de empalme.
Cita: Kleiber, N., Petrosyan, J., Greve, M. et al. 2′-O-methylation-dependent installation of N2-methylguanosine in the U6 internal stem loop facilitates efficient spliceosome assembly. Nat Commun 17, 3793 (2026). https://doi.org/10.1038/s41467-026-72355-2
Palabras clave: Empalme de ARN, ARNsn U6, Modificaciones de ARN, Ensamblaje del espliceosoma, THUMPD2