Clear Sky Science · pt
Instalação dependente de 2′-O‑metilação de N2‑metilguanosina no laço interno do U6 facilita a montagem eficiente do spliceossomo
Por que pequenos ajustes no RNA importam
Dentro de cada célula humana, uma máquina molecular intrincada chamada spliceossomo edita mensagens brutas de RNA para que possam ser transformadas em proteínas funcionais. Essa edição precisa ser rápida e precisa, e depende de pequenos RNAs que são fortemente “afinados” com marcas químicas. Este artigo revela como uma sequência específica de ajustes químicos em um desses RNAs, chamado U6, ajuda o spliceossomo a se montar corretamente e a processar segmentos de RNA especialmente difíceis, com possíveis implicações para doenças em que o splicing falha.
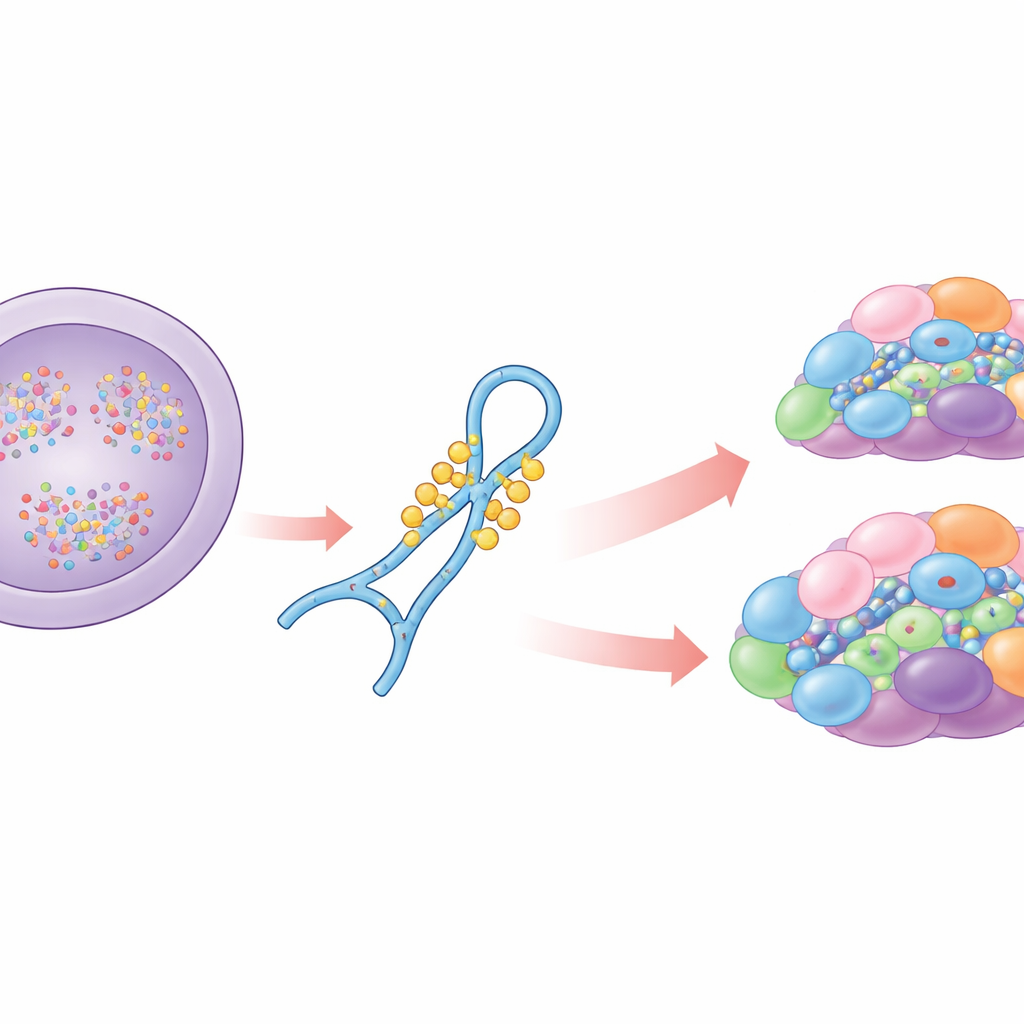
Um ajudante chave na edição do RNA
A maioria dos genes humanos contém trechos não codificantes que precisam ser removidos do RNA antes da síntese proteica. O spliceossomo realiza esse corte‑e‑colar usando vários pequenos RNAs, entre os quais o U6, que faz parte do coração catalítico da máquina. O U6 não age sozinho: ele faz par com proteínas e outros RNAs em um processo de montagem em etapas. Ao longo desse processo, o U6 é quimicamente modificado em várias posições. Os autores concentram‑se em uma região do laço interno do U6 que carrega vários grupos metil na ribose e uma modificação especial em uma base guanosina. Trabalhos anteriores mostraram que a metilação da base, conhecida como N2‑metilguanosina na posição 72, é necessária para splicar sítios fracos e que a enzima THUMPD2 instala essa marca. O que permanecia desconhecido era quando essa marca é adicionada, como a enzima reconhece o U6 e como essas alterações químicas afetam a montagem do spliceossomo e o splicing.
Toque final adicionado tardiamente na vida do U6
Usando cruzamento por UV e sequenciamento de alto rendimento, os pesquisadores mostraram que o THUMPD2 se liga ao RNA U6 muito mais do que a qualquer outro RNA nas células, confirmando o U6 como seu principal alvo. Ao analisar as extremidades 3′ de moléculas de U6 associadas ao THUMPD2, eles descobriram que a enzima interage com o U6 apenas depois que sua extremidade 3′ foi totalmente processada, o que significa que a metilação na posição 72 é um evento tardio na maturação do U6. Mapeamento de interações proteicas revelou que o THUMPD2 se associa a complexos contendo U6 e a fatores precoces de splicing, mas não aos fatores de biogênese mais iniciais. Microscopia de fluorescência então posicionou o THUMPD2 em corpos de Cajal — subestruturas nucleares onde ocorrem etapas tardias da montagem do spliceossomo — sustentando a ideia de que a metilação da guanosina é uma das marcas finais de controle de qualidade antes que o U6 se junte a montagens spliceossomais maiores.
Interdependência entre modificações na ribose e na base
Para entender como o THUMPD2 reconhece o U6, a equipe combinou modelagem estrutural, espectrometria de massa após cruzamento e análise de mutantes. Eles construíram um modelo no qual o laço interno do U6 se encaixa tanto no domínio THUMP de ligação ao RNA quanto no domínio metiltransferase catalítico do THUMPD2, posicionando a base alvo próxima ao sítio ativo da enzima. Em seguida, mostraram que ambos os domínios são necessários para segurar o U6 de forma estável, enquanto uma pequena proteína parceira, TRMT112, é essencial para a atividade catalítica do THUMPD2. Notavelmente, ensaios de metilação in vitro revelaram que o THUMPD2 mal modifica um laço U6 não modificado, mas funciona mais de dez vezes mais eficientemente quando duas riboses próximas na fita oposta já estão 2′‑O‑metiladas. Em células, a depleção de LARP7 — um fator necessário para instalar esses grupos metil na ribose — reduziu tanto as marcas na ribose quanto a metilação da guanosina. Ainda assim, a força de ligação entre THUMPD2 e U6 foi semelhante com ou sem metilação na ribose, indicando que essas marcas prévias afinam o próprio passo reacional, e não o reconhecimento inicial.
Impacto nos padrões de splicing e na montagem do spliceossomo
Os autores investigaram então como essas marcas químicas influenciam o splicing gênico real. Ao comparar dados de RNA‑sequenciamento de células sem THUMPD2, células com depleção de LARP7 e células sem ambos, eles descobriram que cada perturbação alterou de forma sutil, porém significativa, as escolhas de splicing alternativo. A perda apenas da metilação da guanosina levou principalmente ao aumento da retenção de íntrons, particularmente em íntrons que já são processados de forma ineficiente. Em contraste, a perda das metilações na ribose deslocou o uso de sítios de splicing 3′ alternativos para opções mais distantes. Quando ambos os tipos de modificação foram prejudicados, o número de eventos de splicing afetados foi o maior, e os efeitos combinados puderam ser explicados em grande parte como uma soma dos defeitos individuais. Fracionamento bioquímico de extratos nucleares revelou os defeitos de montagem subjacentes: sem a metilação da base, o U6 se acumulou em complexos intermediários de RNA–proteína pequenos, sugerindo uma progressão mais lenta para spliceossomos totalmente formados. Sem as metilações na ribose, muito menos U6 entrou em partículas ribonucleoproteicas nucleares pequenas, e componentes chave do spliceossomo foram mal distribuídos, apontando para um problema de montagem mais fundamental.
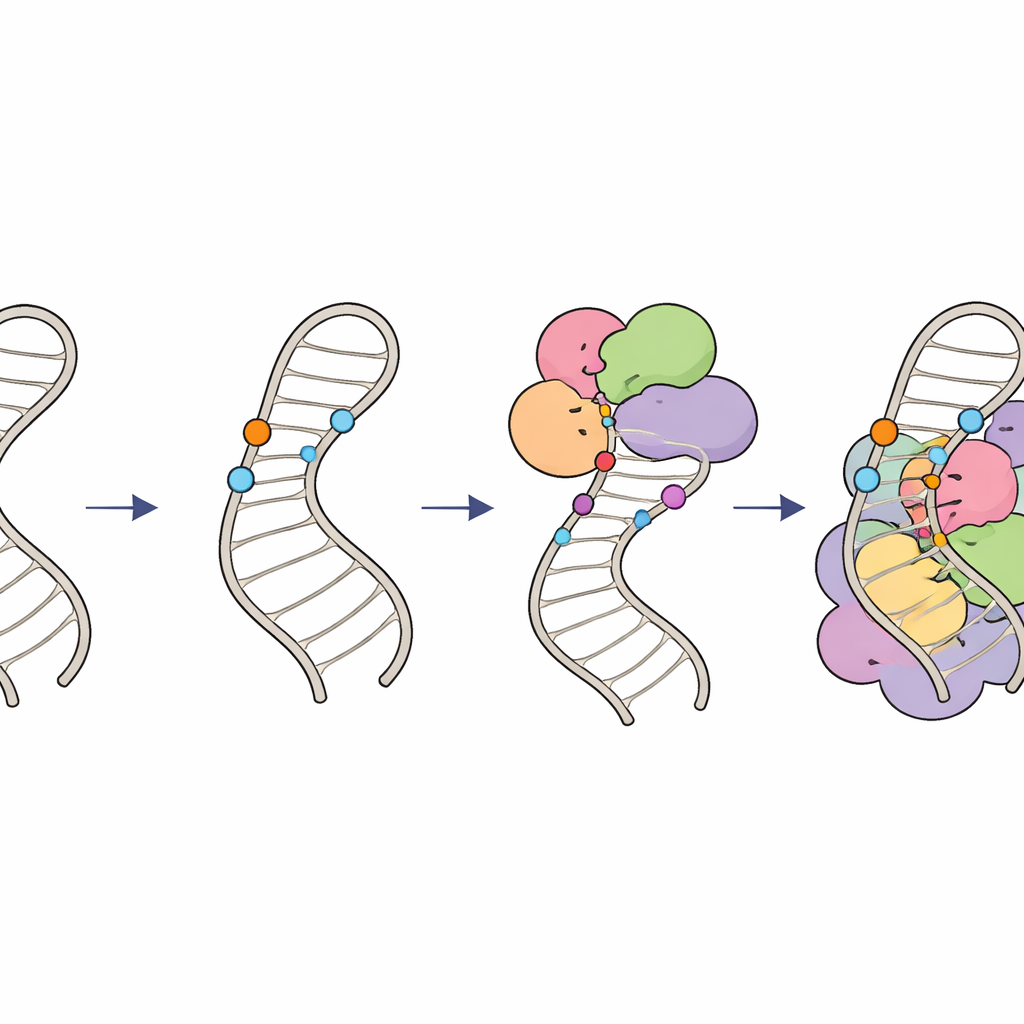
Como marcas químicas mantêm a edição do RNA nos trilhos
Em conjunto, esses achados delineiam um “circuito de modificação” hierárquico no RNA U6. Primeiro, RNAs guias especializados e o fator LARP7 colocam grupos 2′‑O‑metil nas riboses dentro do laço interno, moldando sua estrutura e criando um substrato ideal. Depois, o complexo enzimático THUMPD2–TRMT112 adiciona um grupo metil final a uma base específica, provavelmente atuando como uma autorização de estágio tardio para que o U6 progrida para complexos spliceossomais de ordem superior. Ao coordenar quando e onde essas minúsculas marcas químicas aparecem, as células garantem que o U6 esteja dobrado corretamente e integrado ao spliceossomo com o timing adequado, mantendo um splicing de RNA preciso e eficiente. Defeitos sutis nesse sistema podem repercutir por todo o genoma e contribuir para doenças humanas ligadas a erros de splicing.
Citação: Kleiber, N., Petrosyan, J., Greve, M. et al. 2′-O-methylation-dependent installation of N2-methylguanosine in the U6 internal stem loop facilitates efficient spliceosome assembly. Nat Commun 17, 3793 (2026). https://doi.org/10.1038/s41467-026-72355-2
Palavras-chave: Splicing de RNA, snRNA U6, Modificações de RNA, Montagem do spliceossomo, THUMPD2