Clear Sky Science · ja
2′-O-メチル化依存的なN2-メチルグアノシンのU6内部幹ループへの付加は効率的なスプライソーム組み立てを促進する
なぜ小さなRNAの手直しが重要なのか
すべてのヒト細胞の内部では、スプライソームと呼ばれる精密な分子機械が未加工のRNAメッセージを編集し、機能するタンパク質に翻訳できるようにしている。この編集は迅速かつ正確でなければならず、化学的タグで精巧に「微調整」された小さなRNA群に依存している。本論文は、U6と呼ばれるそのようなRNAの一つに施された特定の化学修飾の連続が、スプライソームの正しい組み立てを助け、特に扱いにくいRNA部位の処理を可能にする仕組みを明らかにしており、スプライシング異常が関与する疾患への含意を示している。
RNA編集の重要な助っ人
ほとんどのヒト遺伝子はタンパク質になる前にRNAから除かれるべき非翻訳領域(イントロン)を含む。スプライソームはこの切り貼りをいくつかの小さなRNAを用いて行い、その中でU6は装置の触媒中心の一部を構成する。U6は単独で機能するわけではなく、タンパク質や他のRNAと段階的に結合して組み立てられる。過程の中でU6は多数の部位で化学修飾を受ける。著者らはU6の内部ループ領域に注目し、そこには複数のリボース2′-O-メチル基と、1つのグアノシン塩基の特別な修飾が存在する。以前の研究は、位置72の塩基メチル化(N2-メチルグアノシン)がスプライシング効率の低い部位に必要であり、この標識は酵素THUMPD2によって付加されることを示していた。しかし、いつこの標識が付けられるのか、酵素がU6をどのように認識するのか、これらの化学変化がスプライソームの組み立てやスプライシングにどう影響するのかは不明だった。
U6の最終段階で付与される仕上げ
研究者らはUV架橋とハイスループットシーケンシングを用いて、THUMPD2が細胞内の他のどのRNAよりもU6 RNAに強く結合することを示し、U6が主要な標的であることを確証した。THUMPD2に結合したU6分子の3′末端を解析すると、酵素はU6の3′末端が完全に加工された後にのみU6に関与することが分かり、位置72のメチル化はU6成熟の後期イベントであることが示された。タンパク質相互作用マッピングでは、THUMPD2がU6含有複合体や初期のスプライシング因子と結びつく一方で、非常に初期の生合成因子とは結合しないことが明らかになった。蛍光顕微鏡観察はTHUMPD2がカジャル小体(スプライソーム組み立ての後期段階が起こる核内構造)に局在することを示し、グアノシンのメチル化がU6がより大きなスプライソーム複合体に参加する前の最終的な品質管理マークの一つであるという考えを支持した。
糖修飾と塩基修飾の相互作用
THUMPD2がU6をどのように認識するかを理解するために、チームは構造モデリング、架橋質量分析、および変異解析を組み合わせた。彼らはU6の内部幹ループがTHUMPD2のTHUMP RNA結合ドメインと触媒メチルトランスフェラーゼドメインの両方に寄り添うモデルを構築し、標的塩基が酵素の活性部位の近くに位置することを示した。続いて、両ドメインがU6を安定的に保持するために必要であり、小さなパートナータンパク質であるTRMT112がTHUMPD2の触媒活性に不可欠であることを示した。注目すべきことに、試験管内メチル化アッセイでは、THUMPD2は無修飾のU6ループをほとんど修飾しないが、対側鎖の近傍にある2つのリボースが既に2′-O-メチル化されているときには10倍以上効率的に作用した。細胞内では、これらのリボースメチルを導入するために必要な因子LARP7を枯渇させると、糖修飾とグアノシンのメチル化の両方が減少した。しかしTHUMPD2とU6の結合力は糖修飾の有無にかかわらずほぼ同じであり、これらの前駆的マークは初期認識ではなく反応段階そのものを調整していることを示している。
スプライシング様式とスプライソーム組み立てへの影響
著者らは次に、これらの化学的標識が遺伝子のスプライシングにどのように影響するかを検討した。THUMPD2欠損細胞、LARP7枯渇細胞、両者欠損の細胞のRNAシーケンスデータを比較したところ、それぞれの撹乱が代替スプライシングの選択にわずかだが有意な変化を引き起こすことが分かった。塩基メチル化の喪失だけでは主にイントロン保持の増加をもたらし、特にもともとスプライシング効率の低いイントロンで顕著だった。これに対して糖メチル化の喪失は代替3′スプライス部位の使用をより遠位の選択肢へとシフトさせた。両方の修飾が障害されると影響を受けるスプライシング事象の数は最も多くなり、両者の結合効果は個々の欠陥の加法的な混合として大部分説明できた。核抽出物の生化学的分画はその基礎にある組み立て欠陥を明らかにした:塩基メチル化がないとU6は中間的な小さなRNA–タンパク質複合体に蓄積し、完全なスプライソームへの進行が遅れることを示唆した。一方、糖メチル化が欠けるとU6が小核リボ核タンパク質粒子に入る量が大幅に減り、主要なスプライソーム成分の分布が乱れ、より根本的な組み立て障害を示した。
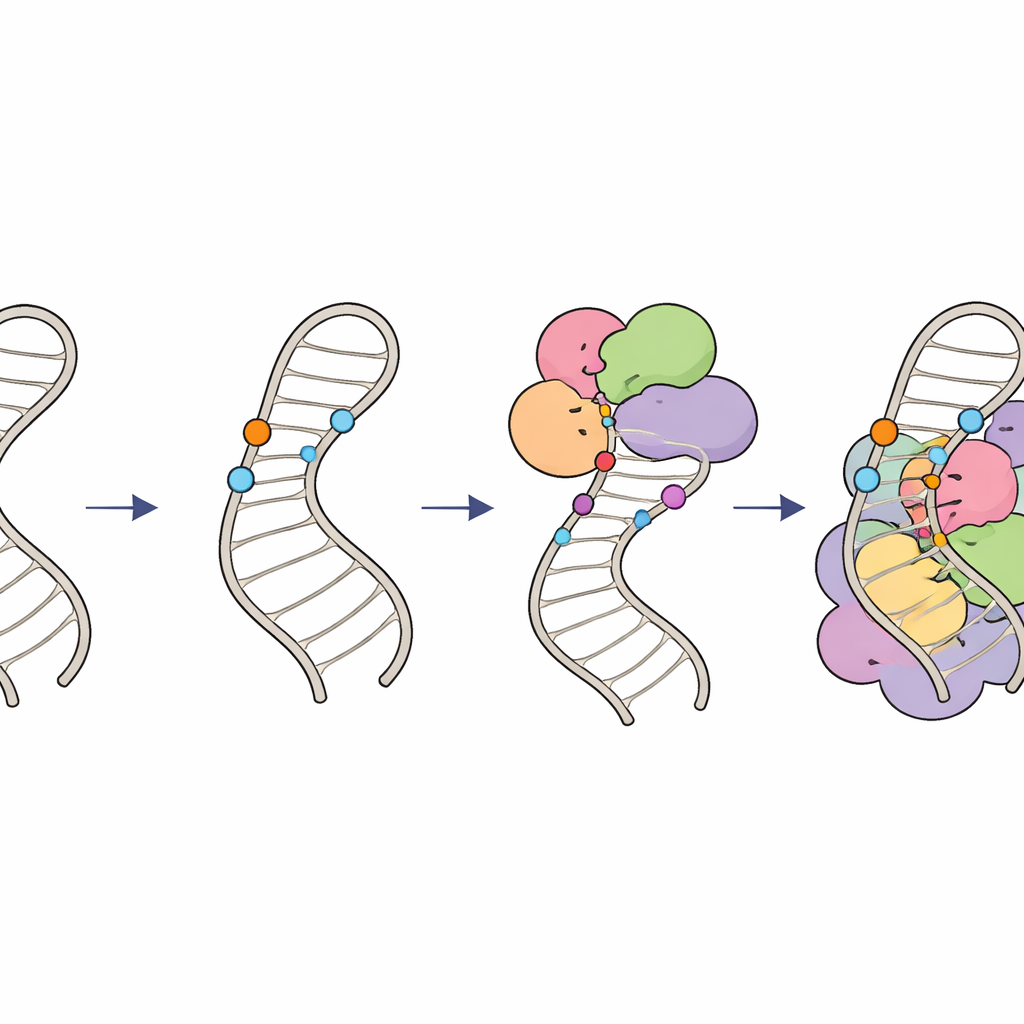
化学的マークがRNA編集を軌道に乗せる仕組み
これらの発見は、U6 RNA上に階層的な「修飾回路」が存在することを描き出している。まず、特殊なガイドRNAとLARP7因子が内部幹ループ内のリボースに2′-O-メチル基を配置し、その構造を形作って最適な基質を作る。次にTHUMPD2–TRMT112酵素複合体が特定の塩基に仕上げのメチル基を付加し、おそらくU6がより高次のスプライソーム複合体へ進行するための後期段階のライセンスとして働く。これらの小さな化学的標識がいつどこに現れるかを調整することで、細胞はU6が正しく折りたたまれ、適切なタイミングでスプライソームに組み込まれることを保証し、正確で効率的なRNAスプライシングを維持している。この系の微妙な欠陥はゲノム全体のスプライシング様式を変化させ、人の疾患に寄与する可能性がある。
引用: Kleiber, N., Petrosyan, J., Greve, M. et al. 2′-O-methylation-dependent installation of N2-methylguanosine in the U6 internal stem loop facilitates efficient spliceosome assembly. Nat Commun 17, 3793 (2026). https://doi.org/10.1038/s41467-026-72355-2
キーワード: RNAスプライシング, U6 snRNA, RNA修飾, スプライソーム組み立て, THUMPD2