Clear Sky Science · ar
التركيب المعتمد على 2′-O-مثيلة لتركيب N2-مثيلجوانينوزين في الحلقة الداخلية لـU6 يسهل تجميع سبلايسوسوم فعال
لماذا تهم التعديلات الطفيفة على الـRNA
داخل كل خلية بشرية، هناك آلة جزيئية معقدة تُسمى السبلايسوسوم تقوم بتحرير رسائل الـRNA الخام حتى يمكن تحويلها إلى بروتينات عاملة. يجب أن يكون هذا التحرير سريعًا ودقيقًا، ويعتمد على RNAs صغيرة تُزوَّد بكثافة بعلامات كيميائية "للفنِّية". تكشف هذه الورقة كيف أن تسلسلًا محددًا من التعديلات الكيميائية على أحد هذه الـRNA، المسمى U6، يساعد السبلايسوسوم على التجمع بشكل صحيح والتعامل مع مقاطع الـRNA الصعبة بشكل خاص، مع تبعات محتملة لأمراض تنطوي على خلل في القصّ.
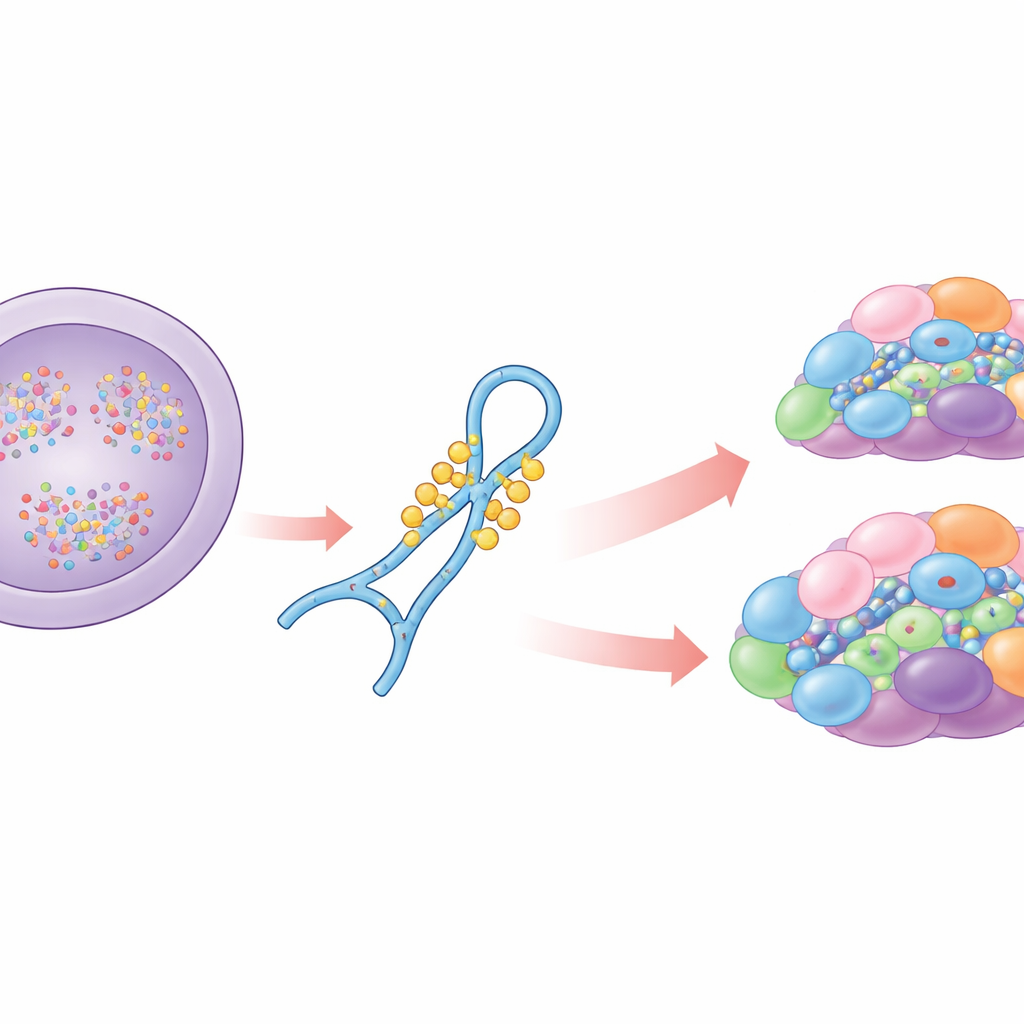
مساعد رئيسي في تحرير الـRNA
معظم الجينات البشرية تحتوي على مقاطع غير مشفرة يجب إزالتها من الـRNA قبل تصنيع البروتينات. يقوم السبلايسوسوم بعملية القصّ واللصق هذه باستخدام عدة RNAs صغيرة، من بينها U6 التي تُشكّل جزءًا من القلب الحفّاز للآلة. لا تعمل U6 بمفردها: تتعاون مع بروتينات و RNAs أخرى في عملية تجميع متدرجة. على طول الطريق، تُعدَّل U6 كيميائيًا في مواقع عديدة. يركز المؤلفون على منطقة حلقة داخلية من U6 تحمل عدة مجموعات مثيلة على السكر وتعديلًا خاصًا على قاعدة غوانين. أوضحت أعمال سابقة أن مثيلة القاعدة، المعروفة باسم N2-مثيلجوانينوزين في الموقع 72، ضرورية لقصّ مواقع ضعيفة وأن الإنزيم THUMPD2 يركّب هذه العلامة. وما ظل غير معلوم هو متى تُضاف هذه العلامة، وكيف يتعرف الإنزيم على U6، وكيف تؤثر هذه التغييرات الكيميائية على تجميع السبلايسوسوم والقصّ.
اللمسة النهائية تُضاف متأخرًا في عمر U6
باستخدام التقاطع الضوئي مع الربط والتسلسل عالي الإنتاجية، بيّن الباحثون أن THUMPD2 يرتبط بـU6 RNA أكثر بكثير من أي RNA آخر في الخلايا، مؤكّدين أن U6 هو الهدف الرئيسي له. من خلال تحليل نهايات الذيل لجزيئات U6 المرتبطة بـTHUMPD2، وجدوا أن الإنزيم يتعامل مع U6 فقط بعد أن تُعالج نهايته 3′ بالكامل، ما يعني أن المثيلة في الموضع 72 تُعد حدثًا متأخرًا في نضج U6. كشفت خريطة تفاعلات البروتين أن THUMPD2 يرتبط بمجمعات تحتوي U6 وعوامل قصّ مبكرة، لكنه لا يترافق مع عوامل التكوّن الأقدم جدًا. ثم وضعت المراصيف الفلورية THUMPD2 في أجسام كاجال—هياكل نووية فرعية حيث تحدث خطوات متأخرة من تجميع السبلايسوسوم—مما يدعم فكرة أن مثيلة الغوانين هي واحدة من علامات التحكم بالجودة النهائية قبل أن تنضم U6 إلى التجمعات السبلايسوسومية الأكبر.
تواصل بين تعديلات السكر والقاعدة
لفهم كيف يتعرف THUMPD2 على U6، جمع الفريق النمذجة الهيكلية، مطيافية الكتلة بعد التقاطع، والتحليل الطفري. بنوا نموذجًا تظهر فيه الحلقة الداخلية لـU6 وهي تستند إلى كل من نطاق ربط الـRNA من نوع THUMP والمجال الميثيلترانسفيرازي الحفّاز لـTHUMPD2، بحيث تقترب القاعدة المستهدفة من الموقع الفعّال للإنزيم. ثم أظهروا أن كلا المجالين مطلوبان للإمساك المستقر بـU6، بينما بروتين شريك صغير، TRMT112، ضروري للنشاط الحفّاز لـTHUMPD2. اللافت أنه في تجارب المثيلة في أنبوب الاختبار تبين أن THUMPD2 يكاد لا يغيّر حلقة U6 غير المعدلة لكنه يعمل بأكثر من عشرة أضعاف الكفاءة عندما تكون مجموعتان من سكريات الرايبوز المجاورة في الشريط المعاكس مثيلة عند موضعي 2′-O بالفعل. في الخلايا، أدى نضوب LARP7—عامل مطلوب لتركيب هذه المجموعات السكرية—إلى خفض كل من علامات السكر ومثيلة الغوانين. ومع ذلك، كانت قوة الارتباط بين THUMPD2 وU6 مشابهة بوجود أو بدون مثيلة السكر، مما يشير إلى أن هذه العلامات السابقة تضبط خطوة التفاعل نفسها وليس التعرف الابتدائي.
التأثير على أنماط القصّ وتجميع السبلايسوسوم
تساءل المؤلفون بعد ذلك كيف تؤثر هذه العلامات الكيميائية على القصّ الفعلي للجينات. بمقارنة بيانات تسلسل الـRNA للخلايا الخالية من THUMPD2، والخلايا التي نُقَص فيها LARP7، والخلايا التي تفتقد كلاهما، وجدوا أن كل تعديل يغيّر خيارات القصّ البديل بشكل طفيف لكن ملحوظ إحصائيًا. أدت خسارة مثيلة الغوانين وحدها بشكل رئيسي إلى زيادة احتباس الإنترونات، خصوصًا في الإنترونات التي تُقصّ بكفاءة منخفضة أصلًا. في المقابل، أدت خسارة مثيلات السكر إلى تحوّل استخدام مواقع القصّ 3′ البديلة باتجاه خيارات أبعد. عندما تعطلت كلا نوعي التعديل، كان عدد أحداث القصّ المتأثرة الأعلى، ويمكن تفسير التأثيرات المجمعة إلى حد كبير كمزيج إضافي من العيوب الفردية. كشفت التجزيئات الميكروبيولوجية للمستخرجات النووية عن عيوب التجميع الأساسية: بدون مثيلة القاعدة، تراكمت U6 في مجمعات وسطية من بروتينات وRNA صغيرة، مما يوحي بتباطؤ التقدّم إلى سبلايسوسومات مكتملة التكوين. بدون مثيلات السكر، دخلت كمية أقل بكثير من U6 إلى جسيمات RNP النووية الصغيرة أصلًا، وتوزعت مكوّنات سبلايسوسوم رئيسية بشكل غير سليم، مشيرة إلى مشكلة تجميع أكثر جوهرية.
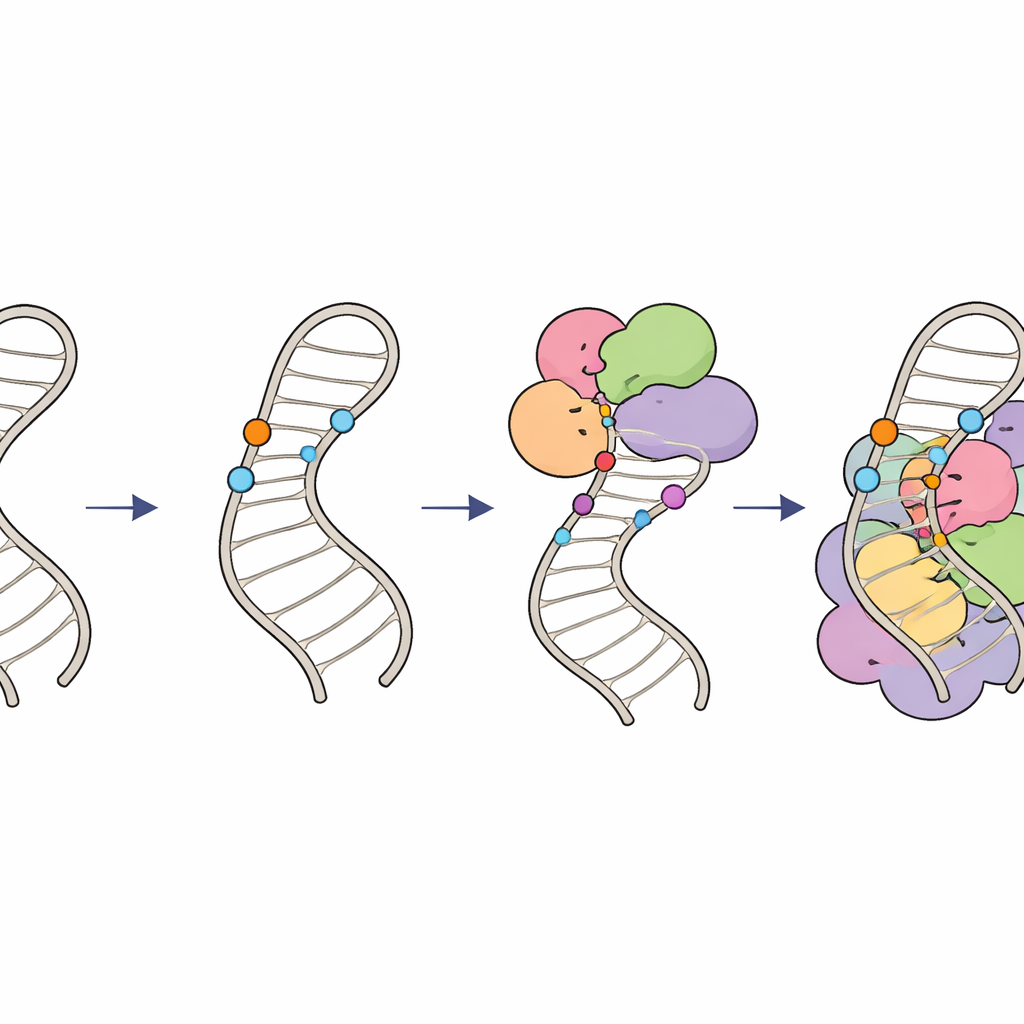
كيف تحافظ العلامات الكيميائية على مسار تحرير الـRNA
معًا، تحدد هذه النتائج "دائرة تعديل" هرمية على RNA U6. أولاً، توجه RNAs مرشدة متخصصة وعامل LARP7 مجموعات 2′-O-مثيلة إلى سكريات داخل الحلقة الداخلية، مما يشكل بنيتها ويخلق ركائز مثالية. ثم يضيف مركب الإنزيم THUMPD2–TRMT112 مجموعة مثيلة نهائية إلى قاعدة محددة، على الأرجح كتصريح مرحلي متأخر يسمح لـU6 بالتقدّم إلى مجمعات سبلايسوسوم أعلى ترتيبًا. من خلال تنسيق متى وأين تظهر هذه العلامات الكيميائية الصغيرة، تضمن الخلايا أن U6 مطوية بشكل صحيح ومُوصلَة إلى السبلايسوسوم بالتوقيت المناسب، محافظًة على قصّ RNA دقيق وفعال. يمكن أن تؤدي عيوب طفيفة في هذا النظام إلى تغيّر أنماط القصّ عبر الجينوم وقد تسهم في أمراض بشرية مرتبطة بأخطاء في القصّ.
الاستشهاد: Kleiber, N., Petrosyan, J., Greve, M. et al. 2′-O-methylation-dependent installation of N2-methylguanosine in the U6 internal stem loop facilitates efficient spliceosome assembly. Nat Commun 17, 3793 (2026). https://doi.org/10.1038/s41467-026-72355-2
الكلمات المفتاحية: قصّ الـRNA, حموضة نووية صغيرة U6, تعديلات الـRNA, تجميع السبلايسوسوم, THUMPD2