Clear Sky Science · de
2′-O‑Methylierungs‑abhängige Einführung von N2‑Methylguanosin in der U6‑internen Stem‑Loop fördert die effiziente Assemblierung des Spleißosoms
Warum winzige RNA‑Änderungen wichtig sind
In jeder menschlichen Zelle bearbeitet eine komplexe molekulare Maschine, das Spleißosom, unvollständige RNA‑Botschaften, damit sie in funktionelle Proteine übersetzt werden können. Diese Bearbeitung muss schnell und präzise erfolgen und beruht auf kleinen RNAs, die mit zahlreichen chemischen Markierungen feinabgestimmt sind. Diese Arbeit zeigt, wie eine spezifische Abfolge chemischer Modifikationen an einer solchen RNA, der U6, die korrekte Assemblierung des Spleißosoms unterstützt und insbesondere schwierige RNA‑Abschnitte handhabbar macht, mit möglichen Folgen für Krankheiten, bei denen das Spleißen gestört ist.
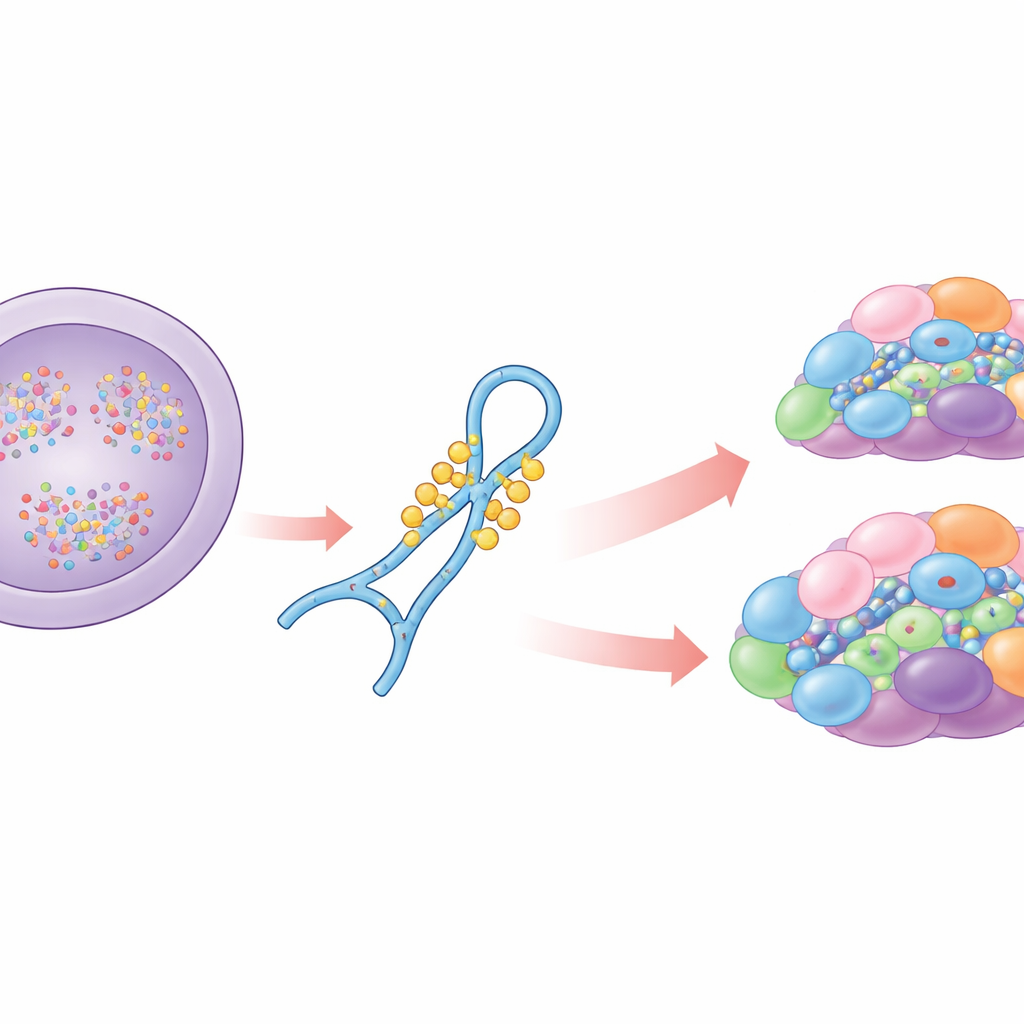
Ein zentraler Helfer bei der RNA‑Bearbeitung
Die meisten menschlichen Gene enthalten nichtkodierende Abschnitte, die vor der Proteinsynthese aus der RNA entfernt werden müssen. Das Spleißosom führt dieses Schneiden und Zusammenfügen mithilfe mehrerer kleiner RNAs aus, darunter U6, das Teil des katalytischen Kerns der Maschine ist. U6 arbeitet nicht allein: Es geht in einem schrittweisen Assemblierungsprozess Verbindungen mit Proteinen und anderen RNAs ein. Dabei wird U6 an vielen Positionen chemisch modifiziert. Die Autoren konzentrieren sich auf eine interne Loop‑Region von U6, die mehrere Zucker‑Methylgruppen und eine spezielle Modifikation an einer Guanosin‑Base trägt. Frühere Arbeiten zeigten, dass die Basenmethylierung, bekannt als N2‑Methylguanosin an Position 72, zum Spleißen schwacher Stellen erforderlich ist und dass das Enzym THUMPD2 diese Markierung anbringt. Unklar war jedoch, wann diese Markierung hinzugefügt wird, wie das Enzym U6 erkennt und wie diese chemischen Änderungen die Assemblierung des Spleißosoms und das Spleißen beeinflussen.
Der letzte Schliff, spät im Leben von U6
Mithilfe von UV‑Crosslinking und Hochdurchsatzsequenzierung zeigten die Forscher, dass THUMPD2 im Vergleich zu allen anderen RNAs in Zellen deutlich stärker an U6 bindet und bestätigten damit U6 als Hauptziel. Durch Analyse der 3′‑Enden von U6‑Molekülen, die mit THUMPD2 assoziiert waren, fanden sie heraus, dass das Enzym U6 erst nach vollständiger Verarbeitung seines 3′‑Endes erkennt — die Methylierung an Position 72 ist demnach ein spätes Ereignis in der U6‑Reifung. Protein‑Interaktionskartierungen zeigten, dass THUMPD2 mit U6‑enthaltenden Komplexen und frühen Spleißfaktoren assoziiert ist, jedoch nicht mit den allerersten Biogenesefaktoren. Fluoreszenzmikroskopie lokalisierte THUMPD2 in Cajal‑Körpern — nukleären Substrukturen, in denen späte Schritte der Spleißosomassemblierung stattfinden — und stützt die Idee, dass die Guanosin‑Methylierung eine der finalen Qualitätskontrollmarkierungen ist, bevor U6 in größere Spleißosomkomplexe eintritt.
Wechselwirkung zwischen Zucker‑ und Basenmodifikationen
Um zu verstehen, wie THUMPD2 U6 erkennt, kombinierten die Forscher Strukturmodellierung, Crosslinking‑Massenspektrometrie und Mutationsanalysen. Sie entwickelten ein Modell, in dem die interne Stem‑Loop von U6 an sowohl die THUMP‑RNA‑Bindedomäne als auch an die katalytische Methyltransferase‑Domäne von THUMPD2 anschmiegt und die Zielbase nahe der aktiven Stelle des Enzyms positioniert. Sie zeigten weiter, dass beide Domänen erforderlich sind, um U6 stabil zu halten, während ein kleines Partnerprotein, TRMT112, für die katalytische Aktivität von THUMPD2 unverzichtbar ist. Auffällig war, dass Reaktionen im Reagenzglas zeigten: THUMPD2 modifiziert eine unveränderte U6‑Loop kaum, arbeitet aber mehr als zehnmal effizienter, wenn zwei benachbarte Ribose‑Zucker in der gegenüberliegenden Strangseite bereits 2′‑O‑methylierte Gruppen tragen. In Zellen führte die Depletion von LARP7 — einem Faktor, der nötig ist, um diese Zucker‑Methylgruppen zu installieren — sowohl zu einem Rückgang der Zucker‑Markierungen als auch der Guanosin‑Methylierung. Die Bindungsstärke zwischen THUMPD2 und U6 blieb jedoch mit oder ohne Zucker‑Methylierung ähnlich, was darauf hindeutet, dass diese vorausgehenden Markierungen den eigentlichen Reaktionsschritt abstimmen und nicht die anfängliche Erkennung.
Auswirkungen auf Spleißmuster und Assemblierung des Spleißosoms
Die Autoren untersuchten anschließend, wie diese chemischen Markierungen das tatsächliche Genspleißen beeinflussen. Durch den Vergleich von RNA‑Sequenzierungsdaten aus Zellen ohne THUMPD2, Zellen mit LARP7‑Depletion und Zellen, denen beide fehlten, stellten sie fest, dass jede Störung die alternativen Spleißentscheidungen dezent, aber signifikant veränderte. Der Verlust der Guanosin‑Methylierung allein führte hauptsächlich zu verstärkter Intron‑Retention, besonders in Introns, die ohnehin ineffizient gespleißt werden. Im Gegensatz dazu verschob der Verlust der Zucker‑Methylierungen die Nutzung alternativer 3′‑Spleißstellen hin zu weiter entfernten Optionen. Wenn beide Modifikationstypen beeinträchtigt waren, war die Zahl der betroffenen Spleißereignisse am höchsten, und die kombinierten Effekte ließen sich weitgehend als additive Mischung der Einzeldefekte erklären. Biochemische Fraktionierung nukleärer Extrakte legte die zugrundeliegenden Assemblierungsdefekte offen: Ohne die Basenmethylierung reicherte sich U6 in intermediären kleinen RNA‑Protein‑Komplexen an, was auf eine verlangsamte Progression zu vollständig ausgebildeten Spleißosomen hindeutet. Ohne die Zucker‑Methylierungen gelang deutlich weniger U6 überhaupt in kleine nukleare Ribonukleoproteinpartikel, und wichtige Spleißosomkomponenten wurden fehlverteilt — Hinweis auf ein grundsätzlicheres Assemblierungsproblem.
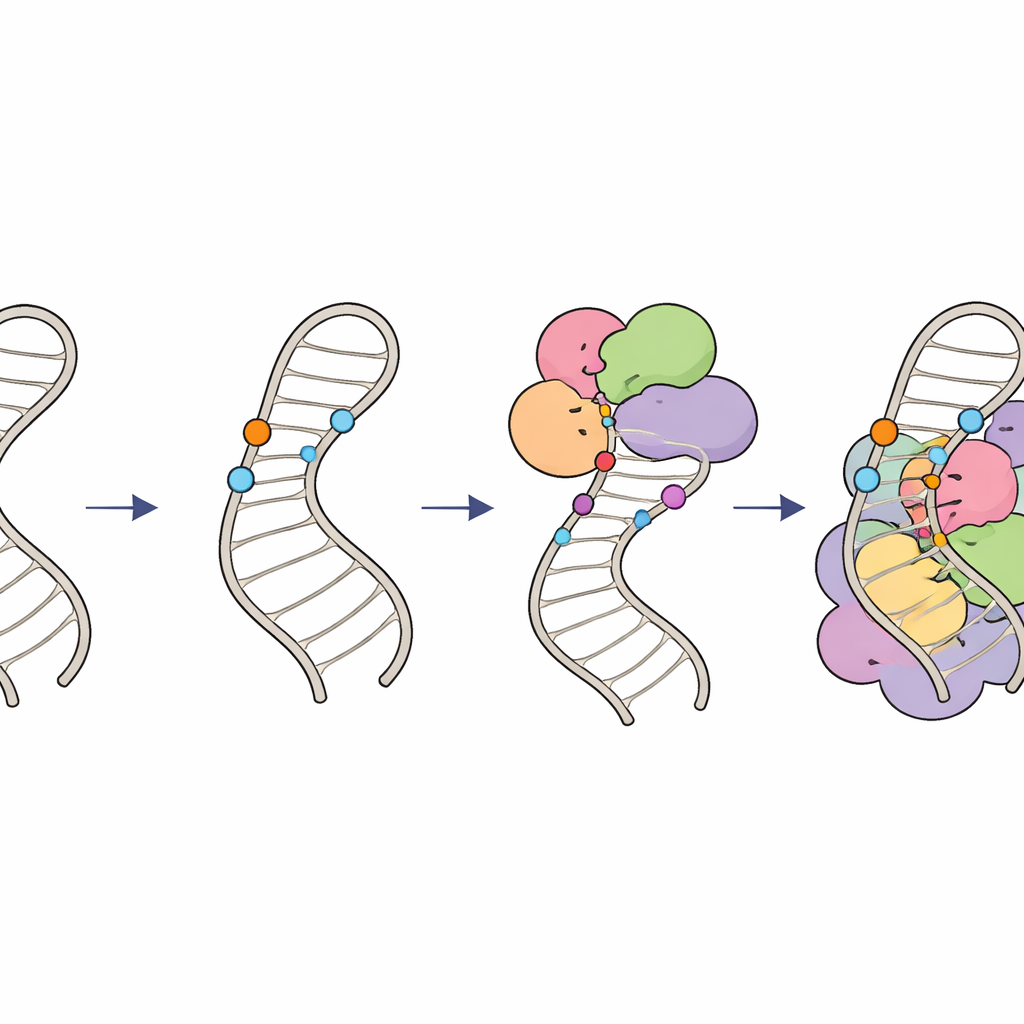
Wie chemische Markierungen das RNA‑Editing auf Kurs halten
Zusammen führen diese Befunde zu einem hierarchischen „Modifikations‑Circuit“ auf der U6‑RNA. Zunächst platzieren spezialisierte Guide‑RNAs und der Faktor LARP7 2′‑O‑Methylgruppen an Zuckern innerhalb der internen Stem‑Loop und formen so deren Struktur und schaffen ein optimales Substrat. Anschließend fügt der THUMPD2–TRMT112‑Enzymkomplex einer spezifischen Base eine abschließende Methylgruppe hinzu, wahrscheinlich als späte Lizenz, damit U6 in höhergeordnete Spleißosomkomplexe übergehen kann. Indem Zellen zeitlich und räumlich koordinieren, wann und wo diese winzigen chemischen Markierungen erscheinen, stellen sie sicher, dass U6 korrekt gefaltet ist und mit genau dem richtigen Timing ins Spleißosom integriert wird, wodurch präzises und effizientes RNA‑Spleißen erhalten bleibt. Subtile Fehler in diesem System können sich auf Spleißmuster im gesamten Genom auswirken und möglicherweise zu menschlichen Erkrankungen beitragen, die mit Spleißfehlern verbunden sind.
Zitation: Kleiber, N., Petrosyan, J., Greve, M. et al. 2′-O-methylation-dependent installation of N2-methylguanosine in the U6 internal stem loop facilitates efficient spliceosome assembly. Nat Commun 17, 3793 (2026). https://doi.org/10.1038/s41467-026-72355-2
Schlüsselwörter: RNA‑Spleißen, U6 snRNA, RNA‑Modifikationen, Assemblierung des Spleißosoms, THUMPD2