Clear Sky Science · nl
2′-O-methylering-afhankelijke aanbrenging van N2-methylguanosine in de U6 interne stamlus bevordert efficiënte spliceosoomassemblage
Waarom kleine RNA-aanpassingen ertoe doen
In elke menselijke cel bewerkt een ingewikkelde moleculaire machine, het spliceosoom, onbewerkte RNA-berichten zodat ze in werkzame eiwitten kunnen worden omgezet. Deze bewerking moet zowel snel als nauwkeurig verlopen en is afhankelijk van kleine RNA’s die sterk zijn "afgestemd" met chemische labels. Dit artikel onthult hoe een specifieke reeks chemische aanpassingen op een van die RNA’s, U6 genaamd, helpt dat het spliceosoom correct assembleert en bijzonder lastige RNA-segmenten verwerkt, met mogelijke implicaties voor ziekten waarin splicing misgaat.
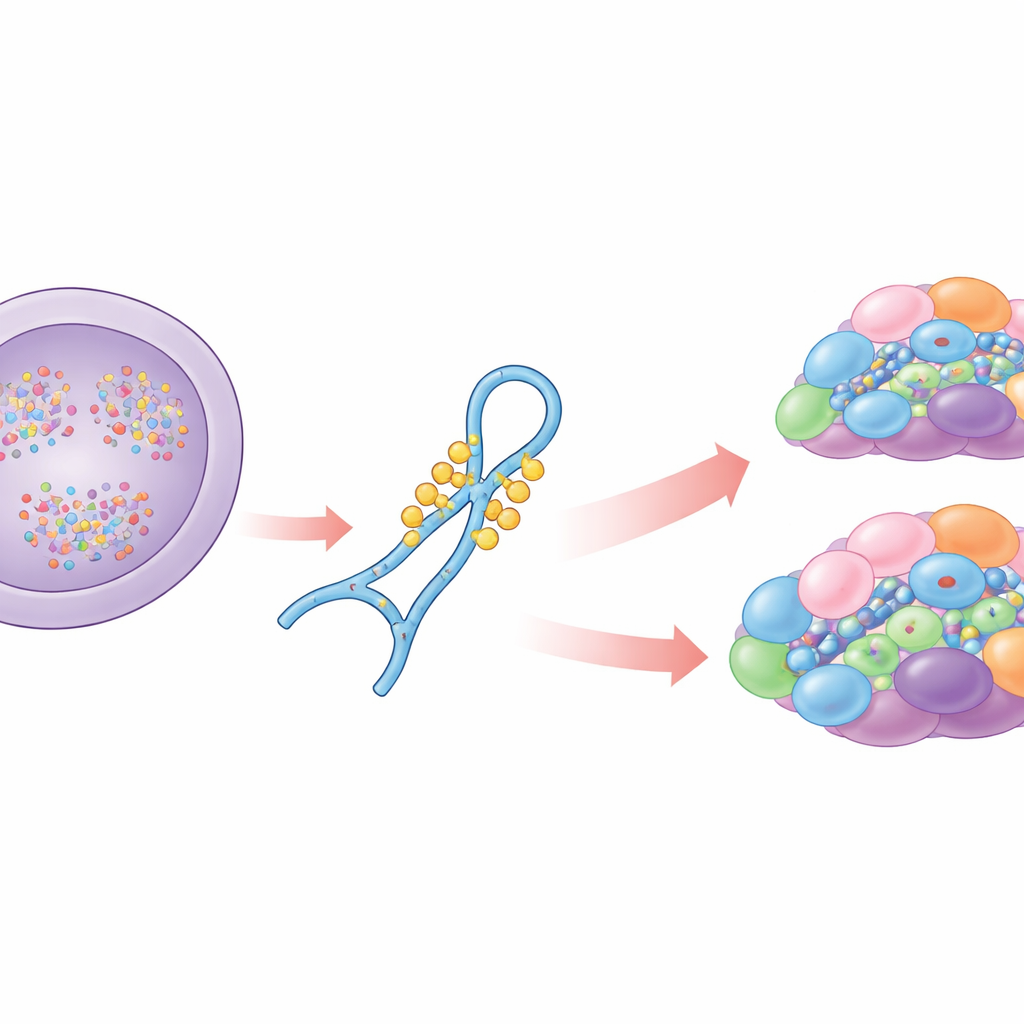
Een belangrijke helper bij RNA-bewerking
De meeste menselijke genen bevatten niet-coderende stukken die uit het RNA moeten worden verwijderd voordat eiwitten worden gemaakt. Het spliceosoom voert dit knip-en-plakwerk uit met behulp van meerdere kleine RNA’s, waaronder U6, dat onderdeel vormt van het catalytische hart van het complex. U6 werkt niet alleen: het werkt samen met eiwitten en andere RNA’s in een stapsgewijs assemblageproces. Onderweg wordt U6 op veel plaatsen chemisch gemodificeerd. De auteurs richten zich op een interne lusregio van U6 die meerdere suikermethyleren draagt en een speciale wijziging op één guanosine-base. Eerder werk toonde aan dat die basemethylering, bekend als N2-methylguanosine op positie 72, nodig is om zwakke sites te splitsen en dat het enzym THUMPD2 deze markering aanbrengt. Wat onbekend bleef, was wanneer deze markering wordt toegevoegd, hoe het enzym U6 herkent en hoe deze chemische veranderingen de assemblage van het spliceosoom en de splicing beïnvloeden.
Laatste afwerking toegevoegd laat in U6’s levenscyclus
Met UV-crosslinking en high-throughput sequencing toonden de onderzoekers aan dat THUMPD2 veel sterker aan U6-RNA bindt dan aan welk ander RNA dan ook in cellen, waarmee U6 als het primaire doelwit wordt bevestigd. Door de staarten van U6-moleculen die aan THUMPD2 waren gebonden te analyseren, vonden ze dat het enzym U6 pas benadert nadat het 3′-einde volledig is verwerkt, wat betekent dat methylering op positie 72 een laat stadium in de rijping van U6 is. Kaartlegging van eiwitinteracties liet zien dat THUMPD2 geassocieerd is met U6-bevattende complexen en vroege splicingfactoren, maar niet met de allervroegste biogenesefactoren. Fluorescentiemicroscopie plaatste THUMPD2 vervolgens in Cajal-lichamen — nucleaire substructuren waar late stappen van spliceosoomassemblage plaatsvinden — wat de gedachte ondersteunt dat de guanosinemethylering een van de laatste kwaliteitscontrolemerken is voordat U6 zich aansluit bij grotere spliceosomale assemblages.
Onderlinge beïnvloeding tussen suiker- en basismodificaties
Om te begrijpen hoe THUMPD2 U6 herkent, combineerde het team structurele modellering, crosslinking massaspectrometrie en mutatieanalyse. Ze bouwden een model waarin de interne stamlus van U6 zich nestelt tegen zowel het THUMP RNA-bindingsdomein als het catalytische methyltransferasedomein van THUMPD2, waardoor de doeldoos dicht bij het actieve centrum van het enzym ligt. Ze toonden vervolgens aan dat beide domeinen nodig zijn om U6 stevig vast te houden, terwijl een kleine partnerproteïne, TRMT112, essentieel is voor de katalytische activiteit van THUMPD2. Opvallend was dat testbuis-methyleringsassays lieten zien dat THUMPD2 nauwelijks een ongewijzigde U6-lus modificeert, maar meer dan tien keer efficiënter werkt wanneer twee nabijgelegen riboses aan de tegenoverliggende streng al 2′-O-gemethyleerd zijn. In cellen leidde het uitputten van LARP7 — een factor die nodig is om deze suikermethyleren aan te brengen — tot vermindering van zowel de suikerlabels als de guanosinemethylering. Toch was de bindingssterkte tussen THUMPD2 en U6 vergelijkbaar met of zonder suikermethylering, wat aangeeft dat deze voorafgaande merken de reactiesnelheid zelf bijsturen, niet de initiële herkenning.
Effect op splicepatronen en spliceosoomassemblage
De auteurs onderzochten vervolgens hoe deze chemische merken de daadwerkelijke gen-splicing beïnvloeden. Door RNA-sequencinggegevens te vergelijken van cellen zonder THUMPD2, cellen met uitputting van LARP7 en cellen die beide misten, vonden ze dat elke verstoring subtiel maar significant alternatieve splicingkeuzes veranderde. Verlies van alleen de guanosinemethylering leidde voornamelijk tot verhoogde intronretentie, vooral in introns die al inefficiënt werden gesplitst. Verlies van de suikermethyleren verschoof daarentegen het gebruik van alternatieve 3′-splicesites naar verder gelegen opties. Wanneer beide typen modificatie werden aangetast, was het aantal getroffen splicinggebeurtenissen het grootst, en de gecombineerde effecten konden grotendeels worden verklaard als een optelsom van de afzonderlijke defecten. Biochemische fractionatie van nucleaire extracten onthulde de onderliggende assemblagefouten: zonder de basemethylering stapelde U6 zich op in intermediaire kleine RNA–eiwitcomplexen, wat wijst op vertraagde voortgang naar volledig gevormde spliceosomen. Zonder de suikermethyleren kwam veel minder U6 überhaupt in kleine nucleaire ribonucleoproteïne-deeltjes terecht, en sleutelcomponenten van het spliceosoom waren misverdeeld, wat wijst op een fundamenteler assemblageprobleem.
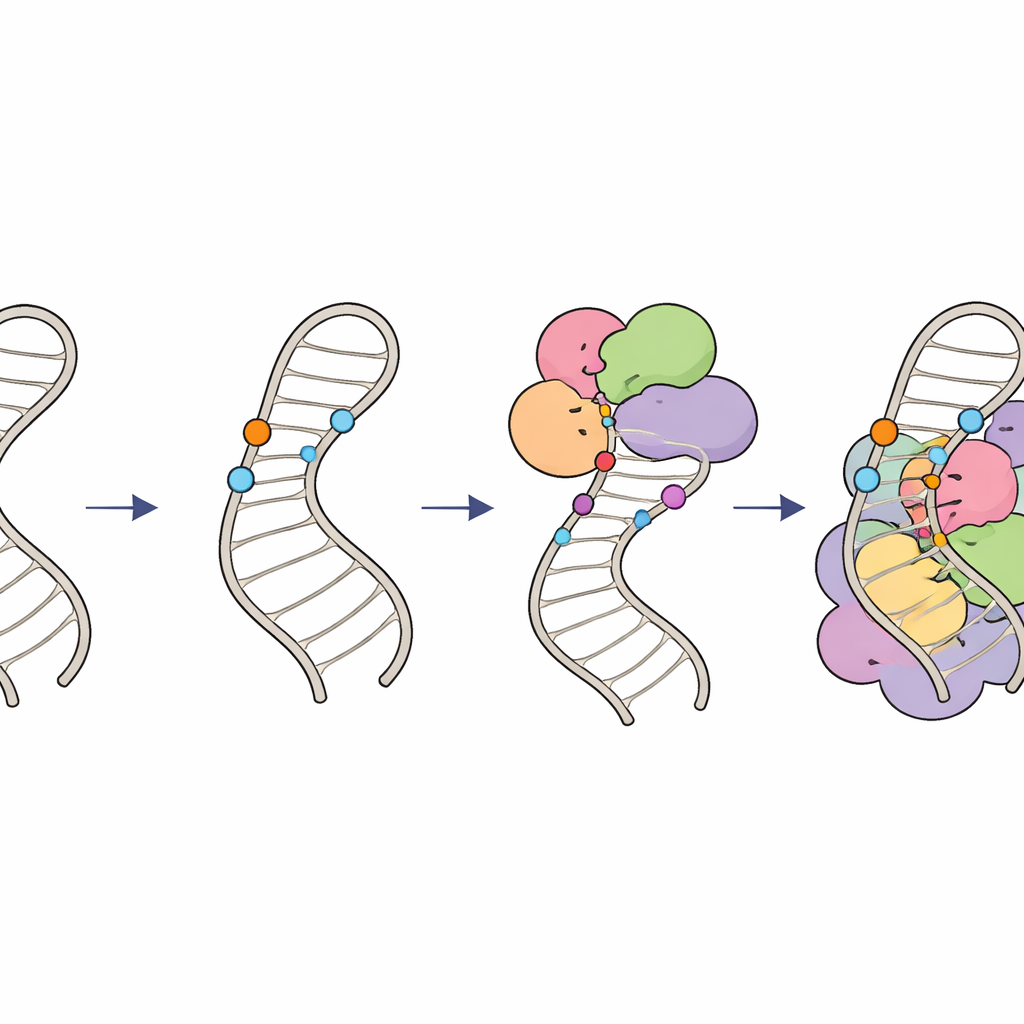
Hoe chemische merken RNA-bewerking op koers houden
Samen schetsen deze bevindingen een hiërarchische "modificatiecircuits" op U6-RNA. Eerst plaatsen gespecialiseerde gids-RNA’s en de factor LARP7 2′-O-methylgroepen op suikers binnen de interne stamlus, waarmee de structuur wordt gevormd en een optimaal substraat ontstaat. Daarna brengt het THUMPD2–TRMT112-enzymcomplex een afrondende methylgroep aan op een specifieke base, waarschijnlijk als een laat stadium-licentie voor U6 om door te stromen naar hogere orde spliceosomale complexen. Door te coördineren wanneer en waar deze kleine chemische merken verschijnen, zorgen cellen ervoor dat U6 correct gevouwen is en op het juiste moment in het spliceosoom wordt ingeplugd, waardoor nauwkeurige en efficiënte RNA-splicing wordt gehandhaafd. Subtiele defecten in dit systeem kunnen doorwerken en splicepatronen in het hele genoom veranderen en kunnen bijdragen aan menselijke ziekten die verband houden met splicingfouten.
Bronvermelding: Kleiber, N., Petrosyan, J., Greve, M. et al. 2′-O-methylation-dependent installation of N2-methylguanosine in the U6 internal stem loop facilitates efficient spliceosome assembly. Nat Commun 17, 3793 (2026). https://doi.org/10.1038/s41467-026-72355-2
Trefwoorden: RNA-splitsing, U6 snRNA, RNA-bewerkingen, spliceosoomassemblage, THUMPD2