Clear Sky Science · it
Installazione dipendente da 2′-O-metilazione della N2-metilguanosina nell'anello interno U6 facilita l'assemblaggio efficiente dello spliceosoma
Perché piccole modifiche all'RNA contano
All'interno di ogni cellula umana, una complessa macchina molecolare chiamata spliceosoma modifica i messaggi RNA grezzi affinché possano essere tradotti in proteine funzionanti. Queste modifiche devono essere rapide e accurate e si basano su piccoli RNA che sono fortemente "rifiniti" con marche chimiche. Questo studio rivela come una specifica sequenza di modifiche chimiche su uno di questi RNA, chiamato U6, aiuti lo spliceosoma ad assemblarsi correttamente e a gestire segmenti di RNA particolarmente difficili, con possibili implicazioni per malattie in cui lo splicing è compromesso.
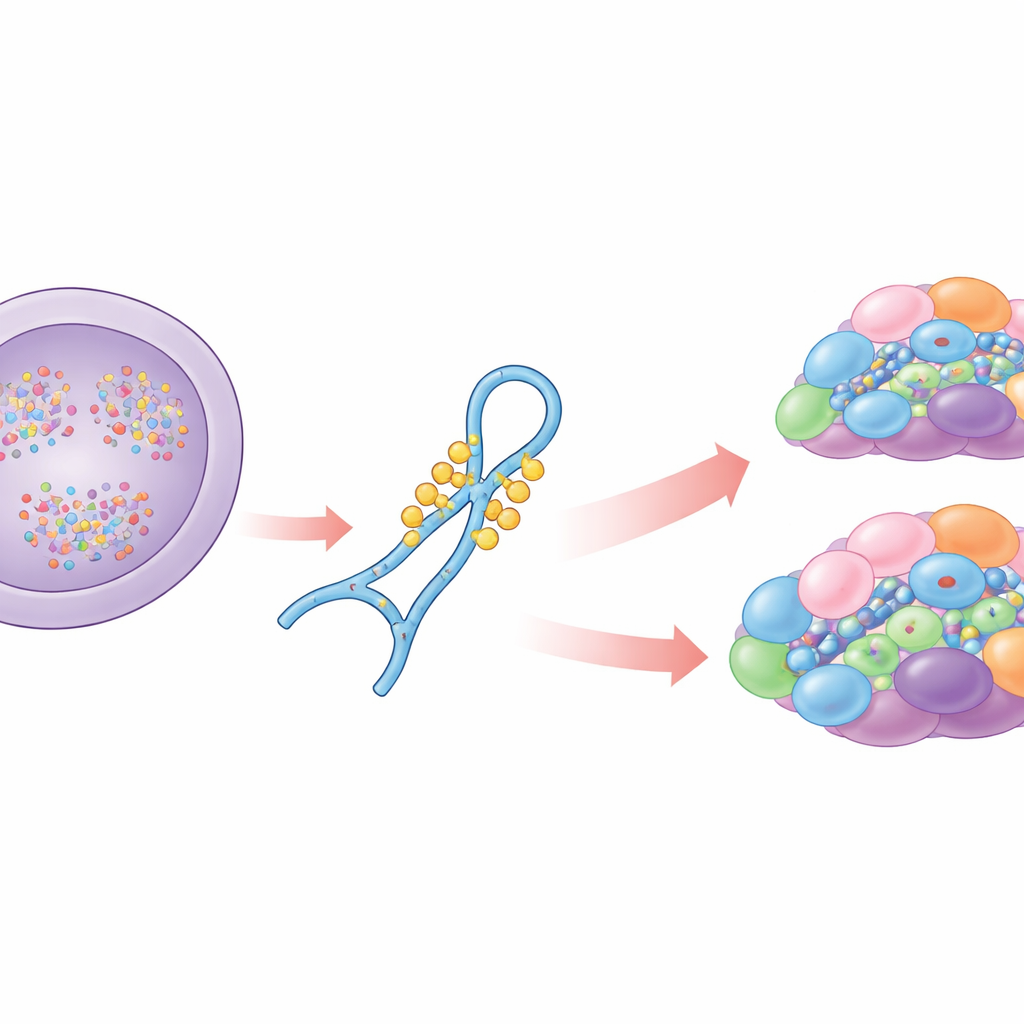
Un aiutante chiave nell'editing dell'RNA
La maggior parte dei geni umani contiene tratti non codificanti che devono essere rimossi dall'RNA prima della sintesi proteica. Lo spliceosoma effettua questo taglio e cucito usando diversi piccoli RNA, tra cui U6, che fa parte del cuore catalitico della macchina. U6 non agisce da solo: collabora con proteine e altri RNA in un processo di assemblaggio graduale. Lungo questo percorso, U6 viene chimicamente modificato in molte posizioni. Gli autori si concentrano su una regione ad anello interno di U6 che porta diversi gruppi metile sullo zucchero e una modifica speciale su una base guanosina. Lavori precedenti avevano mostrato che la metilazione della base, nota come N2‑metilguanosina alla posizione 72, è necessaria per splicare siti deboli e che l'enzima THUMPD2 installa questo marchio. Ciò che rimaneva sconosciuto era quando questo marchio viene aggiunto, come l'enzima riconosce U6 e in che modo questi cambiamenti chimici influenzano l'assemblaggio dello spliceosoma e lo splicing.
Tocco finale aggiunto nella fase finale della vita di U6
Usando crosslinking UV e sequenziamento ad alto rendimento, i ricercatori hanno dimostrato che THUMPD2 si lega all'RNA U6 molto più che a qualsiasi altro RNA nelle cellule, confermando U6 come suo principale bersaglio. Analizzando le estremità 3′ delle molecole di U6 associate a THUMPD2, hanno scoperto che l'enzima interagisce con U6 solo dopo che la sua estremità 3′ è stata completamente processata, il che significa che la metilazione alla posizione 72 è un evento tardivo nella maturazione di U6. La mappatura delle interazioni proteiche ha rivelato che THUMPD2 si associa a complessi contenenti U6 e a fattori di splicing precoci, ma non ai primissimi fattori di biogenesi. La microscopia a fluorescenza ha poi localizzato THUMPD2 nei corpi di Cajal—sottostrutture nucleari dove avvengono gli stadi finali dell'assemblaggio dello spliceosoma—sostenendo l'idea che la metilazione della guanosina sia uno dei marchi di controllo qualità finali prima che U6 si unisca a complessi spliceosomiali più grandi.
Crosstalk tra modifiche sullo zucchero e sulla base
Per capire come THUMPD2 riconosce U6, il gruppo ha combinato modellizzazione strutturale, spettrometria di massa con crosslinking e analisi mutazionale. Hanno costruito un modello in cui l'anello interno di U6 si appoggia sia al dominio di legame all'RNA THUMP sia al dominio metiltransferasico catalitico di THUMPD2, posizionando la base bersaglio vicino al sito attivo dell'enzima. Hanno quindi dimostrato che entrambi i domini sono necessari per ancorare stabilmente U6, mentre una piccola proteina partner, TRMT112, è essenziale per l'attività catalitica di THUMPD2. Sorprendentemente, saggi di metilazione in vitro hanno rivelato che THUMPD2 modifica a malapena un anello U6 non modificato, ma opera più di dieci volte più efficacemente quando due ribosio vicini nel filamento opposto sono già 2′‑O‑metilati. Nelle cellule, l'esaurimento di LARP7—un fattore necessario per installare questi gruppi metile sugli zuccheri—ha ridotto sia i marchi sullo zucchero sia la metilazione sulla guanosina. Tuttavia, la forza di legame tra THUMPD2 e U6 era simile con o senza metilazione dello zucchero, indicando che questi marchi precedenti modulano il passo reattivo stesso, non il riconoscimento iniziale.
Impatto sui modelli di splicing e sull'assemblaggio dello spliceosoma
Gli autori hanno poi esaminato come questi marchi chimici influenzano lo splicing genico reale. Confrontando dati di RNA‑sequencing da cellule prive di THUMPD2, cellule deplete di LARP7 e cellule mancanti di entrambi, hanno trovato che ciascuna perturbazione alterava in modo sottile ma significativo le scelte di splicing alternativo. La perdita della sola metilazione della guanosina portava principalmente a un aumento della ritenzione degli introni, in particolare in introni che sono già inefficientemente splicati. Al contrario, la perdita delle metilazioni sullo zucchero spostava l'uso di siti di splicing 3′ alternativi verso opzioni più lontane. Quando entrambi i tipi di modifica erano compromessi, il numero di eventi di splicing interessati era massimo, e gli effetti combinati potevano essere in gran parte spiegati come una somma degli difetti individuali. La frazionamento biochimico degli estratti nucleari ha rivelato i difetti di assemblaggio sottostanti: senza la metilazione della base, U6 si accumulava in complessi intermedi ribonucleoproteici, suggerendo un rallentamento nella progressione verso spliceosomi completamente formati. Senza le metilazioni sullo zucchero, molto meno U6 entrava affatto nei piccoli ribonucleoproteine nucleari e componenti chiave dello spliceosoma risultavano mal distribuiti, indicando un problema di assemblaggio più fondamentale.
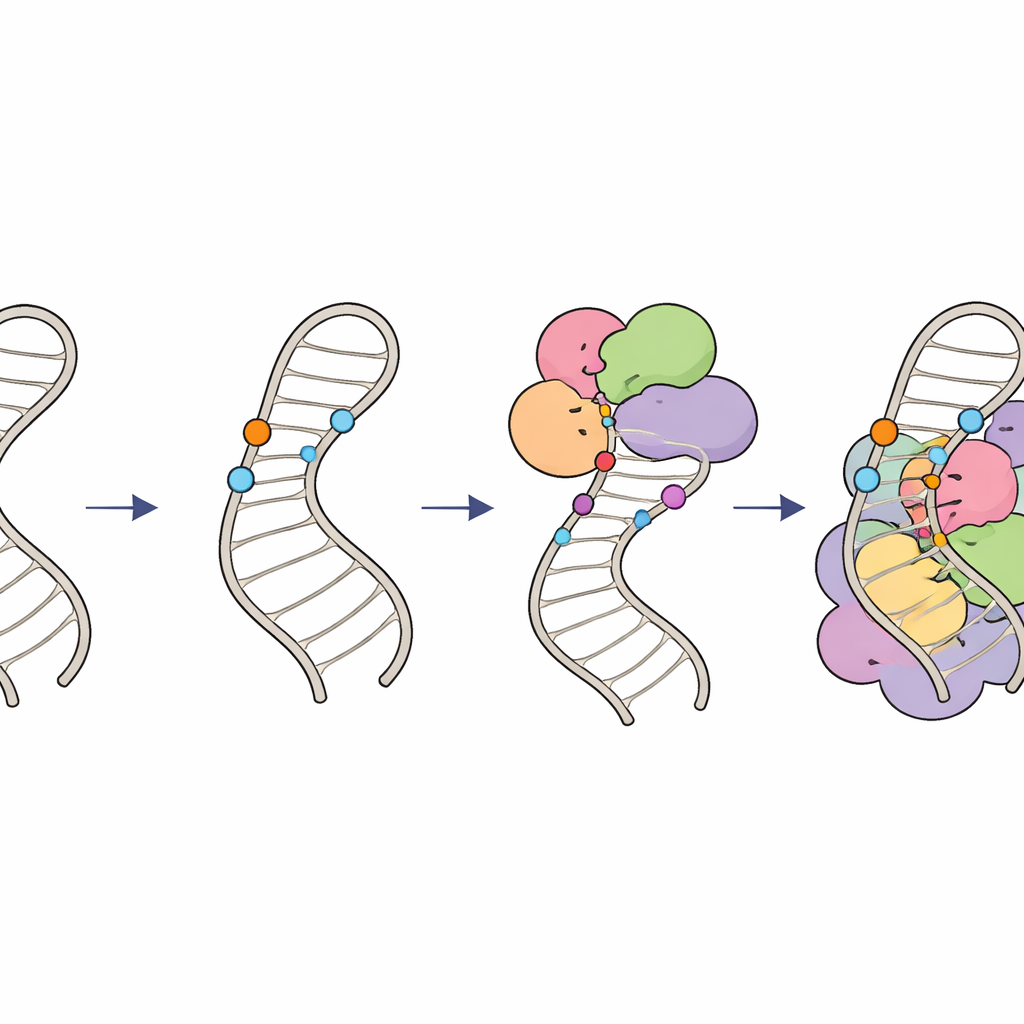
Come i marchi chimici mantengono lo splicing sulla giusta traiettoria
Nel complesso, questi risultati delineano un "circuito di modificazione" gerarchico sull'RNA U6. Prima, RNA guida specializzati e il fattore LARP7 posizionano gruppi 2′‑O‑metile sugli zuccheri all'interno dell'anello interno, plasmando la sua struttura e creando un substrato ottimale. Poi, il complesso enzimatico THUMPD2–TRMT112 aggiunge un gruppo metile finale a una base specifica, agendo probabilmente come una licenza di late stage perché U6 progredisca verso complessi spliceosomiali di ordine superiore. Coordinando quando e dove compaiono questi piccoli marchi chimici, le cellule garantiscono che U6 si pieghi correttamente e si integri nello spliceosoma con il giusto tempismo, mantenendo uno splicing dell'RNA accurato ed efficiente. Difetti sottili in questo sistema possono riverberare modificando i modelli di splicing nel genoma e potrebbero contribuire a malattie umane legate ad errori di splicing.
Citazione: Kleiber, N., Petrosyan, J., Greve, M. et al. 2′-O-methylation-dependent installation of N2-methylguanosine in the U6 internal stem loop facilitates efficient spliceosome assembly. Nat Commun 17, 3793 (2026). https://doi.org/10.1038/s41467-026-72355-2
Parole chiave: Splicing dell'RNA, snRNA U6, Modifiche dell'RNA, Assemblaggio dello spliceosoma, THUMPD2