Clear Sky Science · pl
Instalacja N2‑metyloguanozyny w pętli wewnętrznej U6 zależna od 2′‑O‑metylacji ułatwia efektywny montaż spliceosomu
Dlaczego drobne korekty RNA mają znaczenie
W każdej komórce człowieka skomplikowana maszyna molekularna zwana spliceosomem edytuje surowe komunikaty RNA, aby mogły zostać przetłumaczone na funkcjonalne białka. Ta edycja musi być szybka i dokładna, a opiera się na małych RNA, które są intensywnie „dostrajane” przy pomocy chemicznych znaków. W artykule tym opisano, jak określona sekwencja chemicznych modyfikacji na jednym z takich RNA, zwanym U6, pomaga spliceosomowi składać się poprawnie i radzić sobie ze szczególnie trudnymi fragmentami RNA — co może mieć znaczenie dla chorób związanych z zaburzeniami splicingu.
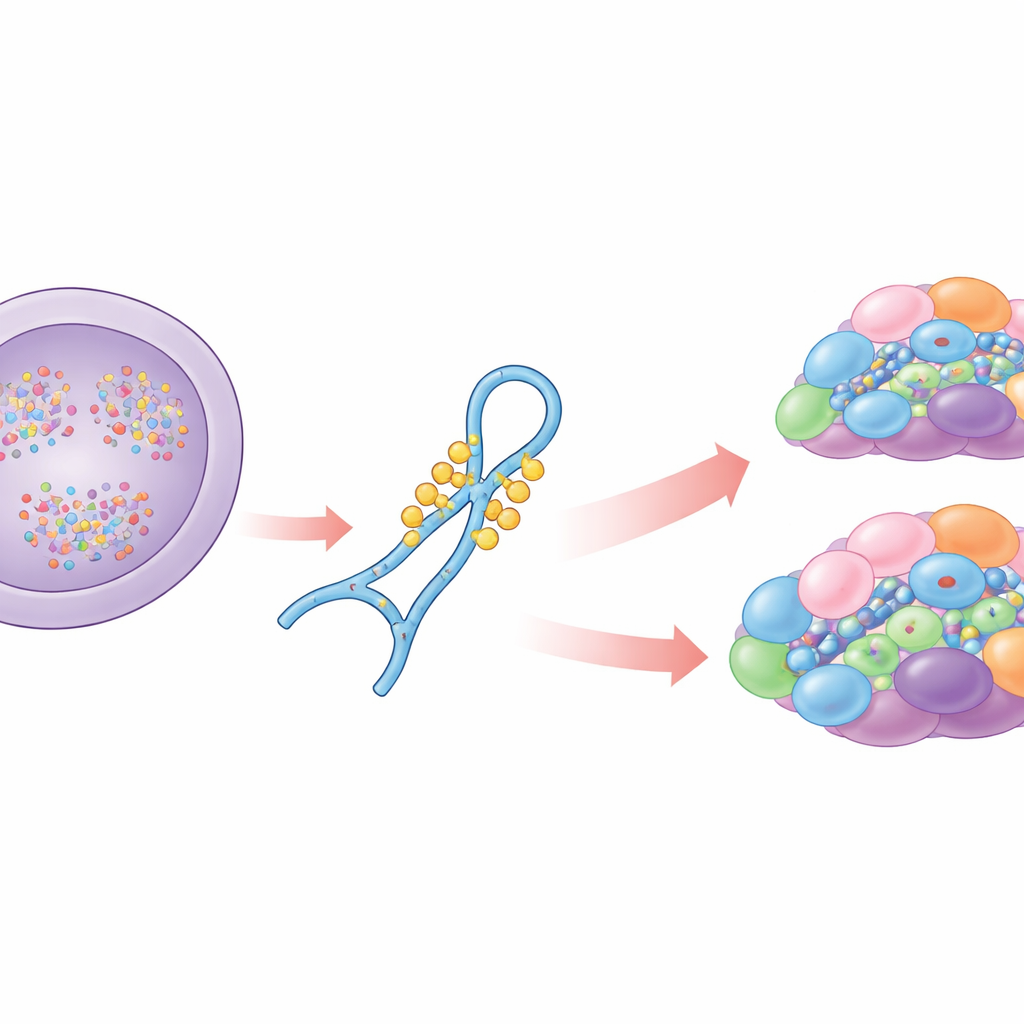
Kluczowy pomocnik w edycji RNA
Większość ludzkich genów zawiera sekwencje niekodujące, które muszą zostać usunięte z RNA zanim powstaną białka. Spliceosom wykonuje to cięcie i sklejanie przy udziale kilku małych RNA, w tym U6, które wchodzi w skład katalitycznego centrum maszyny. U6 nie działa samodzielnie: współdziała z białkami i innymi RNA w wieloetapowym procesie składania. W trakcie tego procesu U6 jest chemicznie modyfikowany w wielu miejscach. Autorzy skupili się na regionie z pętlą wewnętrzną U6, który nosi kilka 2′‑O‑metylacji cukrowych oraz specyficzną modyfikację jednej zasady guaninowej. Wcześniejsze prace wykazały, że metylacja zasady, znana jako N2‑metyloguanozyna na pozycji 72, jest potrzebna do splicingu słabych miejsc oraz że enzym THUMPD2 wprowadza tę modyfikację. Wciąż nie było jednak jasne, kiedy ten znak jest dodawany, jak enzym rozpoznaje U6 i jak te chemiczne zmiany wpływają na składanie spliceosomu i splicing.
Wykończenie dodawane późno w życiu U6
Za pomocą UV‑powiązań i wysokoprzepustowego sekwencjonowania badacze pokazali, że THUMPD2 wiąże się z RNA U6 znacznie silniej niż z innymi RNA w komórkach, potwierdzając U6 jako jego główny cel. Analiza końców 3′ cząsteczek U6 związanych z THUMPD2 wykazała, że enzym angażuje U6 dopiero po pełnym przetworzeniu końca 3′, co oznacza, że metylacja na pozycji 72 jest zdarzeniem późnym w maturacji U6. Mapowanie interakcji białkowych ujawniło, że THUMPD2 łączy się z kompleksami zawierającymi U6 i z wczesnymi czynnikami splicingu, ale nie z najwcześniejszymi czynnikami biogenezy. Mikroskopia fluorescencyjna umiejscowiła następnie THUMPD2 w ciałkach Cajala — podstrukturach jądrowych, gdzie zachodzą późne etapy składania spliceosomu — co wspiera koncepcję, że metylacja guaniny jest jednym z końcowych znaków kontroli jakości przed dołączeniem U6 do większych zespołów spliceosomalnych.
Przekaz między modyfikacjami cukru a zasad
Aby zrozumieć, jak THUMPD2 rozpoznaje U6, zespół połączył modelowanie strukturalne, krzyżujące się spektrometrię mas i analizę mutacyjną. Zbudowali model, w którym pętla wewnętrzna U6 przylega zarówno do domeny wiążącej RNA typu THUMP, jak i do katalitycznej domeny metylotransferazy THUMPD2, umieszczając docelową zasadę blisko miejsca aktywnego enzymu. Pokazali następnie, że obie domeny są niezbędne do stabilnego uchwycenia U6, podczas gdy mały partner białkowy TRMT112 jest konieczny dla aktywności katalitycznej THUMPD2. Co uderzające, testy metylacji in vitro wykazały, że THUMPD2 słabo modyfikuje niemodyfikowaną pętlę U6, ale pracuje ponad dziesięciokrotnie wydajniej, gdy dwa pobliskie cukry w naprzeciwnej nici są już 2′‑O‑metylowane. W komórkach zubożenie LARP7 — czynnika potrzebnego do wstawienia tych metylacji cukrowych — zmniejszyło zarówno znaki cukrowe, jak i metylację guaniny. Jednak siła wiązania między THUMPD2 a U6 była podobna niezależnie od obecności metylacji cukrowej, co wskazuje, że te wcześniejsze modyfikacje dostrajają sam etap reakcji, a nie początkowe rozpoznanie.
Wpływ na wzorce splicingu i montaż spliceosomu
Autorzy zapytali następnie, jak te chemiczne znaki wpływają na rzeczywisty splicing genów. Porównując dane z sekwencjonowania RNA z komórek pozbawionych THUMPD2, z komórek zubożonych w LARP7 oraz z komórek pozbawionych obu czynników, odkryli, że każda z tych perturbacji subtelnie, ale istotnie zmienia wybory alternatywnego splicingu. Utrata metylacji guaniny sama w sobie prowadziła głównie do zwiększonego zatrzymywania intronów, szczególnie w intronach już i tak słabo splicedowanych. Natomiast utrata metylacji cukrowych przesunęła użycie alternatywnych 3′ miejsc splicingu w kierunku dalszych opcji. Gdy oba typy modyfikacji były upośledzone, liczba dotkniętych zdarzeń splicingu była największa, a połączone efekty dały się w dużej mierze wyjaśnić jako addytywne zsumowanie pojedynczych defektów. Frakcjonowanie biochemiczne ekstraktów jądrowych ujawniło leżące u ich podstaw defekty montażowe: bez metylacji zasady U6 gromadziło się w pośrednich kompleksach RNA–białko, sugerując spowolnione przejście do w pełni ukształtowanych spliceosomów. Bez metylacji cukrowych znacznie mniej U6 trafiało w ogóle do cząsteczek snRNP, a kluczowe składniki spliceosomu były błędnie zdystrybuowane, co wskazuje na bardziej podstawowy problem montażowy.
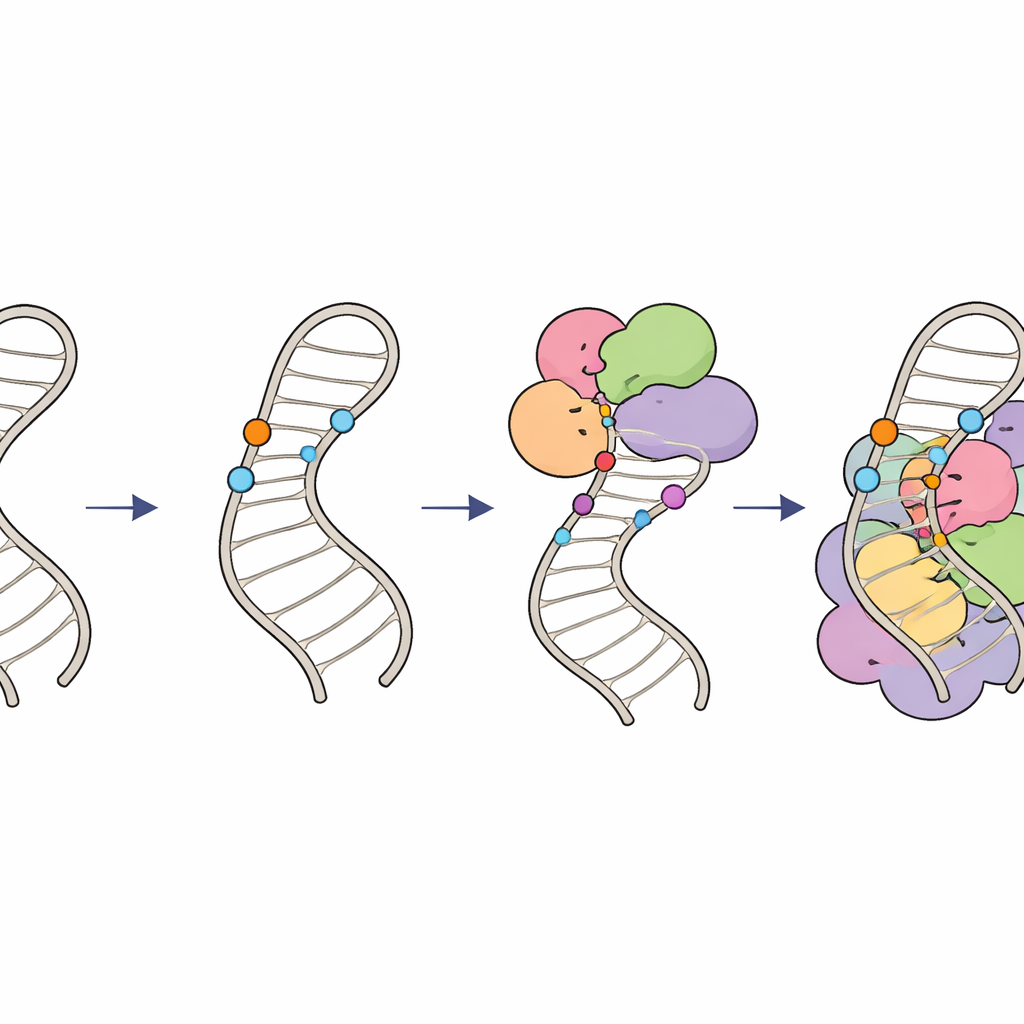
Jak chemiczne znaki utrzymują edycję RNA na właściwym torze
Razem te wyniki szkicują hierarchiczny „obwód modyfikacji” na RNA U6. Najpierw wyspecjalizowane przewodnikowe RNA i czynnik LARP7 umieszczają grupy 2′‑O‑metylowe na cukrach w obrębie pętli wewnętrznej, kształtując jej strukturę i tworząc optymalne podłoże. Następnie kompleks enzymatyczny THUMPD2–TRMT112 dodaje wykończeniową grupę metylową do specyficznej zasady, prawdopodobnie działając jako późnoetapowa licencja pozwalająca U6 przejść do wyższych zespołów spliceosomalnych. Koordynując, kiedy i gdzie pojawiają się te drobne chemiczne znaki, komórki zapewniają, że U6 jest poprawnie złożone i włączone do spliceosomu we właściwym momencie, utrzymując dokładny i wydajny splicing RNA. Subtelne defekty w tym systemie mogą rozlać się na zmianę wzorców splicingu w całym genomie i przyczyniać się do chorób ludzkich związanych z błędami splicingu.
Cytowanie: Kleiber, N., Petrosyan, J., Greve, M. et al. 2′-O-methylation-dependent installation of N2-methylguanosine in the U6 internal stem loop facilitates efficient spliceosome assembly. Nat Commun 17, 3793 (2026). https://doi.org/10.1038/s41467-026-72355-2
Słowa kluczowe: Splicing RNA, snRNA U6, Modyfikacje RNA, Montaż spliceosomu, THUMPD2