Clear Sky Science · sv
Sexspecifikt KDM6A-HNF4A-CREBH-nätverk styr lipoproteincholesterolmetabolism och ateroskleros via epigenetisk omprogrammering av hepatocyter
Varför denna forskning är viktig för hjärthälsan
Hjärtattacker och stroke börjar ofta med långsamma förändringar i hur levern hanterar kolesterol. Män och kvinnor skiljer sig i sina kolesterolnivåer och risken för tilltäppta artärer, men de bakomliggande orsakerna är fortfarande under utredning. Denna studie avslöjar ett könsbundet kontrollsystem i leverceller som hjälper till att hålla blodfetter i ett hälsosammare intervall, särskilt hos kvinnor. Att förstå detta system kan peka mot mer personanpassade behandlingar för högt kolesterol och ateroskleros.
En leverbrytare på X-kromosomen
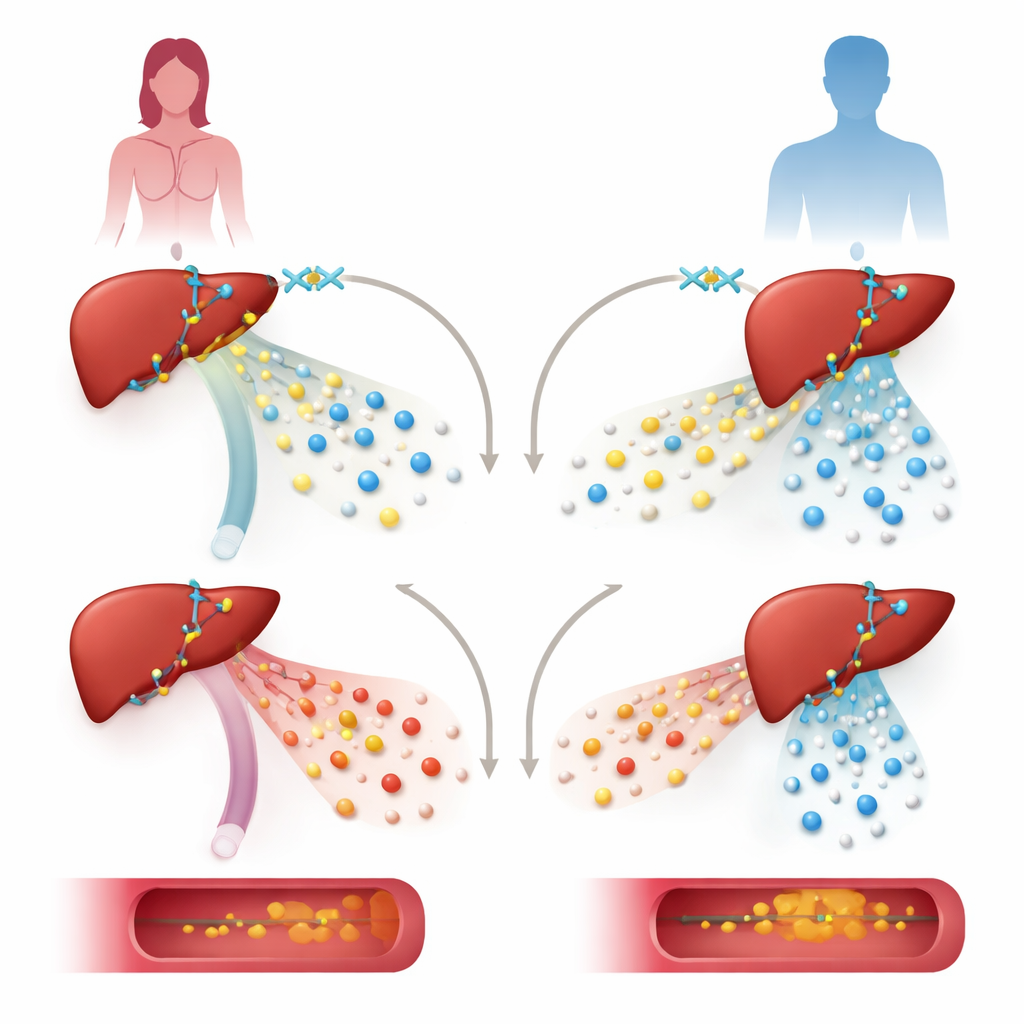
I centrum för detta arbete står ett protein som heter KDM6A, framställt från en gen på X-kromosomen. KDM6A transporterar inte kolesterol; istället verkar det i cellkärnan som en del av maskineriet som avgör vilka gener som är aktiva eller inaktiva. Eftersom det ligger på X-kromosomen och kan undkomma den vanliga inaktiveringen av en X hos honor kan dess aktivitet skilja sig mellan kvinnor och män. Författarna frågade om denna skillnad kan hjälpa till att förklara varför de två könen hanterar kolesterol och lipoproteiner—fettbärande partiklar i blodet—olika.
Vad händer när brytaren dämpas
För att testa KDM6As roll minskade teamet dess nivåer i mänskliga levercellinjer och i möss konstruerade för att sakna KDM6A endast i hepatocyter, leverns huvudceller. I leverceller från en kvinnlig donator sänkte nedreglering av KDM6A starkt aktiviteten hos gener som bygger och bearbetar lipoproteiner, inklusive gener som stödjer skyddande högdensitetslipoprotein (HDL). Samma manipulation i celler härledda från manliga källor påverkade en annan uppsättning gener och fokuserade inte på kolesterolvägar. Hos honor ledde förlust av KDM6A i levern till ett mer “aterogent” lipoproteinmönster: mycket låg-densitetslipoprotein (VLDL)-partiklar blev ovanligt rika på kolesterol, HDL-nivåerna sjönk och fettansamling i stora artären ökade, särskilt när djuren utsattes för en fettrik, kolesterolrik diet och ett genetiskt verktyg som driver ateroskleros.
Hur leverns genkontrollnätverk omkopplas
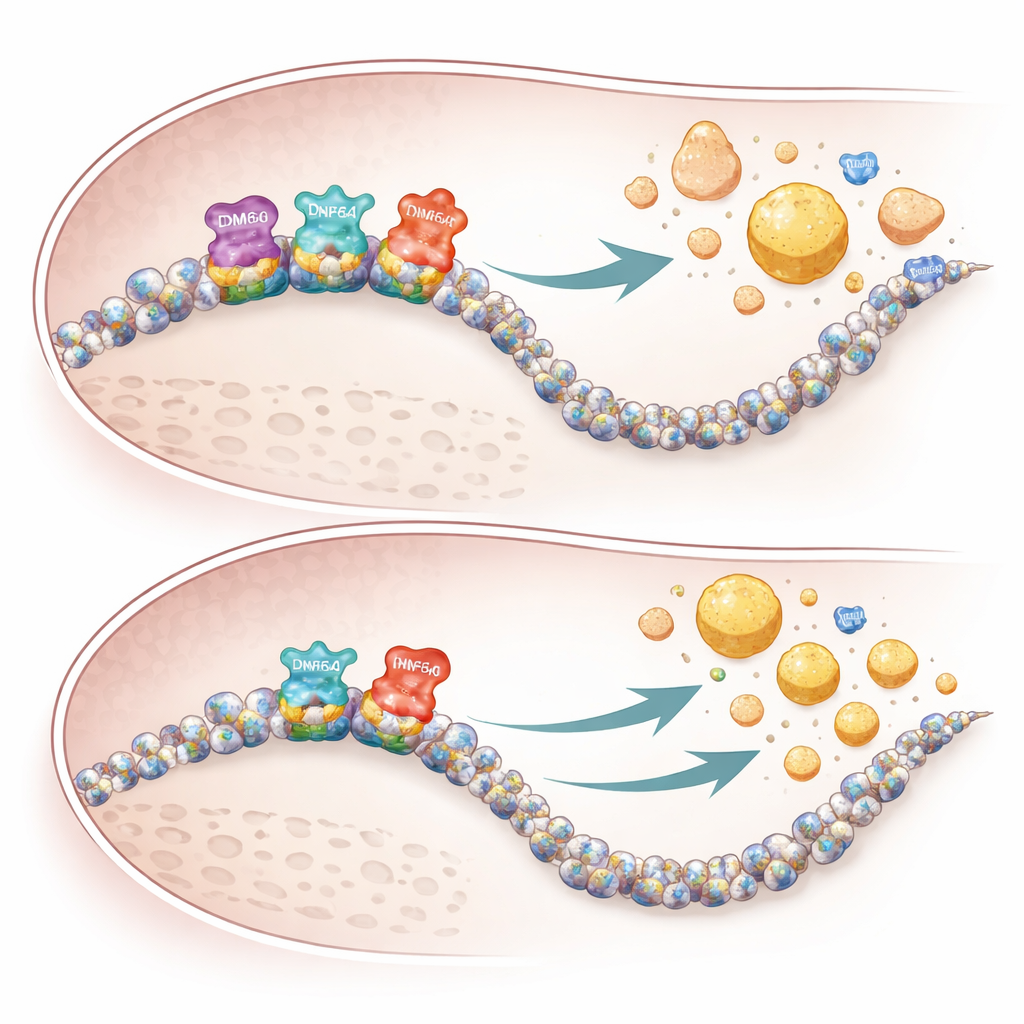
Genom att gå djupare kartlade forskarna hur KDM6A binder till DNA och interagerar med andra regulatorer. De fann att KDM6A samarbetar med en central levertranskriptionsfaktor, HNF4A, vid kontrollregioner nära många lipoprotein- och kolesterolgener, såsom de som kodar för ApoA1, ApoM och ApoH. Istället för att agera främst genom sin kända kemiska “raderare” av en specifik histonmark fungerar KDM6A här mer som ett stödstrukturellt element. Tillsammans med HNF4A och ett enzymkomplex kallat MLL3/4 hjälper det till att skapa öppet, aktivt kromatin—lösligt packat DNA-proteinstruktur—markerat av vissa kemiska flaggor som gynnar genaktivitet. Avlägsnande av KDM6A försvagade dessa aktiva markörer utan att kraftigt öka de repressiva markörer som det vanligtvis avlägsnar, vilket tyder på en icke-enzymatisk, strukturell roll.
En tredje aktör kopplar brytaren till kolesterolutflödet
Studien identifierar också en tredje faktor, CREBH, ett leverstress-responsivt protein som direkt förstärker gener som styr triglycerid- och kolesterolhantering. Med genomeomfattande bindningskartor visar författarna att när KDM6A förloras binder CREBH svagare till många av sina vanliga målgeners involverade i gallsyraproduktion, kolesterolrensning och HDL-bildning. Hos honmöss utan lever-KDM6A var dessa gener mindre aktiva, gallsyror samlades i lever och blod, och VLDL-partiklar som lämnade levern var ovanligt berikade på kolesterol men relativt fattiga på triglycerider. Denna snedvridna produktion, tillsammans med reducerade HDL-byggande gener, skapade förutsättningar för mer kolesterolavsättning i artärväggar.
Varför kvinnor påverkas mer
Det könsspecifika utfallet verkar reflektera både genetik och reservsystem. Eftersom KDM6A är X-bundet och uttrycks starkare i kvinnlig vävnad har dess förlust större effekt hos honor. Hanar bär en besläktad gen på Y-kromosomen, kallad KDM6C, som kan delvis kompensera i leverceller. Hos hanmöss förändrade deletion av KDM6A i hepatocyter knappast genaktivitet eller lipoproteinmönster, medan liknande manipulationer hos honor orsakade omfattande omprogrammering av kolesterolvägar och påtagliga förändringar i blodfetter. Human genetisk data från stora databaser speglade dessa mönster: sällsynta KDM6A-varianter var associerade med lägre nivåer av fördelaktigt ApoA1 och högre nivåer av aterogent ApoB hos människor.
Vad detta betyder för framtida behandlingar
Sammanfattningsvis avslöjar arbetet ett könsbundet KDM6A–HNF4A–CREBH-nätverk som finjusterar hur levern paketerar och rensar kolesterol. Hos kvinnor lutar störning av detta nätverk balansen mot fler artärtilltäppande lipoproteiner, mindre skyddande HDL och försämrad gallsyra-driven kolesterolutrensning—alla faktorer som främjar ateroskleros. Genom att lyfta fram en epigenetisk kontrollnod som skiljer sig mellan könen antyder studien att framtida kolesterolsänkande strategier—och läkemedel som riktar sig mot kromatinmodifierande enzymer—kan behöva skräddarsys olika för kvinnor och män för att undvika oönskade skiftningar i lipoproteinprofiler.
Citering: Chen, L., Kang, Z., Härdfeldt, J. et al. Sex-specific KDM6A-HNF4A-CREBH network controls lipoprotein cholesterol metabolism and atherosclerosis via epigenetic reprograming of hepatocytes. Nat Commun 17, 3945 (2026). https://doi.org/10.1038/s41467-026-70846-w
Nyckelord: kolesterolmetabolism, leverepigenetik, lipoproteiner, sexskillnader, ateroskleros