Clear Sky Science · pt
Rede KDM6A-HNF4A-CREBH específica por sexo controla o metabolismo do colesterol em lipoproteínas e a aterosclerose via reprogramação epigenética dos hepatócitos
Por que esta pesquisa importa para a saúde do coração
Infartos e acidentes vasculares cerebrais frequentemente começam com mudanças graduais em como o fígado processa o colesterol. Sabe-se que homens e mulheres diferem nos níveis de colesterol e no risco de artérias obstruídas, mas as razões subjacentes ainda estão sendo desvendadas. Este estudo revela um sistema de controle ligado ao sexo em células hepáticas que ajuda a manter as gorduras sanguíneas em uma faixa mais saudável, especialmente nas fêmeas. Entender esse sistema pode apontar caminhos para tratamentos mais personalizados para colesterol alto e aterosclerose.
Um interruptor hepático no cromossomo X
No centro deste trabalho está uma proteína chamada KDM6A, produzida por um gene no cromossomo X. KDM6A não transporta colesterol; em vez disso, atua no núcleo celular como parte da maquinaria que decide quais genes são ativados ou silenciados. Como está no cromossomo X e pode escapar da inativação usual de um dos X nas fêmeas, sua atividade pode diferir entre fêmeas e machos. Os autores perguntaram se essa diferença ajuda a explicar por que os dois sexos lidam de formas distintas com colesterol e lipoproteínas — partículas que carregam gordura no sangue.
O que acontece quando o interruptor é reduzido
Para testar o papel de KDM6A, a equipe diminuiu seus níveis em linhagens celulares hepáticas humanas e em camundongos geneticamente modificados para não expressarem KDM6A apenas nos hepatócitos, as principais células do fígado. Em células hepáticas de uma doadora feminina, reduzir KDM6A diminuiu fortemente a atividade de genes que constroem e processam lipoproteínas, incluindo genes que sustentam a lipoproteína de alta densidade (HDL) protetora. A mesma manipulação em células derivadas de doador masculino afetou um conjunto diferente de genes e não se concentrou nas vias do colesterol. Em camundongas fêmeas, a perda de KDM6A no fígado levou a um padrão de lipoproteínas mais “aterogênico”: partículas de lipoproteína de densidade muito baixa (VLDL) tornaram-se incomumente ricas em colesterol, os níveis de HDL caíram e o acúmulo de gordura na artéria principal aumentou, especialmente quando os animais foram submetidos a uma dieta rica em gordura e colesterol e a um instrumento genético que promove aterosclerose.
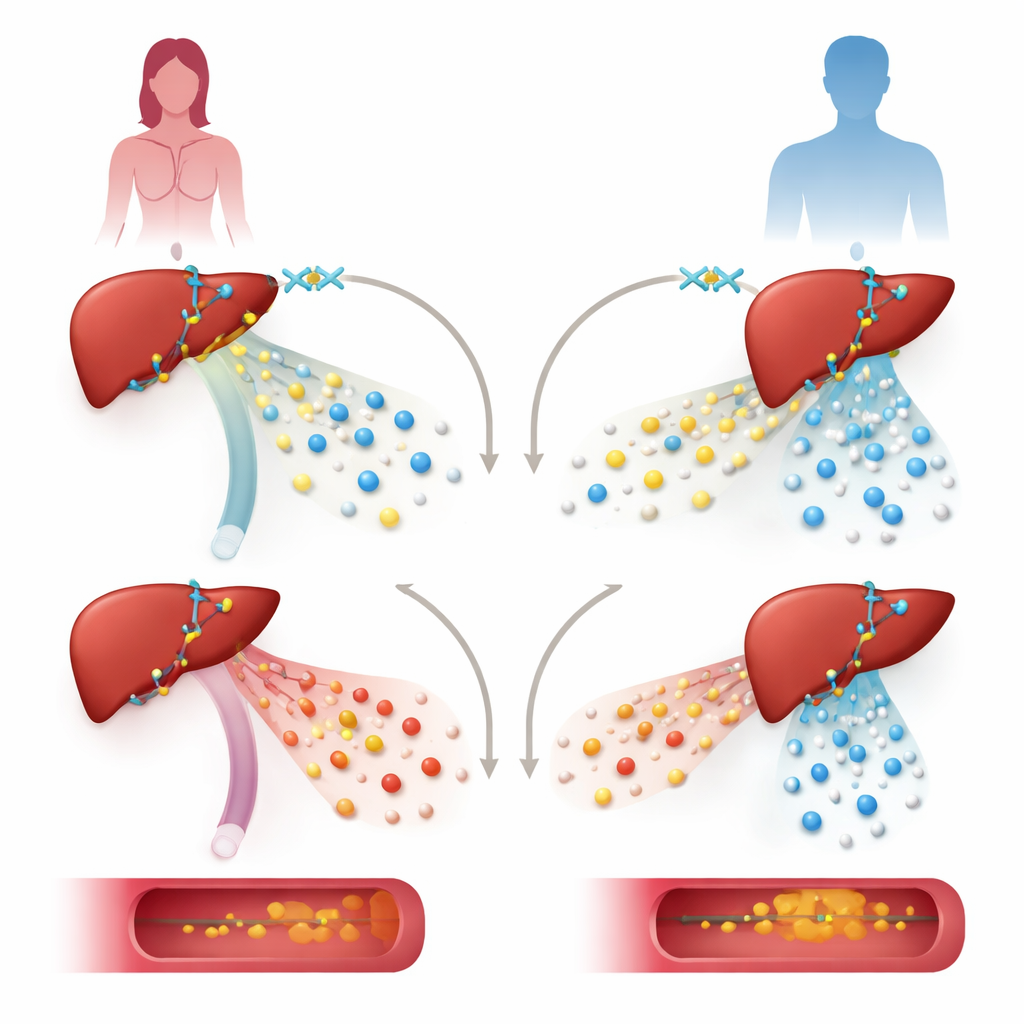
Como a rede de controle gênico do fígado é reconfigurada
Ao investigar mais a fundo, os pesquisadores mapearam como KDM6A se localiza no DNA e interage com outros reguladores. Eles descobriram que KDM6A faz parceria com um fator de transcrição hepático chave, HNF4A, em regiões de controle próximas a muitos genes de lipoproteínas e colesterol, como aqueles que codificam as proteínas ApoA1, ApoM e ApoH. Em vez de agir principalmente por meio de sua conhecida função enzimática de “apagador” de uma marca específica de histona, KDM6A aqui comporta-se mais como uma plataforma estrutural. Junto com HNF4A e um complexo enzimático chamado MLL3/4, ajuda a criar cromatina aberta e ativa — estrutura DNA-proteína menos compacta — marcada por determinados sinais químicos que favorecem a atividade gênica. Remover KDM6A enfraqueceu essas marcas ativas sem aumentar muito as marcas repressivas que normalmente apaga, sugerindo um papel estrutural não enzimático.
Um terceiro ator conecta o interruptor à saída de colesterol
O estudo também identifica um terceiro fator, CREBH, uma proteína hepática responsiva ao estresse que estimula diretamente genes que controlam o manejo de triglicerídeos e colesterol. Usando mapas de ligação em todo o genoma, os autores mostram que quando KDM6A é perdido, o CREBH se liga com menos intensidade a muitos de seus genes-alvo habituais envolvidos na produção de ácidos biliares, depuração do colesterol e formação de HDL. Em camundongas fêmeas sem KDM6A hepático, esses genes ficaram menos ativos, ácidos biliares se acumularam no fígado e no sangue, e as partículas de VLDL saíram do fígado incomumente enriquecidas em colesterol, mas relativamente pobres em triglicerídeos. Essa saída enviesada, combinada com a redução dos genes que constroem HDL, preparou o terreno para maior deposição de colesterol nas paredes das artérias.
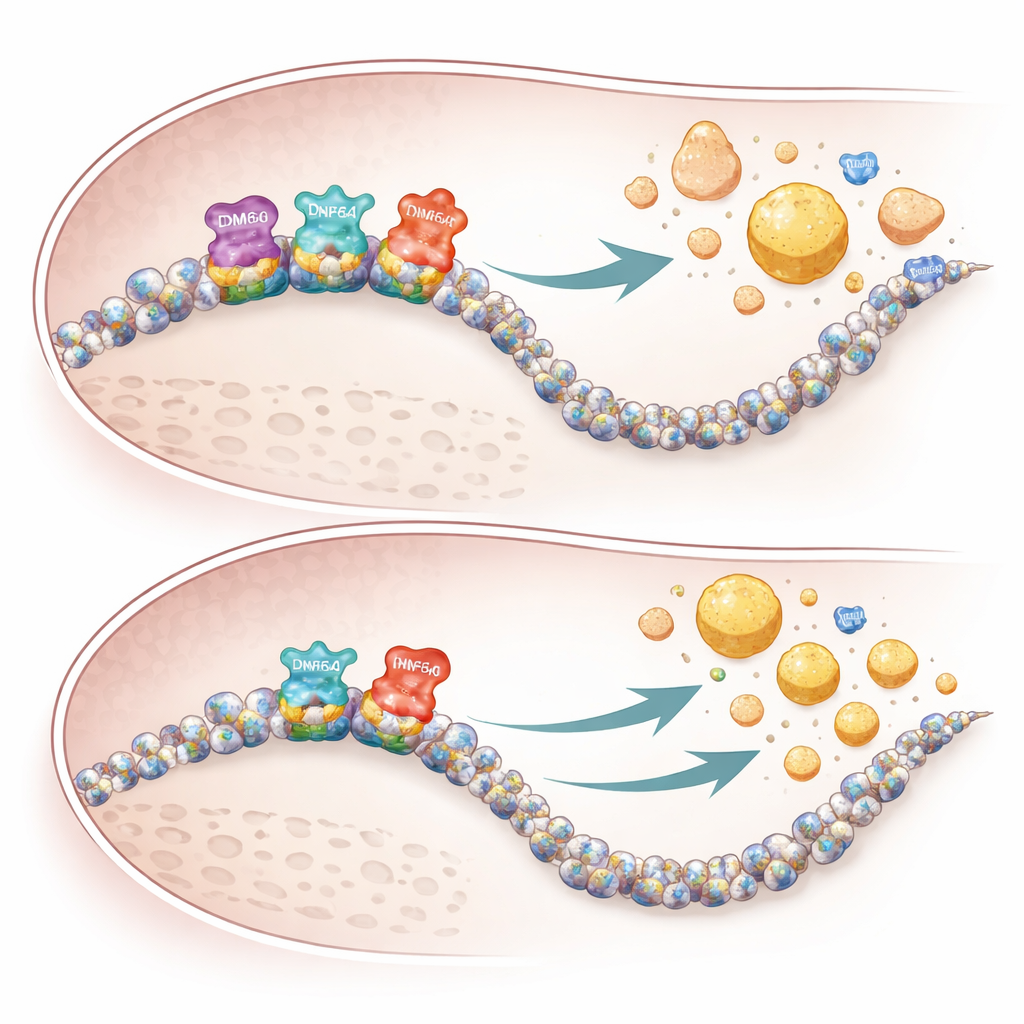
Por que as fêmeas são mais afetadas
A natureza específica por sexo das descobertas parece refletir tanto genética quanto sistemas de reserva. Como KDM6A é ligado ao X e mais fortemente expresso em tecidos femininos, sua perda tem um impacto maior nas fêmeas. Machos carregam um gene relacionado no cromossomo Y, chamado KDM6C, que pode compensar parcialmente nas células hepáticas. Em camundongos machos, deletar KDM6A nos hepatócitos mal alterou a atividade gênica ou os padrões de lipoproteínas, enquanto manipulações semelhantes em fêmeas causaram reprogramação ampla das vias do colesterol e mudanças marcantes nos lipídios sanguíneos. Dados genéticos humanos de grandes bancos ecoaram esses padrões: variantes raras de KDM6A foram associadas a níveis mais baixos da benéfica ApoA1 e níveis mais altos da aterogênica ApoB em pessoas.
O que isso significa para tratamentos futuros
No conjunto, o trabalho revela uma rede KDM6A–HNF4A–CREBH ligada ao sexo que ajusta finamente como o fígado empacota e elimina o colesterol. Nas fêmeas, a interrupção dessa rede inclina o equilíbrio para lipoproteínas mais obstruidoras das artérias, menos HDL protetor e eliminação do colesterol via ácidos biliares comprometida, todos fatores que promovem aterosclerose. Ao destacar um eixo de controle epigenético que difere entre os sexos, o estudo sugere que futuras estratégias redutoras de colesterol — e fármacos que miram enzimas que modificam a cromatina — podem precisar ser adaptados de forma diferente para mulheres e homens, para evitar mudanças indesejadas no perfil das lipoproteínas.
Citação: Chen, L., Kang, Z., Härdfeldt, J. et al. Sex-specific KDM6A-HNF4A-CREBH network controls lipoprotein cholesterol metabolism and atherosclerosis via epigenetic reprograming of hepatocytes. Nat Commun 17, 3945 (2026). https://doi.org/10.1038/s41467-026-70846-w
Palavras-chave: metabolismo do colesterol, epigenética hepática, lipoproteínas, diferenças entre sexos, aterosclerose