Clear Sky Science · ru
Сеть KDM6A–HNF4A–CREBH, зависящая от пола, контролирует метаболизм липопротеинного холестерина и атеросклероз посредством эпигенетической перепрограммировки гепатоцитов
Почему это исследование важно для здоровья сердца
Инфаркты и инсульты часто начинаются с медленных изменений в том, как печень обращается с холестерином. Известно, что у мужчин и женщин различаются уровни холестерина и риск закупорки артерий, но причины этих различий всё ещё изучаются. В этом исследовании показана зависящая от пола система контроля в печёночных клетках, которая помогает поддерживать липиды в крови в более здоровых пределах, особенно у женщин. Понимание этой системы может указать путь к более персонализированным методам лечения высокого холестерина и атеросклероза.
Переключатель в печени на Х-хромосоме
В центре работы находится белок KDM6A, кодируемый геном на Х-хромосоме. KDM6A сам по себе не переносит холестерин; он действует в ядре клетки как часть механизма, определяющего, какие гены включаются или выключаются. Поскольку ген расположен на Х-хромосоме и может «ускользать» от обычной инактивации одной из Х у самок, его активность может отличаться у женщин и мужчин. Авторы задали вопрос, помогает ли эта разница объяснить, почему оба пола по-разному обрабатывают холестерин и липопротеины — частицы, переносящие жиры в крови.
Что происходит при снижении работы переключателя
Чтобы проверить роль KDM6A, команда снизила его уровень в линиях человеческих печёночных клеток и в мышах, у которых KDM6A удалён только в гепатоцитах. В печёночных клетках от донора-женщины снижение KDM6A резко понижало активность генов, участвующих в синтезе и переработке липопротеинов, включая гены, поддерживающие защитный липопротеин высокой плотности (HDL). Та же манипуляция в клетках мужского происхождения затрагивала иной набор генов и не была сосредоточена на путях холестерина. У самок мышей потеря KDM6A в печени приводила к более «атерогенному» профилю липопротеинов: частицы очень низкой плотности (VLDL) становились необычно богаты холестерином, уровни HDL падали, а отложение жиров в главной артерии увеличивалось, особенно при воздействии диеты с высоким содержанием жиров и холестерина и генетического фактора, усиливающего атеросклероз.
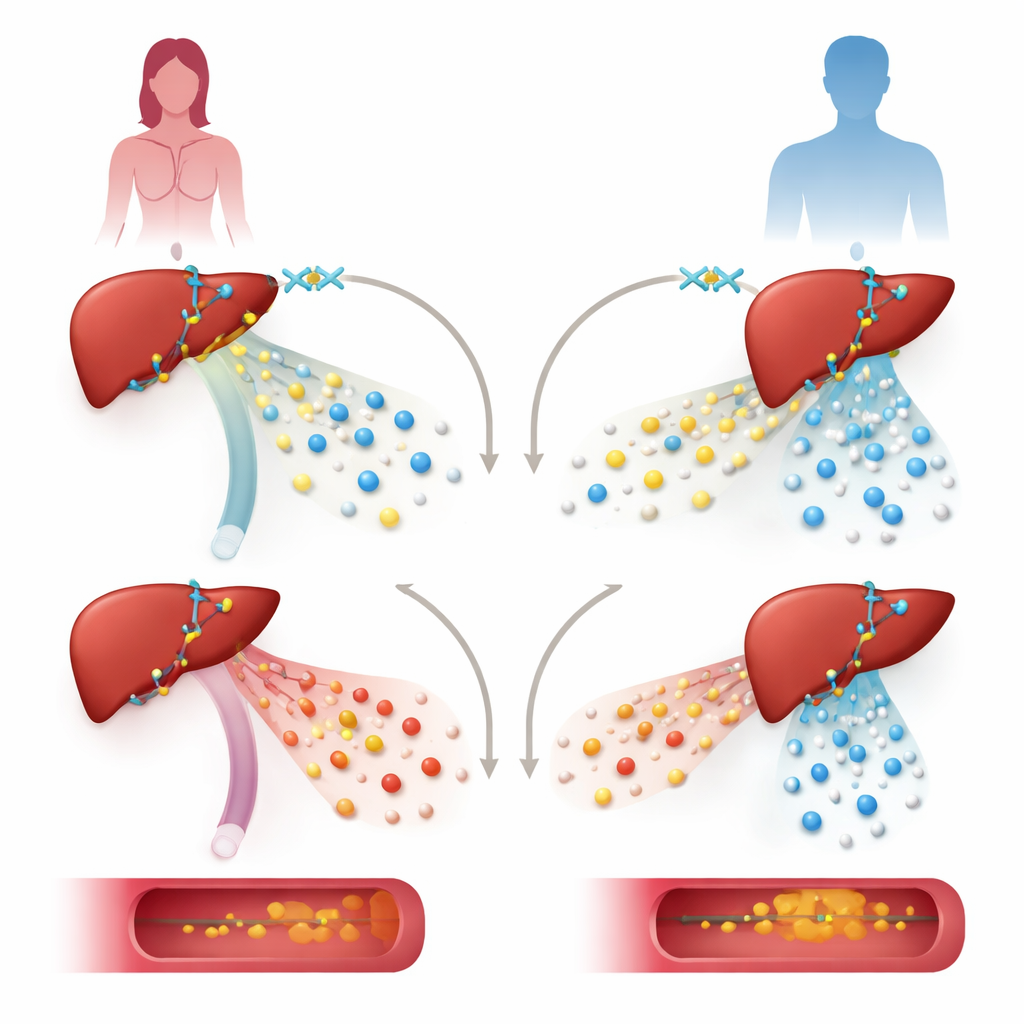
Как перепрограммируется сеть генетического контроля в печени
Углубляясь, исследователи картировали, где KDM6A располагается на ДНК и как взаимодействует с другими регуляторами. Они обнаружили, что KDM6A взаимодействует с ключевым печёночным транскрипционным фактором HNF4A в областях управления рядом со многими генами липопротеинов и холестерина, такими как гены, кодирующие белки ApoA1, ApoM и ApoH. Вместо того чтобы действовать главным образом через свою известную химическую «стирающую» функцию на определённую метку гистонов, KDM6A здесь ведёт себя больше как каркас. Вместе с HNF4A и ферментным комплексом MLL3/4 он способствует формированию открытой, активной хроматиновой структуры — слабо упакованной ДНК‑белковой компоновки — отмеченной химическими маркерами, благоприятствующими активности генов. Удаление KDM6A ослабляло эти активные метки без значительного увеличения репрессивных меток, которые он обычно «стирает», что указывает на неэнзимную, структурную роль.
Третий участник связывает переключатель с выходом холестерина
Исследование также выявляет третьий фактор — CREBH, печёночный белок, реагирующий на стресс, который напрямую усиливает гены, управляющие переработкой триглицеридов и холестерина. С помощью карт глобального связывания генома авторы показывают, что при потере KDM6A CREBH слабее связывается со многими своими обычными целевыми генами, вовлечёнными в синтез желчных кислот, клиренс холестерина и формирование HDL. У самок мышей без печёночного KDM6A эти гены были менее активны, желчные кислоты накапливались в печени и крови, а VLDL, покидая печень, были необычно обогащены холестерином, но относительно бедны триглицеридами. Такое смещённое соотношение выхода в сочетании со снижением генов, формирующих HDL, создавало условия для усиленного отложения холестерина в стенках артерий.
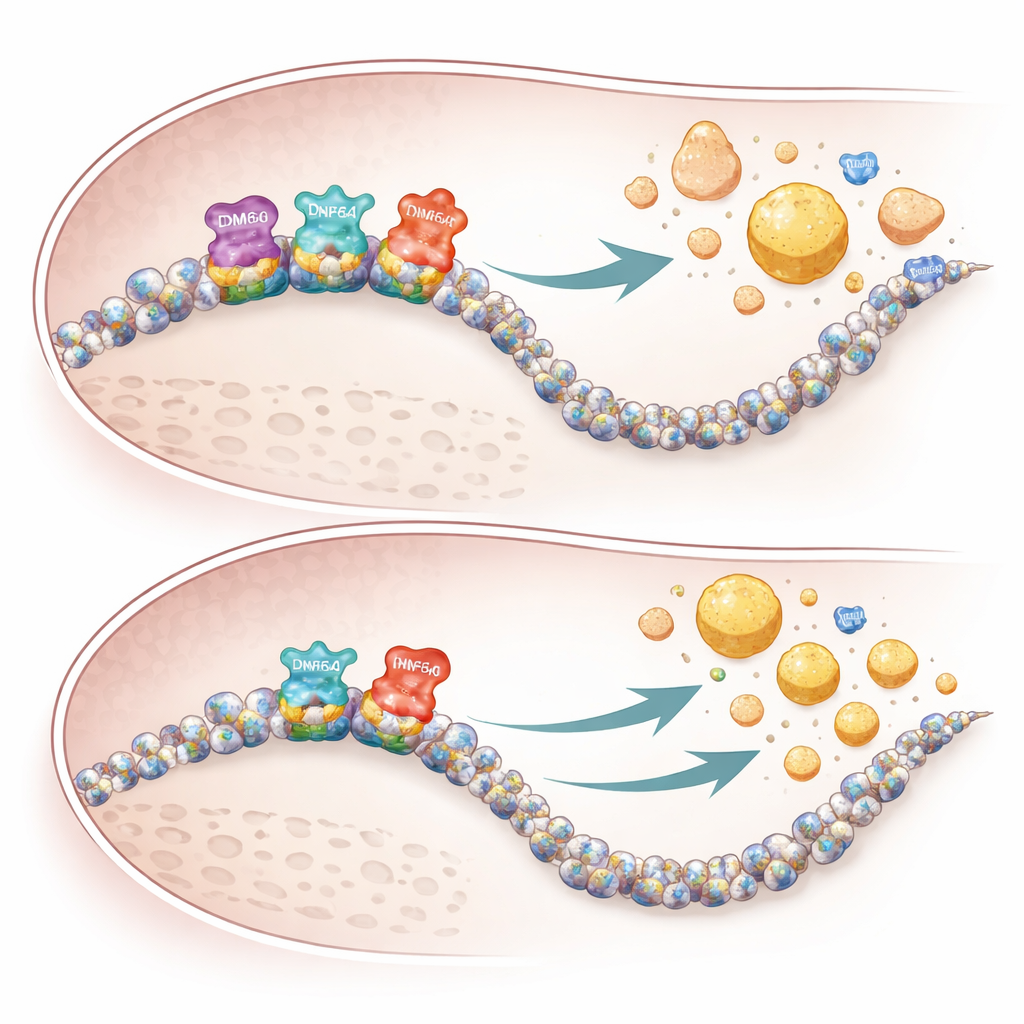
Почему самки испытывают больший эффект
Специфичность по полу, по-видимому, отражает как генетику, так и компенсаторные механизмы. Поскольку KDM6A находится на Х-хромосоме и сильнее экспрессируется в тканях самок, его потеря оказывает более заметное влияние у самок. У самцов имеется родственный ген на Y-хромосоме, называемый KDM6C, который может частично компенсировать в печёночных клетках. У самцов мышей удаление KDM6A в гепатоцитах едва меняло активность генов или профиль липопротеинов, тогда как аналогичные вмешательства у самок вызывали широкую перепрограммировку путей холестерина и заметные изменения в липидах крови. Данные человека из больших баз также отразили эти закономерности: редкие варианты KDM6A были связаны с более низкими уровнями полезного ApoA1 и более высокими уровнями атерогенного ApoB у людей.
Что это значит для будущих терапий
В целом работа выявляет зависящую от пола сеть KDM6A–HNF4A–CREBH, которая тонко настраивает, как печень упаковывает и удаляет холестерин. У самок нарушение этой сети сдвигает баланс в сторону более атерогенных липопротеинов, меньшего количества защитного HDL и нарушенного выведения холестерина через желчные кислоты — всё это способствует развитию атеросклероза. Подчёркивая эпигенетический узел контроля, различающийся по полу, исследование даёт основание полагать, что будущие стратегии снижения холестерина и препараты, нацеленные на ферменты, модифицирующие хроматин, возможно, потребуется адаптировать по‑разному для женщин и мужчин, чтобы избежать непреднамеренных сдвигов в профилях липопротеинов.
Цитирование: Chen, L., Kang, Z., Härdfeldt, J. et al. Sex-specific KDM6A-HNF4A-CREBH network controls lipoprotein cholesterol metabolism and atherosclerosis via epigenetic reprograming of hepatocytes. Nat Commun 17, 3945 (2026). https://doi.org/10.1038/s41467-026-70846-w
Ключевые слова: метаболизм холестерина, эпигенетика печени, липопротеины, половые различия, атеросклероз