Clear Sky Science · es
La red KDM6A-HNF4A-CREBH específica por sexo controla el metabolismo del colesterol en lipoproteínas y la aterosclerosis mediante la reprogramación epigenética de los hepatocitos
Por qué esta investigación importa para la salud cardiaca
Los infartos y los ictus suelen comenzar con cambios lentos en la forma en que el hígado maneja el colesterol. Se sabe que hombres y mujeres difieren en sus niveles de colesterol y en el riesgo de arterias obstruidas, pero las razones subyacentes aún se están descubriendo. Este estudio revela un sistema de control ligado al sexo en las células hepáticas que ayuda a mantener las grasas en sangre en un rango más saludable, especialmente en las mujeres. Comprender este sistema podría orientar tratamientos más personalizados para el colesterol alto y la aterosclerosis.
Un interruptor hepático en el cromosoma X
En el centro de este trabajo hay una proteína llamada KDM6A, codificada por un gen en el cromosoma X. KDM6A no transporta colesterol; actúa en el núcleo celular como parte de la maquinaria que decide qué genes se activan o se silencian. Debido a su ubicación en el cromosoma X y a que puede escapar de la inactivación típica de una X en las hembras, su actividad puede diferir entre mujeres y hombres. Los autores preguntaron si esta diferencia podría ayudar a explicar por qué los dos sexos manejan el colesterol y las lipoproteínas—partículas que transportan grasas en la sangre—de maneras distintas.
Qué ocurre cuando se atenúa el interruptor
Para probar el papel de KDM6A, el equipo redujo sus niveles en líneas celulares hepáticas humanas y en ratones modificados para carecer de KDM6A solo en los hepatocitos, las principales células del hígado. En células hepáticas procedentes de una donante femenina, reducir KDM6A disminuyó con fuerza la actividad de genes que fabrican y procesan lipoproteínas, incluyendo genes que apoyan a la protectora lipoproteína de alta densidad (HDL). La misma manipulación en células derivadas de un donante masculino afectó a un conjunto distinto de genes y no se centró en las vías del colesterol. En ratonas, la pérdida de KDM6A hepática condujo a un patrón de lipoproteínas más “aterogénico”: las partículas de lipoproteínas de muy baja densidad (VLDL) se volvieron inusualmente ricas en colesterol, los niveles de HDL cayeron y el depósito de grasa en la arteria principal aumentó, sobre todo cuando los animales recibieron una dieta alta en grasas y colesterol y una herramienta genética que favorece la aterosclerosis.
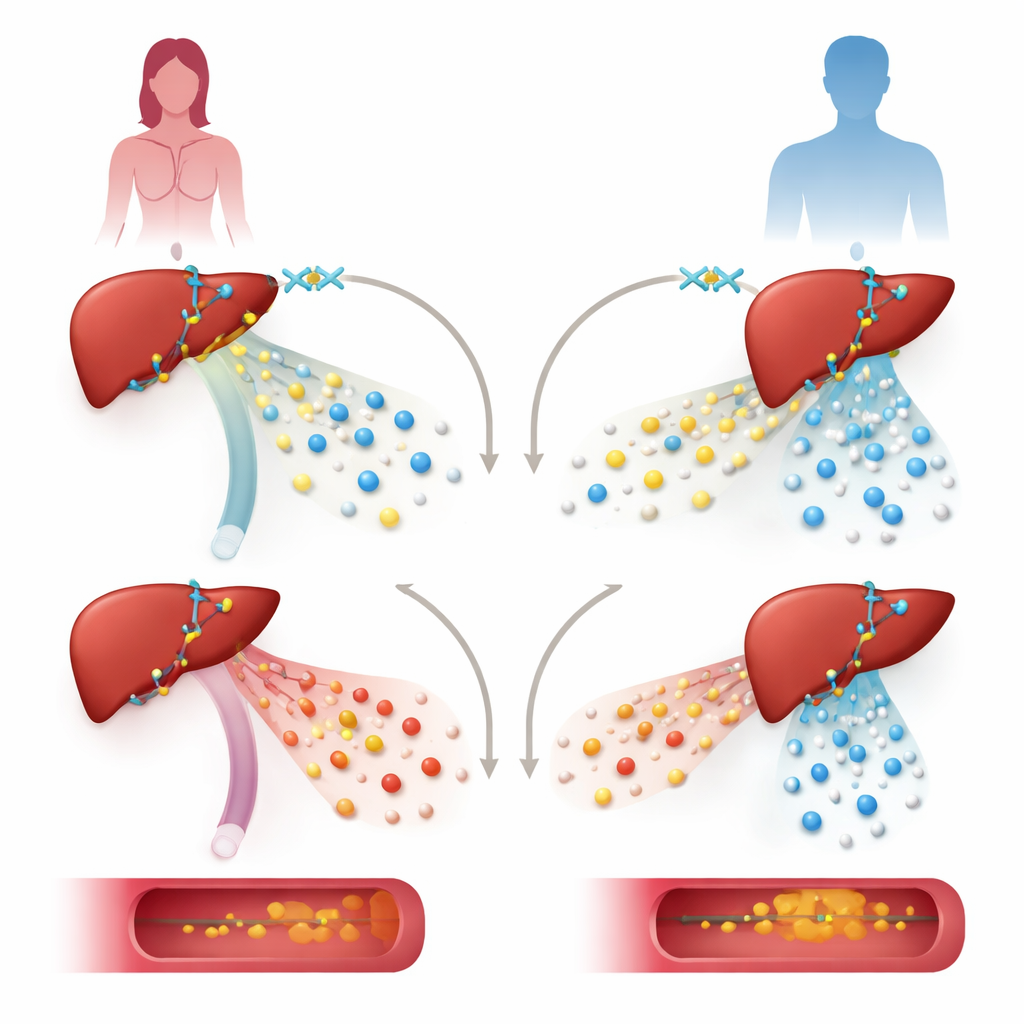
Cómo se reconfigura la red de control génico hepática
Indagando más a fondo, los investigadores cartografiaron cómo KDM6A se sitúa sobre el ADN e interactúa con otros reguladores. Encontraron que KDM6A se asocia con un factor de transcripción hepático clave, HNF4A, en regiones de control cercanas a muchos genes de lipoproteínas y colesterol, como los que codifican las proteínas ApoA1, ApoM y ApoH. En lugar de actuar principalmente mediante su conocida función química de “borrador” sobre una marca específica de histona, KDM6A aquí se comporta más como un andamiaje. Junto con HNF4A y un complejo enzimático llamado MLL3/4, contribuye a crear cromatina abierta y activa—una estructura ADN-proteína menos compacta—marcada por señales químicas que favorecen la actividad génica. La eliminación de KDM6A debilitó estas marcas activas sin aumentar considerablemente las marcas represoras que suele eliminar, lo que sugiere un papel estructural no enzimático.
Un tercer actor vincula el interruptor con la salida de colesterol
El estudio también identifica un tercer factor, CREBH, una proteína hepática sensible al estrés que potencia directamente genes que gobiernan el manejo de triglicéridos y colesterol. Mediante mapas de unión a todo el genoma, los autores muestran que cuando KDM6A se pierde, CREBH se une con menos fuerza a muchos de sus genes diana habituales implicados en la producción de ácidos biliares, la eliminación de colesterol y la formación de HDL. En ratonas sin KDM6A hepático, estos genes fueron menos activos, se acumularon ácidos biliares en hígado y sangre, y las VLDL que salían del hígado estaban inusualmente enriquecidas en colesterol pero relativamente pobres en triglicéridos. Esta salida desequilibrada, combinada con la reducción de genes formadores de HDL, preparó el terreno para un mayor depósito de colesterol en las paredes arteriales.
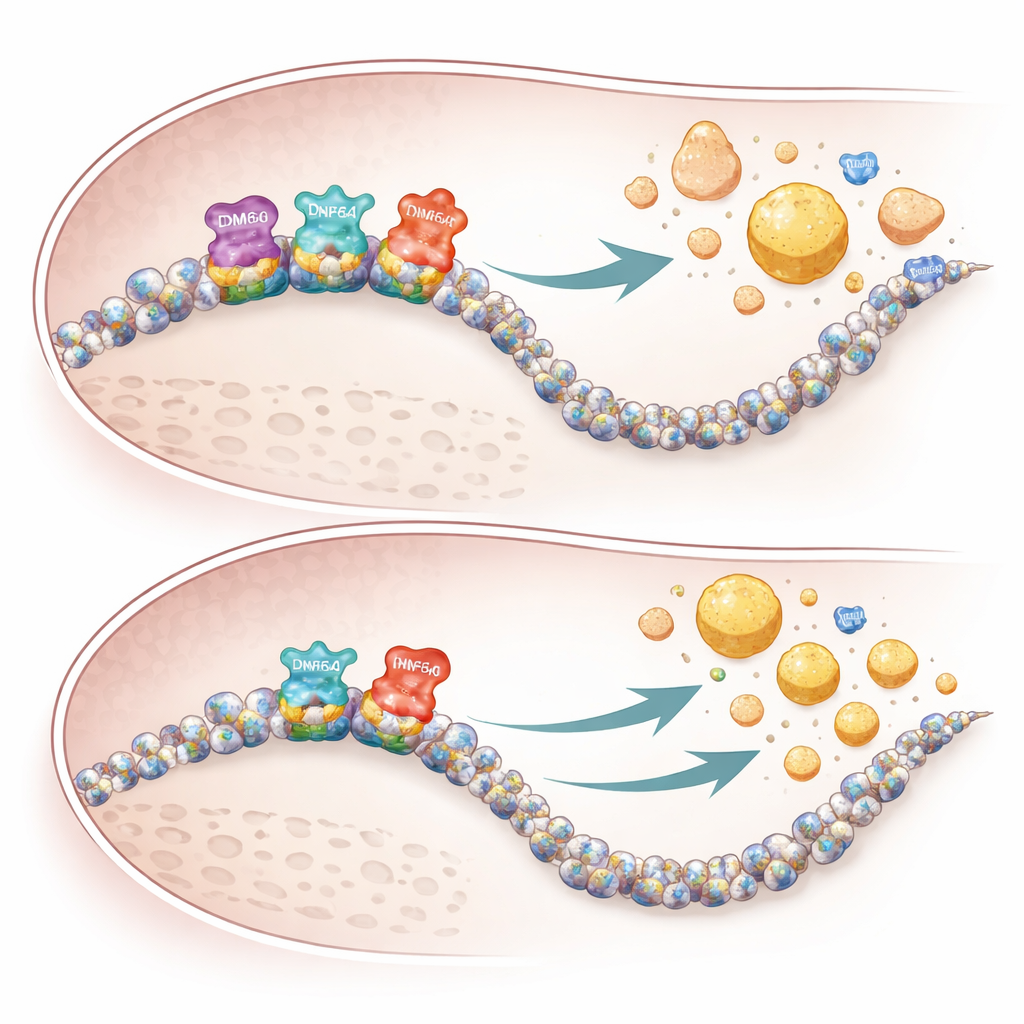
Por qué las hembras se ven más afectadas
La naturaleza específica por sexo de los hallazgos parece reflejar tanto la genética como los sistemas de respaldo. Debido a que KDM6A está ligada al cromosoma X y se expresa con mayor intensidad en tejidos femeninos, su pérdida tiene un impacto mayor en las hembras. Los machos llevan un gen relacionado en el cromosoma Y, llamado KDM6C, que puede compensar parcialmente en las células hepáticas. En ratones machos, la eliminación de KDM6A en hepatocitos apenas cambió la actividad génica o los patrones de lipoproteínas, mientras que manipulaciones similares en hembras provocaron una amplia reprogramación de las vías del colesterol y cambios llamativos en los lípidos sanguíneos. Datos genéticos humanos procedentes de grandes bases de datos reprodujeron estos patrones: variantes raras en KDM6A se asociaron con niveles más bajos de la beneficiosa ApoA1 y niveles más altos de la aterogénica ApoB en personas.
Qué significa esto para futuros tratamientos
En conjunto, el trabajo revela una red ligada al sexo KDM6A–HNF4A–CREBH que afina cómo el hígado empaqueta y elimina el colesterol. En las hembras, la interrupción de esta red inclina la balanza hacia lipoproteínas más propensas a obstruir las arterias, menos HDL protector y una eliminación de colesterol por ácidos biliares menos eficiente, todo lo cual favorece la aterosclerosis. Al destacar un centro de control epigenético que difiere entre sexos, el estudio sugiere que las futuras estrategias para reducir el colesterol—y los fármacos que apuntan a enzimas que modifican la cromatina—podrían necesitar adaptarse de forma diferente en mujeres y hombres para evitar cambios indeseados en los perfiles de lipoproteínas.
Cita: Chen, L., Kang, Z., Härdfeldt, J. et al. Sex-specific KDM6A-HNF4A-CREBH network controls lipoprotein cholesterol metabolism and atherosclerosis via epigenetic reprograming of hepatocytes. Nat Commun 17, 3945 (2026). https://doi.org/10.1038/s41467-026-70846-w
Palabras clave: metabolismo del colesterol, epigenética hepática, lipoproteínas, diferencias entre sexos, aterosclerosis