Clear Sky Science · nl
Geslachtspecifiek KDM6A-HNF4A-CREBH-netwerk stuurt lipoproteïne-cholesteroldistributie en atherosclerose via epigenetische herprogrammering van hepatocyten
Waarom dit onderzoek belangrijk is voor hartgezondheid
Hartaanvallen en beroertes beginnen vaak met geleidelijke veranderingen in hoe de lever cholesterol beheert. Het is bekend dat mannen en vrouwen verschillen in hun cholesterolniveaus en risico op verstopte slagaders, maar de onderliggende oorzaken worden nog onderzocht. Deze studie onthult een geslachtsgebonden controlesysteem in levercellen dat helpt bloedlipiden binnen een gezonder bereik te houden, vooral bij vrouwen. Inzicht in dit systeem kan wijzen op meer gepersonaliseerde behandelingen voor hoog cholesterol en atherosclerose.
Een leverschakelaar op het X-chromosoom
Centraal in dit werk staat een eiwit genaamd KDM6A, gecodeerd door een gen op het X-chromosoom. KDM6A vervoert geen cholesterol; het werkt in de celkern als onderdeel van het mechanisme dat bepaalt welke genen aan of uit staan. Omdat het op het X-chromosoom ligt en soms de gebruikelijke inactivatie van één X bij vrouwen kan ontsnappen, kan de activiteit tussen vrouwen en mannen verschillen. De auteurs onderzochten of dit verschil helpt verklaren waarom de seksen cholesterol en lipoproteïnen—de vettige deeltjes in het bloed—verschillend reguleren.
Wat er gebeurt als de schakel wordt gedimd
Om de rol van KDM6A te testen verlaagde het team de niveaus ervan in menselijke levercellijnen en in muizen die zo waren gemaakt dat KDM6A alleen in hepatocyten ontbrak. In levercellen van een vrouwelijke donor leidde het verminderen van KDM6A tot sterk verlaagde activiteit van genen die lipoproteïnen opbouwen en verwerken, inclusief genen die beschermend high-density lipoproteïne (HDL) ondersteunen. Dezelfde ingreep in mannelijke cellen trof een andere set genen en richtte zich niet op cholesterolroutes. Bij vrouwelijke muizen veroorzaakte verlies van KDM6A in de lever een meer “atherogene” lipoproteïnenpatroon: very low-density lipoproteïne (VLDL)-deeltjes werden ongewoon rijk aan cholesterol, HDL-niveaus daalden en vetophoping in de hoofdslagader nam toe, vooral wanneer de dieren werden blootgesteld aan een vet- en cholesterolrijk dieet en een genetisch middel dat atherosclerose bevordert.
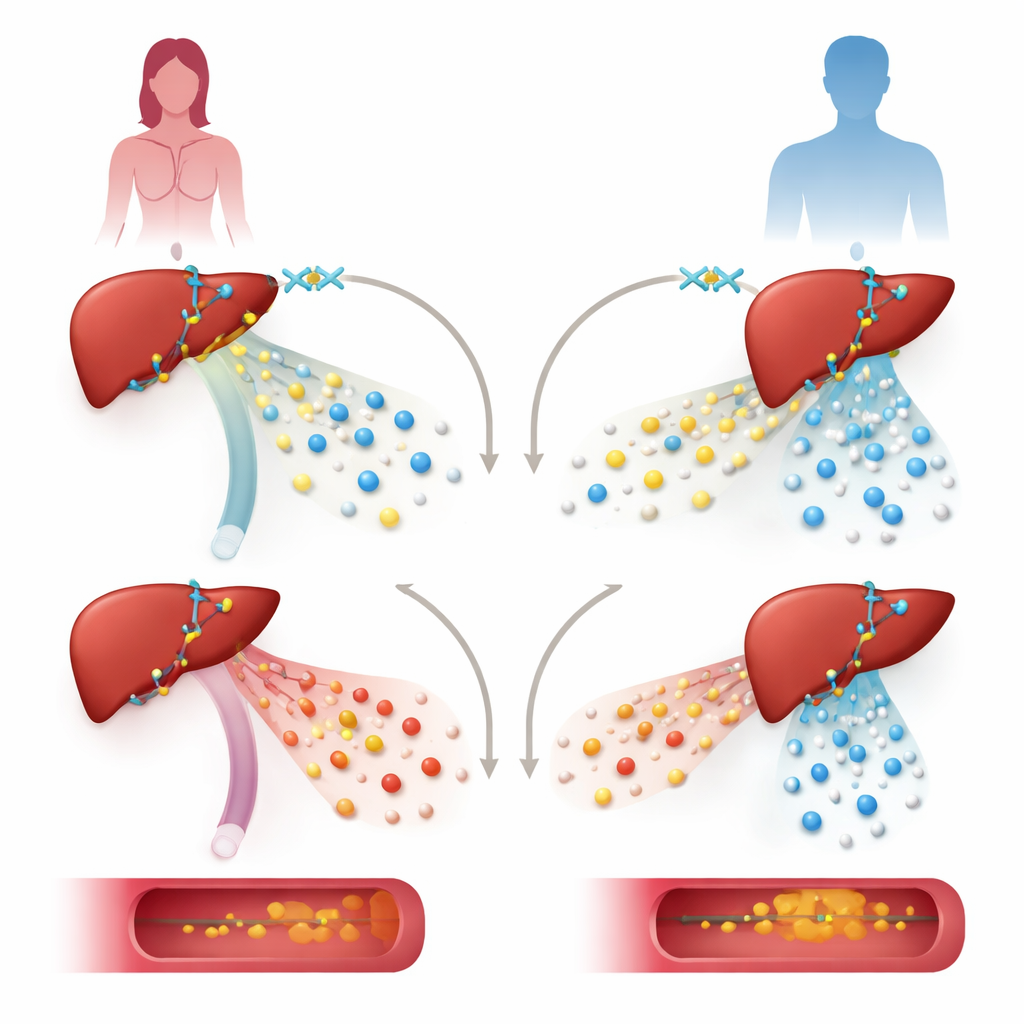
Hoe het gencontrole-netwerk van de lever wordt hersnoeid
Dieper gravend brachten de onderzoekers in kaart hoe KDM6A op het DNA zit en met andere regulatoren samenwerkt. Ze vonden dat KDM6A samenwerkt met een belangrijke levertranscriptiefactor, HNF4A, bij controlegebieden nabij veel lipoproteïne- en cholesterolgenen, zoals genen die ApoA1-, ApoM- en ApoH-eiwitten produceren. In plaats van hoofdzakelijk te werken via zijn bekende chemische “gum”-functie op een specifiek histonmerk, gedraagt KDM6A zich hier meer als een steiger. Samen met HNF4A en een enzymcomplex genaamd MLL3/4 helpt het open, actief chromatine te vormen—losjes verpakte DNA-eiwitstructuur—gemerkt door bepaalde chemische signalen die genactiviteit bevorderen. Het verwijderen van KDM6A verzwakte deze actieve merken zonder de repressieve merken die het gewoonlijk wist sterk te verhogen, wat wijst op een niet-enzymatische, structurele rol.
Een derde speler koppelt de schakel aan cholesterolproductie
De studie identificeert ook een derde factor, CREBH, een lever-eiwit dat reageert op stress en direct genen stimuleert die triglyceride- en cholesterolverwerking regelen. Met genoomwijde bindingskaarten tonen de auteurs aan dat wanneer KDM6A verloren gaat, CREBH minder sterk bindt aan veel van zijn gebruikelijke doelgenen die betrokken zijn bij galzuurproductie, cholesterolclearance en HDL-vorming. In vrouwelijke muizen zonder hepatische KDM6A waren deze genen minder actief, stapelden galzuren zich op in lever en bloed, en verlieten VLDL-deeltjes de lever ongewoon verrijkt aan cholesterol maar relatief arm aan triglyceriden. Deze scheve output, gecombineerd met verminderde HDL-opbouwgenen, creëerde een omgeving die leidde tot meer cholesterolverstrekking in de vaatwanden.
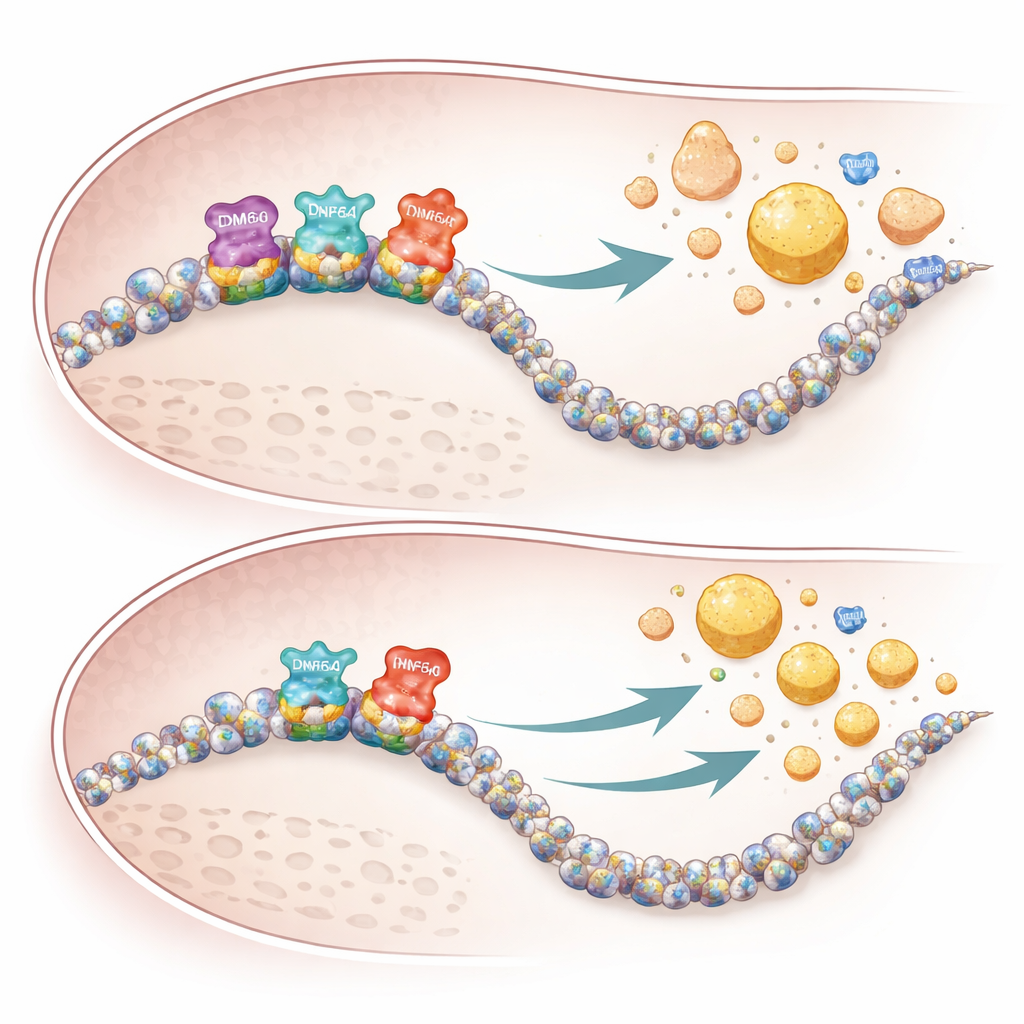
Waarom vrouwen zwaarder worden getroffen
Het geslachtspecifieke karakter van de bevindingen lijkt zowel genetische oorzaken als back-upsystemen te weerspiegelen. Omdat KDM6A X-gebonden is en sterker tot expressie komt in weefsels van vrouwen, heeft het verlies ervan een grotere impact bij vrouwen. Mannen dragen een verwant gen op het Y-chromosoom, KDM6C genoemd, dat gedeeltelijk kan compenseren in levercellen. Bij mannelijke muizen veranderde het verwijderen van KDM6A in hepatocyten nauwelijks genactiviteit of lipoproteïnepatronen, terwijl vergelijkbare manipulaties bij vrouwtjes brede herprogrammering van cholesterolroutes en opvallende veranderingen in bloedlipiden teweegbrachten. Menselijke genetische gegevens uit grote databases weerspiegelden deze patronen: zeldzame KDM6A-varianten waren geassocieerd met lagere niveaus van het gunstige ApoA1 en hogere niveaus van het atherogene ApoB bij mensen.
Wat dit betekent voor toekomstige behandelingen
Samengevat onthult het werk een geslachtsgebonden KDM6A–HNF4A–CREBH-netwerk dat nauwkeurig regelt hoe de lever cholesterol verpakt en elimineert. Bij vrouwen kantelt het verstoren van dit netwerk de balans naar meer slagader-verstoppende lipoproteïnen, minder beschermend HDL en verslechterde galzuur-gedreven cholesterolverwijdering, factoren die allemaal atherosclerose bevorderen. Door een epigenetische controlehub te benadrukken die tussen de seksen verschilt, suggereert de studie dat toekomstige cholesterolverlagende strategieën—en geneesmiddelen die chromatine-modificerende enzymen targeten—mogelijk verschillend moeten worden afgestemd voor vrouwen en mannen om ongewenste verschuivingen in lipoproteïneprofielen te voorkomen.
Bronvermelding: Chen, L., Kang, Z., Härdfeldt, J. et al. Sex-specific KDM6A-HNF4A-CREBH network controls lipoprotein cholesterol metabolism and atherosclerosis via epigenetic reprograming of hepatocytes. Nat Commun 17, 3945 (2026). https://doi.org/10.1038/s41467-026-70846-w
Trefwoorden: cholesterolmetabolisme, leverepigenetica, lipoproteïnen, geslachtsverschillen, atherosclerose