Clear Sky Science · ja
性差に依存するKDM6A–HNF4A–CREBHネットワークは肝細胞のエピジェネティック再プログラミングを介してリポタンパク質コレステロール代謝と動脈硬化を制御する
心血管の健康にとってこの研究が重要な理由
心臓発作や脳卒中は、多くの場合、肝臓のコレステロール処理のゆっくりとした変化から始まります。男性と女性はコレステロール値や動脈閉塞のリスクに違いがあることが知られていますが、その基盤にある理由はまだ解明途上です。本研究は、特に女性で血中脂質をより健全な範囲に保つのに寄与する肝細胞の性別に連動した制御システムを明らかにします。このシステムを理解することは、高コレステロールや動脈硬化に対するより個別化された治療の道を示す可能性があります。
X染色体上の肝臓スイッチ
本研究の中心にあるのは、X染色体上の遺伝子から作られるKDM6Aというタンパク質です。KDM6Aはコレステロールを運ぶわけではなく、細胞核内でどの遺伝子をオン/オフにするかを決める仕組みの一部として働きます。女性では通常ひとつのXが不活性化されますが、KDM6Aはその不活性化を免れることがあり、その活性は男女で異なり得ます。著者らは、この違いが男女でコレステロールや血中の脂質運搬粒子(リポタンパク質)の取り扱いが異なる理由の一端を説明するかどうかを問いました。
スイッチを落とすと何が起きるか
KDM6Aの役割を検証するため、研究チームはヒト肝細胞株および肝細胞(肝実質細胞)にのみKDM6A欠損を導入したマウスでその量を減らしました。女性ドナー由来の肝細胞では、KDM6Aを抑えるとリポタンパク質の構築・代謝を支える遺伝子群、特に保護的な高比重リポタンパク質(HDL)を支える遺伝子の活性が強く低下しました。同じ操作を男性由来の細胞で行うと別の遺伝子群に影響し、コレステロール経路に焦点は当たりませんでした。雌のマウスでは、肝臓のKDM6A欠失によりより「アテローム形成的」なリポタンパク質パターンが現れました:超低比重リポタンパク質(VLDL)粒子が異常にコレステロールを多く含み、HDLレベルは低下し、特に高脂肪・高コレステロール食と動脈硬化を促す遺伝学的操作を加えると、主幹動脈への脂質蓄積が増大しました。
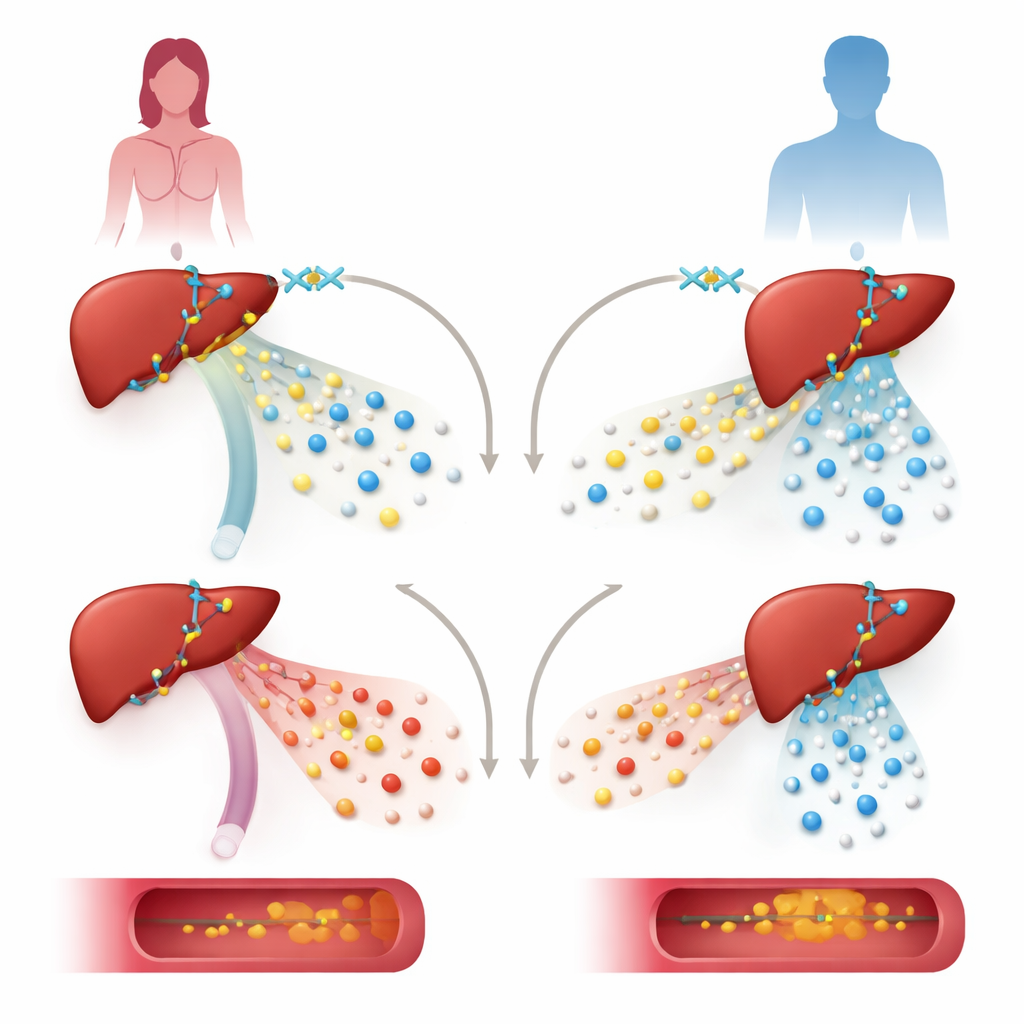
肝臓の遺伝子制御ネットワークはどう書き換えられるか
さらに踏み込み、研究者らはKDM6AがDNA上でどのように位置し他の調節因子と相互作用するかをマッピングしました。彼らはKDM6Aが肝臓の主要な転写因子であるHNF4Aと協調し、ApoA1、ApoM、ApoHなど多くのリポタンパク質・コレステロール関連遺伝子の近傍の制御領域に結合していることを見出しました。ここでKDM6Aは、特定のヒストン修飾を消すという既知の化学的“消しゴム”機能を主に通じて働くのではなく、むしろ足場(スキャフォールド)のように振る舞います。HNF4AおよびMLL3/4と呼ばれる酵素複合体と共に、遺伝子活性を促す開いたクロマチン状態を形成するのを助けます。KDM6Aを失うとこれらの活性化マークが弱まり、通常KDM6Aが消去する抑制的マークが大きく増えないことから、酵素的な役割というより構造的・非酵素的な役割を示唆します。
スイッチをコレステロール産生に結びつける第三の因子
本研究は第三の因子であるCREBHも同定しました。CREBHは肝ストレス応答性のタンパク質で、トリグリセリドやコレステロールの取り扱いを直接亢進する遺伝子を活性化します。ゲノムワイドな結合マップにより、KDM6Aが失われるとCREBHの多くの標的遺伝子への結合が弱まることが示されました。これらの標的には胆汁酸産生、コレステロール除去、HDL形成に関わる遺伝子が含まれます。肝臓でKDM6Aを欠く雌マウスでは、これらの遺伝子の発現が低下し、胆汁酸が肝臓と血中に蓄積し、VLDLは肝臓からコレステロールに富む一方で比較的トリグリセリドに乏しい粒子として放出されました。この偏った産生とHDL合成遺伝子の低下が組み合わさって、動脈壁へのコレステロール沈着を増大させたのです。
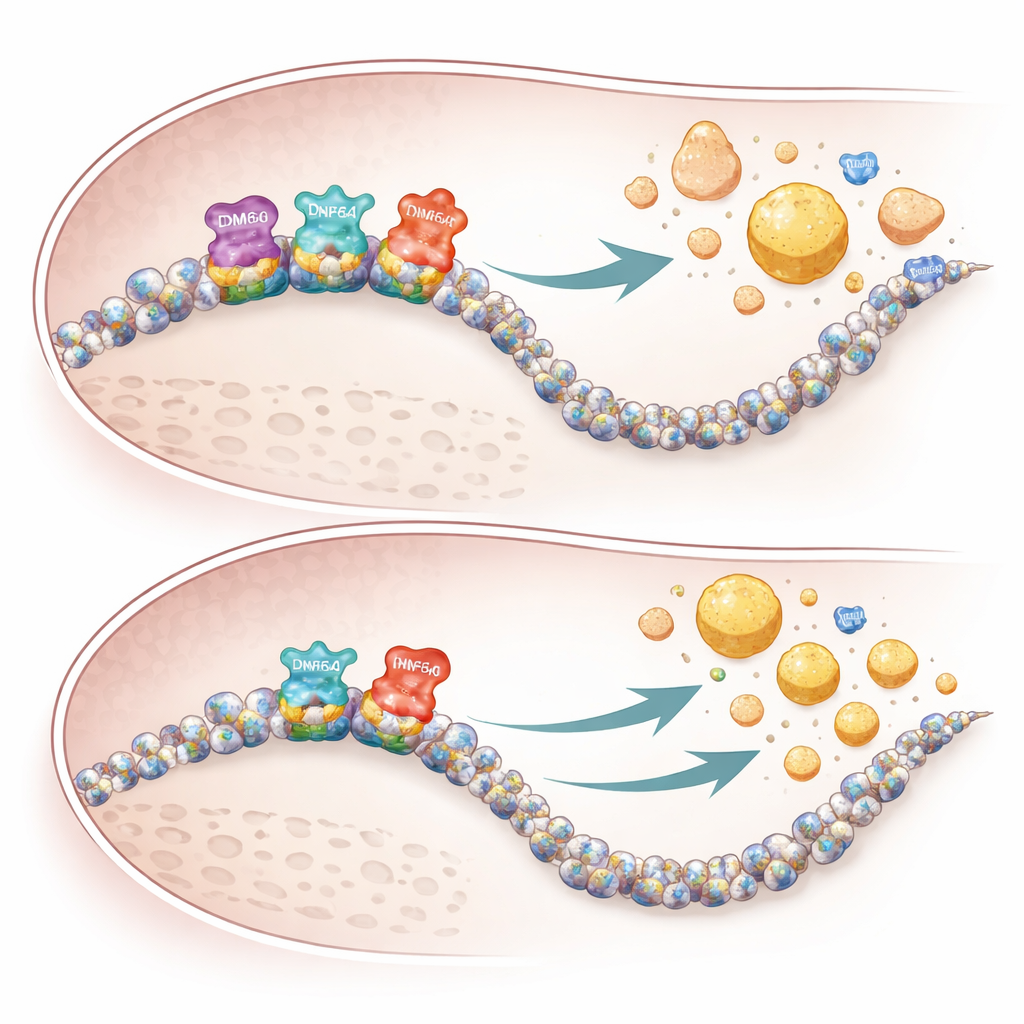
なぜ女性がより影響を受けるのか
性差特異的な所見は、遺伝要因と代替システムの両方を反映しているようです。KDM6AはX連鎖であり女性組織でより強く発現するため、その喪失は女性でより大きな影響を及ぼします。男性はY染色体上に関連遺伝子KDM6Cを持ち、肝細胞では部分的に補償することができます。雄マウスでは肝細胞でKDM6Aを欠失しても遺伝子活性やリポタンパク質パターンにほとんど変化が見られませんでしたが、雌で同様の操作を行うとコレステロール経路の広範な再プログラミングと血中脂質の顕著な変化が起きました。大規模なヒト遺伝データもこれらのパターンを反映しており、稀なKDM6A変異は有益なApoA1の低下とアテローム形成性のApoBの上昇と関連していました。
将来の治療にとっての意味
総じて、本研究は肝臓がコレステロールをパッケージングし除去する方法を微調整する性差に依存するKDM6A–HNF4A–CREBHネットワークを明らかにしました。女性ではこのネットワークを破壊すると、動脈を詰まらせやすいリポタンパク質への傾斜、保護的なHDLの減少、胆汁酸を介したコレステロール排除の障害が生じ、いずれも動脈硬化を促進します。性差のあるエピジェネティック制御ハブを強調したことで、将来のコレステロール低下戦略やクロマチン修飾酵素を標的とする薬剤は、望ましくないリポタンパク質プロファイルの変化を避けるために女性と男性で異なる配慮が必要になる可能性が示唆されます。
引用: Chen, L., Kang, Z., Härdfeldt, J. et al. Sex-specific KDM6A-HNF4A-CREBH network controls lipoprotein cholesterol metabolism and atherosclerosis via epigenetic reprograming of hepatocytes. Nat Commun 17, 3945 (2026). https://doi.org/10.1038/s41467-026-70846-w
キーワード: コレステロール代謝, 肝臓のエピジェネティクス, リポタンパク質, 性差, 動脈硬化