Clear Sky Science · pl
Sieć KDM6A–HNF4A–CREBH zależna od płci kontroluje metabolizm cholesterolu w lipoproteinach i miażdżycę poprzez epigenetyczne przeprogramowanie hepatocytów
Dlaczego te badania są ważne dla zdrowia serca
Zawały serca i udary często zaczynają się od powolnych zmian w tym, jak wątroba gospodaruje cholesterolem. Wiadomo, że mężczyźni i kobiety różnią się poziomami cholesterolu oraz ryzykiem zatkania tętnic, ale przyczyny tych różnic są wciąż badane. Niniejsze badanie ujawnia powiązany z płcią system regulacji w komórkach wątroby, który pomaga utrzymać lipidy krwi w zdrowszym zakresie, szczególnie u samic. Zrozumienie tego systemu może wskazać drogę do bardziej spersonalizowanych terapii przeciwko wysokiemu cholesterolu i miażdżycy.
Przełącznik w wątrobie na chromosomie X
W centrum tej pracy znajduje się białko o nazwie KDM6A, kodowane przez gen na chromosomie X. KDM6A nie przenosi cholesterolu; działa w jądrze komórkowym jako część aparatu decydującego, które geny są włączane lub wyłączane. Ponieważ leży na chromosomie X i może unikać zwykłej inaktywacji jednego X u samic, jego aktywność może różnić się między kobietami a mężczyznami. Autorzy zastanawiali się, czy ta różnica pomaga wyjaśnić, dlaczego obie płci różnie radzą sobie z cholesterolem i lipoproteinami — cząstkami przenoszącymi tłuszcze we krwi.
Co się dzieje, gdy przełącznik zostaje przyciszony
Aby przetestować rolę KDM6A, zespół obniżył jego poziomy w ludzkich liniach komórek wątrobowych oraz u myszy zaprojektowanych tak, by brakowało KDM6A tylko w hepatocytach, głównych komórkach wątroby. W komórkach wątrobowych pochodzących od dawczyni, przyciszenie KDM6A silnie obniżyło aktywność genów budujących i przetwarzających lipoproteiny, w tym genów wspierających ochronne lipoproteiny o wysokiej gęstości (HDL). Ta sama manipulacja w komórkach pochodzenia męskiego wpłynęła na inny zestaw genów i nie koncentrowała się na szlakach cholesterolowych. U samic myszy utrata KDM6A w wątrobie prowadziła do bardziej „aterogennego” profilu lipoprotein: cząsteczki bardzo niskiej gęstości (VLDL) stawały się nietypowo bogate w cholesterol, poziom HDL spadał, a odkładanie tłuszczu w tętnicy głównej wzrastało, zwłaszcza gdy zwierzęta były karmione dietą wysokotłuszczową i wysokocholesterolową oraz poddane dodatkowym zabiegom sprzyjającym miażdżycy.
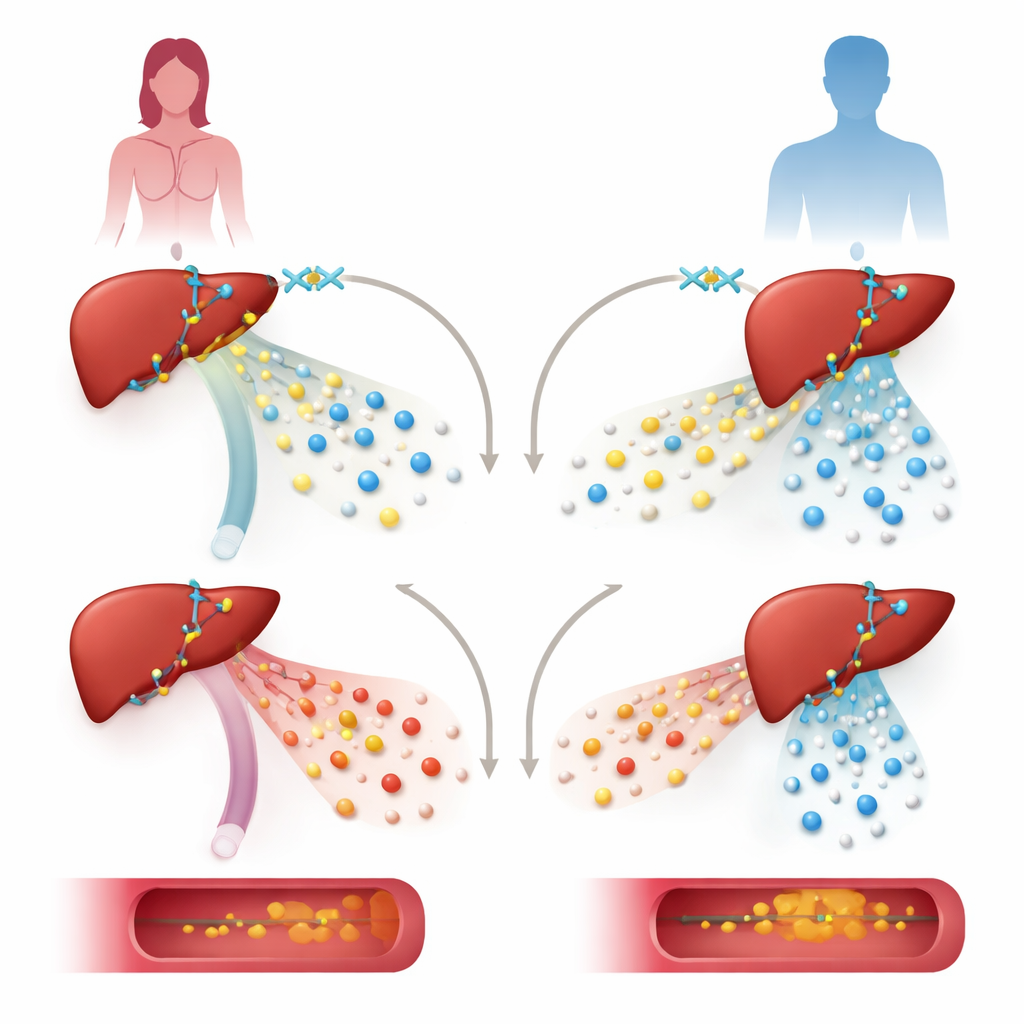
Jak sieć kontrolna w wątrobie zostaje przebudowana
Dziejąc głębiej, badacze zmapowali, gdzie KDM6A wiąże się z DNA i jak współdziała z innymi regulatorami. Odkryli, że KDM6A współpracuje z kluczowym wątrobowym czynnikiem transkrypcyjnym HNF4A w regionach kontrolnych przy wielu genach odpowiedzialnych za lipoproteiny i cholesterol, takich jak te kodujące ApoA1, ApoM i ApoH. Zamiast działać głównie przez znaną funkcję „wymazywania” określonego znacznika histonowego, KDM6A w tym kontekście zachowuje się bardziej jak rusztowanie. Razem z HNF4A i kompleksem enzymatycznym MLL3/4 pomaga tworzyć otwartą, aktywną chromatynę — luźniej upakowaną strukturę DNA i białek — oznaczoną pewnymi chemicznymi flagami sprzyjającymi aktywności genów. Usunięcie KDM6A osłabiło te aktywne markery, nie powodując znaczącego wzrostu represyjnych znaków, które zwykle są jego celem do „wymazywania”, co sugeruje rolę strukturalną niezwiązaną z aktywnością enzymatyczną.
Trzeci gracz łączy przełącznik z wydzielaniem cholesterolu
Badanie identyfikuje także trzeci czynnik, CREBH — wątrobowe białko reagujące na stres, które bezpośrednio wzmacnia geny kontrolujące obróbkę trójglicerydów i cholesterolu. Na podstawie map wiązania w całym genomie autorzy pokazują, że gdy KDM6A znika, CREBH słabiej wiąże się z wieloma swoimi docelowymi genami związanymi z produkcją kwasów żółciowych, usuwaniem cholesterolu i tworzeniem HDL. U samic myszy pozbawionych wątrobowego KDM6A te geny były mniej aktywne, kwasy żółciowe gromadziły się w wątrobie i krwi, a cząsteczki VLDL opuszczały wątrobę nietypowo wzbogacone w cholesterol, lecz stosunkowo ubogie w trójglicerydy. To przesunięcie składu, w połączeniu z redukcją genów budujących HDL, stworzyło warunki sprzyjające większemu odkładaniu cholesterolu w ścianach tętnic.
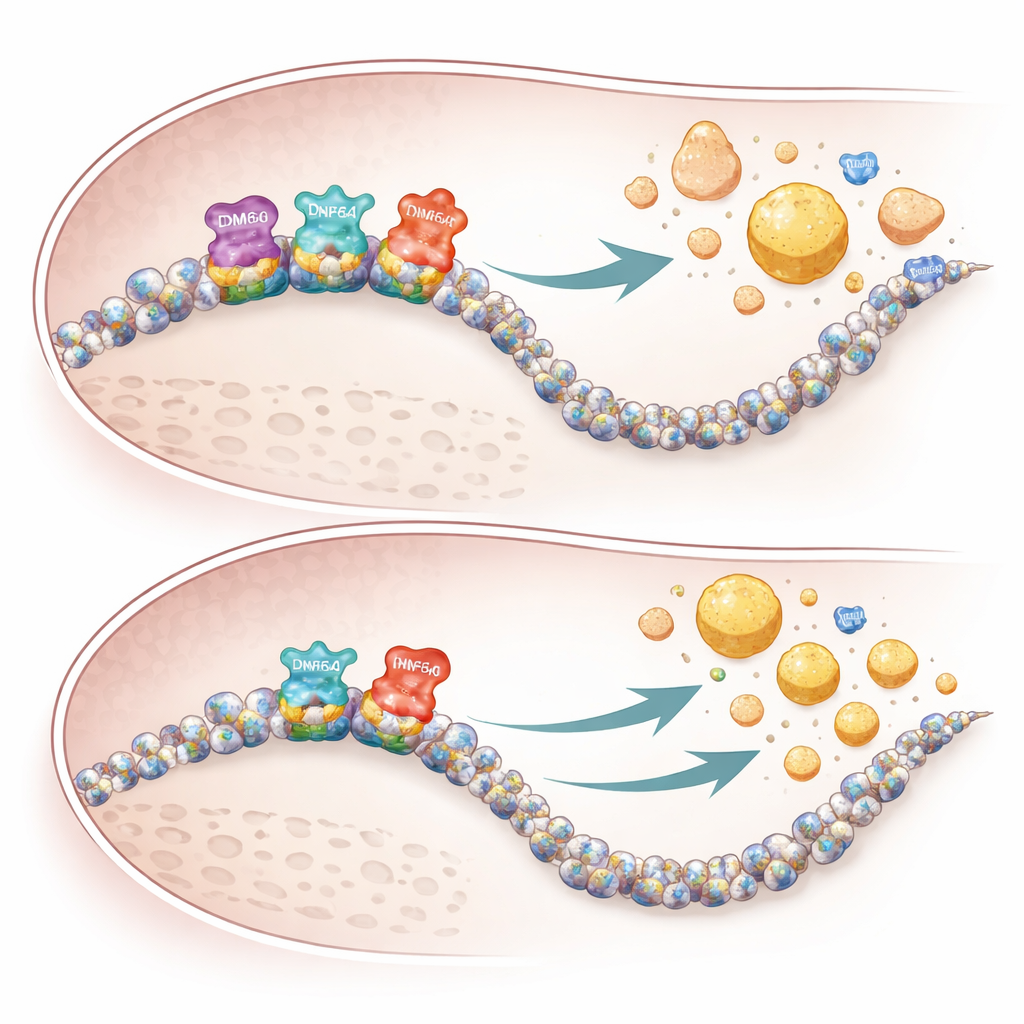
Dlaczego kobiety są bardziej dotknięte
Specyfika związana z płcią wydaje się odzwierciedlać zarówno genetykę, jak i systemy zapasowe. Ponieważ KDM6A jest związany z chromosomem X i silniej eksprymowany w tkankach żeńskich, jego utrata ma większy wpływ u samic. Samce noszą pokrewny gen na chromosomie Y, zwany KDM6C, który może częściowo kompensować w komórkach wątroby. U samców myszy usunięcie KDM6A w hepatocytach ledwie zmieniało aktywność genów czy profile lipoprotein, podczas gdy podobne manipulacje u samic powodowały szerokie przeprogramowanie szlaków cholesterolowych i uderzające zmiany w lipidach krwi. Dane genetyczne ludzi z dużych baz potwierdziły te wzorce: rzadkie warianty KDM6A wiązały się z niższymi poziomami korzystnego ApoA1 i wyższymi poziomami aterogennego ApoB.
Co to oznacza dla przyszłych terapii
Podsumowując, praca ujawnia związany z płcią węzeł regulacyjny KDM6A–HNF4A–CREBH, który precyzuje, jak wątroba pakuje i usuwa cholesterol. U samic zakłócenie tej sieci przesuwa równowagę w kierunku bardziej zatykających tętnice lipoprotein, mniejszej ilości ochronnego HDL i upośledzonego usuwania cholesterolu przez kwasy żółciowe — wszystkie te zmiany sprzyjają miażdżycy. Wskazując na epigenetyczne centrum kontroli różniące się między płciami, badanie sugeruje, że przyszłe strategie obniżania cholesterolu — oraz leki celujące w enzymy modyfikujące chromatynę — mogą wymagać innego dopasowania dla kobiet i mężczyzn, aby uniknąć niepożądanych przesunięć w profilach lipoproteinowych.
Cytowanie: Chen, L., Kang, Z., Härdfeldt, J. et al. Sex-specific KDM6A-HNF4A-CREBH network controls lipoprotein cholesterol metabolism and atherosclerosis via epigenetic reprograming of hepatocytes. Nat Commun 17, 3945 (2026). https://doi.org/10.1038/s41467-026-70846-w
Słowa kluczowe: metabolizm cholesterolu, epigenetyka wątroby, lipoproteiny, różnice między płciami, miażdżyca