Clear Sky Science · ar
شبكة KDM6A-HNF4A-CREBH المرتبطة بالجنس تتحكم في أيض كوليسترول البروتين الدهني وتصلب الشرايين عبر إعادة برمجة وبائية للخلايا الكبدية
لماذا تهم هذه الدراسة صحة القلب
عادة ما تبدأ النوبات القلبية والسكتات بتغيرات بطيئة في كيفية تعامل الكبد مع الكوليسترول. من المعروف أن الرجال والنساء يختلفون في مستويات الكوليسترول وخطر انسداد الشرايين، لكن الأسباب الأساسية لا تزال قيد الاكتشاف. تكشف هذه الدراسة عن نظام ضابط مرتبط بالجنس في خلايا الكبد يساعد على إبقاء دهون الدم ضمن نطاق أكثر صحة، لا سيما لدى الإناث. وفهم هذا النظام قد يفتح طريقًا لعلاجات أكثر تخصيصًا لفرط الكوليسترول وتصلب الشرايين.
مفتاح كبدي على كروموسوم X
المحور المحوري لهذا العمل هو بروتين يسمى KDM6A، ينتج عن جين على كروموسوم X. لا يحمل KDM6A الكوليسترول بنفسه؛ بل يعمل في نواة الخلية كجزء من الآليات التي تقرر أي الجينات تُفعَّل أو تُوقف. وبما أنه موجود على كروموسوم X ويمكن أن يهرب من كبت أحد كروموسومات X في الإناث، فقد تختلف نشاطاته بين الإناث والذكور. تساءل المؤلفون عما إذا كان هذا الاختلاف يساهم في تفسير الفروق بين الجنسين في طريقة تعاملهما مع الكوليسترول والبروتينات الدهنية — الجسيمات الحاملة للدهون في الدم.
ماذا يحدث عند إيقاف المفتاح
لاختبار دور KDM6A خفّض الفريق مستوياته في خطوط خلايا كبدية بشرية وفي فئران مهندسة لتفتقر إلى KDM6A في الخلايا الكبدية فقط. في خلايا كبدية من متبرعة أنثى، أدى خفض KDM6A إلى انخفاض قوي في نشاط جينات بناء ومعالجة البروتينات الدهنية، بما في ذلك جينات تدعم البروتين الدهني عالي الكثافة (HDL) الواقي. نفس التلاعب في خلايا مشتقة من ذكر أثر على مجموعة مختلفة من الجينات ولم يركز على مسارات الكوليسترول. في الفئران الإناث، أدى فقدان KDM6A في الكبد إلى نمط بروتينات دهنية أكثر «مسببة للتصلب»: أصبحت جزيئات البروتين الدهني منخفض الكثافة جدًا (VLDL) غنية بشكل غير اعتيادي بالكوليسترول، انخفضت مستويات HDL، وتزايدت تراكمات الدهن في الشريان الرئيسي، خاصة عندما تعرّضت الحيوانات لنظام غذائي عالي الدهون والكوليسترول وأداة جينية محفزة للتصلب.
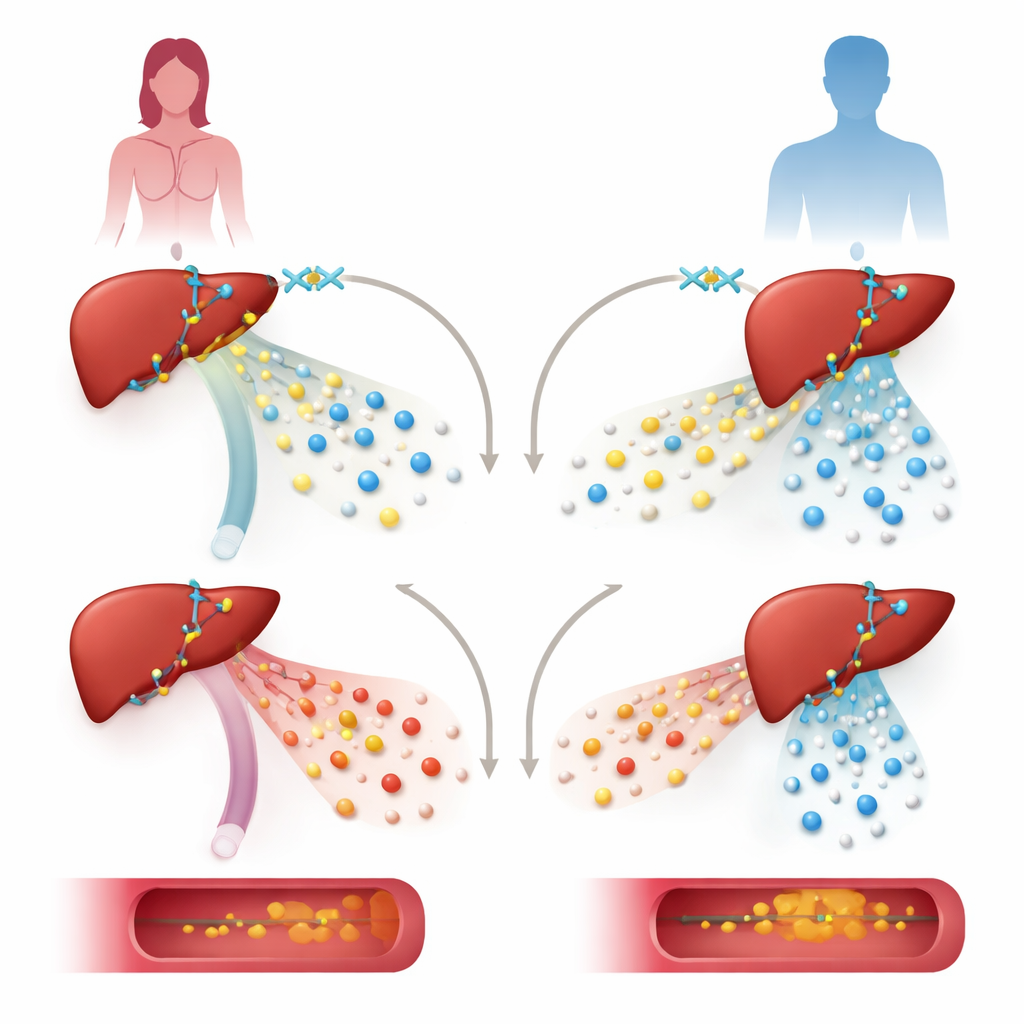
كيف تُعاد تعبئة شبكة التحكم الجيني الكبدية
بالتعمق أكثر، رصد الباحثون مواضع KDM6A على الحمض النووي وتداخلاته مع عوامل تنظيمية أخرى. وجدوا أن KDM6A يتعاون مع عامل نسخ كبدي رئيسي، HNF4A، في مناطق تحكم قريبة من العديد من جينات البروتينات الدهنية والكوليسترول، مثل تلك التي تصنع بروتينات ApoA1 وApoM وApoH. بدلًا من العمل أساسًا عبر وظيفة «الممحاة» الكيميائية المعروفة له على علامة هستونية محددة، يتصرف KDM6A هنا أكثر كسقالة. مع HNF4A ومجمع إنزيمي يُدعى MLL3/4، يساعد في تكوين كروماتين منفتح ونشط — تركيب الحمض النووي والبروتين الأقل تماسكًا — والمُعلَّم بعلامات كيميائية تفضّل نشاط الجينات. أدى إزالة KDM6A إلى إضعاف هذه العلامات النشطة دون زيادة كبيرة في العلامات الكابحة التي يمحوها عادة، مما يشير إلى دور بنيوي غير إنزيمي.
لاعب ثالث يربط المفتاح بمخرجات الكوليسترول
تحدد الدراسة أيضًا عاملًا ثالثًا، CREBH، وهو بروتين مستجيب لإجهاد الكبد يعزز مباشرة جينات تحكم في معالجة الدهون الثلاثية والكوليسترول. باستخدام خريطات الارتباط على مستوى الجينوم، يظهر المؤلفون أنه عند فقدان KDM6A، يلتصق CREBH بأهدافه المعتادة المشاركة في إنتاج أحماض الصفراء، وإزالة الكوليسترول، وتكوين HDL بدرجة أقل. في إناث الفئران الخاليات من KDM6A الكبدي، كانت هذه الجينات أقل نشاطًا، تراكمت أحماض الصفراء في الكبد والدم، وغادرت جزيئات VLDL الكبد مشبعة بالكوليسترول لكن نسبتها من الدهون الثلاثية كانت منخفضة نسبيًا. هذا الخروج المائل، إلى جانب انخفاض جينات بناء HDL، مهد الطريق لمزيد من ترسيب الكوليسترول في جدران الشرايين.
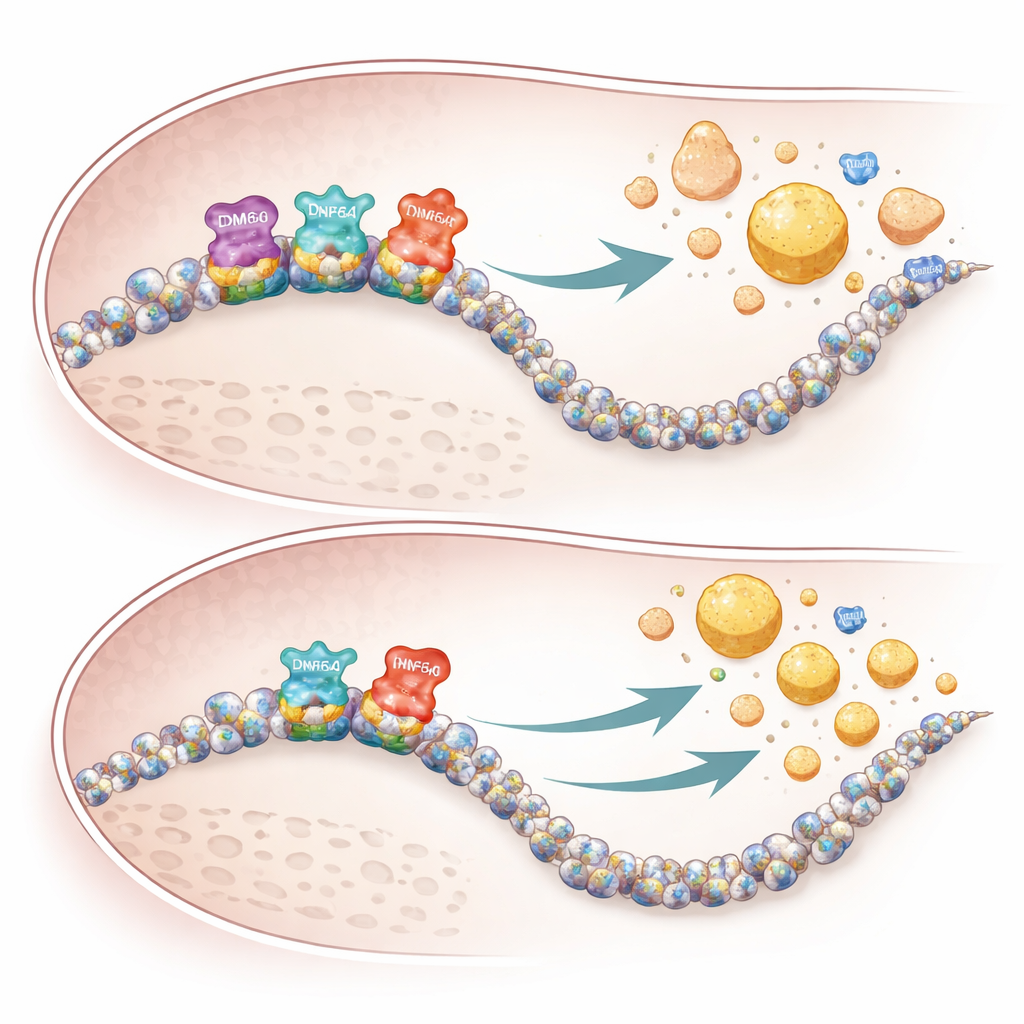
لماذا تتأثر الإناث أكثر
يبدو أن الطبيعة المرتبطة بالجنس للنتائج تعكس كلًا من الجينات وأنظمة التعويض. لأن KDM6A مرتبط بالكروموسوم X ويُعبر عنه بقوة أكبر في أنسجة الإناث، فإن فقدانه له تأثير أكبر في الإناث. يحمل الذكور جينًا ذا صلة على كروموسوم Y يُدعى KDM6C، والذي يمكن أن يعوّض جزئيًا في الخلايا الكبدية. في الفئران الذكور، تغييب KDM6A في الخلايا الكبدية لم يغير نشاط الجينات أو أنماط البروتينات الدهنية إلا بالكاد، بينما تسببت مناورات مماثلة في الإناث في إعادة برمجة واسعة لمسارات الكوليسترول وتغيرات لافتة في دهون الدم. تتوافق بيانات جينية بشرية من قواعد بيانات كبيرة مع هذه الأنماط: رُبطت متغيرات نادرة في KDM6A بمستويات أقل من ApoA1 المفيد ومستويات أعلى من ApoB المسبّب للتصلب في الناس.
ماذا يعني هذا للعلاجات المستقبلية
بشكل عام، تكشف هذه الدراسة عن شبكة مرتبطة بالجنس تضم KDM6A–HNF4A–CREBH تضبط بدقة كيفية تغليف الكبد للكوليسترول وإزالته. في الإناث، يؤدي تعطيل هذه الشبكة إلى ميل التوازن نحو بروتينات دهنية أكثر انسدادًا للشرايين، وانخفاض HDL الواقي، واضطراب في تصريف الكوليسترول عبر أحماض الصفراء، وكلها عوامل تعزز التصلب. من خلال تسليط الضوء على محور تحكم وبائي يختلف بين الجنسين، تقترح الدراسة أن استراتيجيات خفض الكوليسترول المستقبلية — والأدوية التي تستهدف إنزيمات تعديل الكروماتين — قد تحتاج إلى تفصيل مختلف للنساء والرجال لتجنب تحوّلات غير مرغوبة في ملفات البروتينات الدهنية.
الاستشهاد: Chen, L., Kang, Z., Härdfeldt, J. et al. Sex-specific KDM6A-HNF4A-CREBH network controls lipoprotein cholesterol metabolism and atherosclerosis via epigenetic reprograming of hepatocytes. Nat Commun 17, 3945 (2026). https://doi.org/10.1038/s41467-026-70846-w
الكلمات المفتاحية: أيض الكوليسترول, وبائيات الكبد, البروتينات الدهنية, الفروق الجنسية, تصلب الشرايين