Clear Sky Science · fr
Le réseau KDM6A-HNF4A-CREBH spécifique au sexe contrôle le métabolisme du cholestérol des lipoprotéines et l’athérosclérose via le reprogrammation épigénétique des hépatocytes
Pourquoi cette recherche compte pour la santé cardiaque
Les infarctus et les AVC commencent souvent par des modifications progressives de la façon dont le foie gère le cholestérol. On sait que les hommes et les femmes diffèrent par leurs taux de cholestérol et leur risque d’artères obstruées, mais les raisons sous-jacentes restent en grande partie à élucider. Cette étude révèle un système de contrôle lié au sexe dans les cellules hépatiques qui contribue à maintenir les lipides sanguins dans une fourchette plus saine, en particulier chez les femelles. Comprendre ce système pourrait ouvrir la voie à des traitements plus personnalisés contre l’hypercholestérolémie et l’athérosclérose.
Un interrupteur hépatique sur le chromosome X
Au centre de ce travail se trouve une protéine nommée KDM6A, codée par un gène sur le chromosome X. KDM6A ne transporte pas le cholestérol ; elle agit dans le noyau cellulaire comme une composante de la machinerie qui décide quels gènes s’expriment ou non. Parce qu’elle est située sur le chromosome X et peut échapper à l’inactivation habituelle d’un X chez les femelles, son activité peut différer entre femelles et mâles. Les auteurs ont cherché à savoir si cette différence aide à expliquer pourquoi les deux sexes gèrent différemment le cholestérol et les lipoprotéines — les particules qui transportent les graisses dans le sang.
Que se passe-t-il quand l’interrupteur est abaissé
Pour tester le rôle de KDM6A, l’équipe a réduit ses niveaux dans des lignées cellulaires hépatiques humaines et chez des souris génétiquement modifiées pour ne pas exprimer KDM6A uniquement dans les hépatocytes, les principales cellules du foie. Dans des cellules hépatiques provenant d’une donneuse, la diminution de KDM6A a fortement abaissé l’activité des gènes impliqués dans la synthèse et le traitement des lipoprotéines, y compris ceux qui soutiennent les lipoprotéines de haute densité protectrices (HDL). La même manipulation dans des cellules d’origine masculine a affecté un ensemble différent de gènes et ne ciblait pas principalement les voies du cholestérol. Chez les souris femelles, la perte de KDM6A dans le foie a conduit à un profil de lipoprotéines plus « athérogène » : les particules de très basse densité (VLDL) sont devenues inhabituellement riches en cholestérol, les taux de HDL ont chuté et l’accumulation lipidique dans l’artère principale a augmenté, surtout lorsque les animaux ont été soumis à un régime riche en graisses et en cholestérol et à un outil génétique favorisant l’athérosclérose.
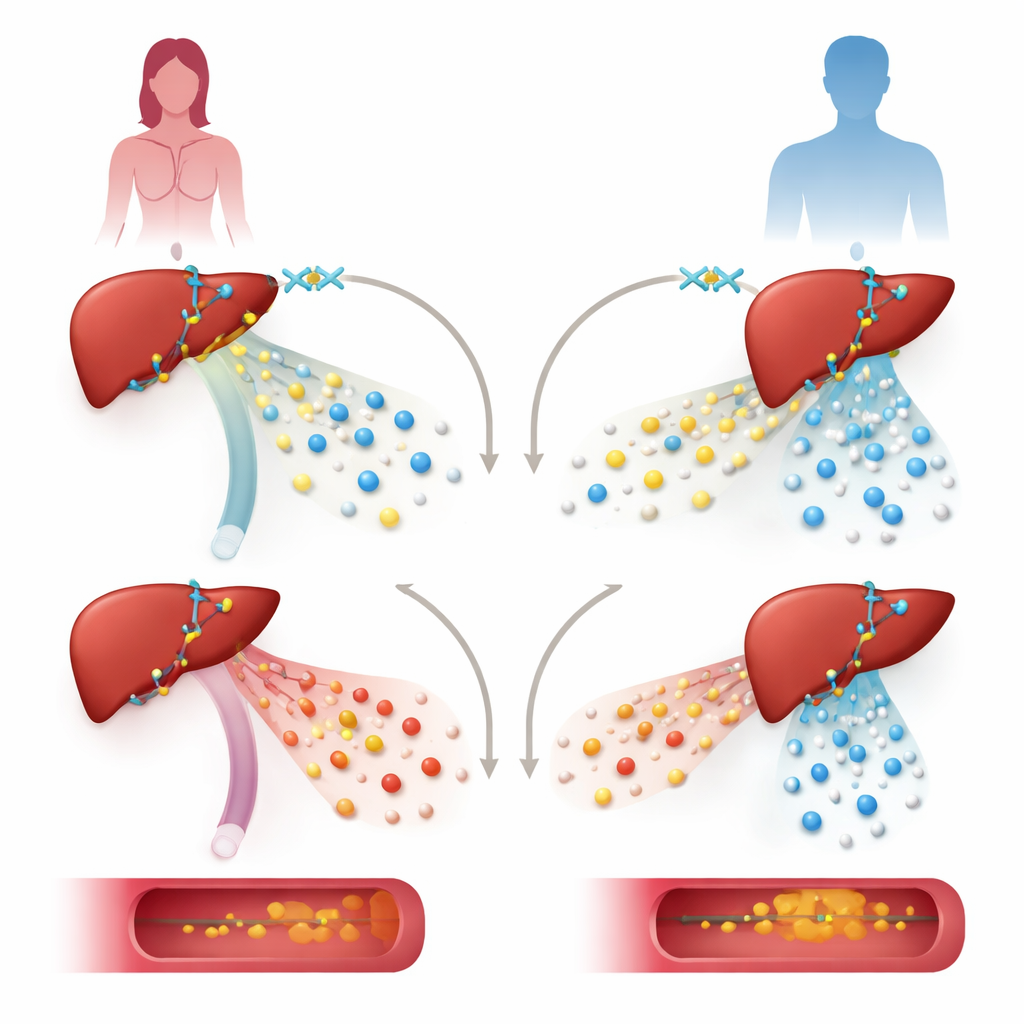
Comment le réseau de contrôle génétique du foie est reconfiguré
En approfondissant, les chercheurs ont cartographié la manière dont KDM6A se positionne sur l’ADN et interagit avec d’autres régulateurs. Ils ont trouvé que KDM6A s’associe à un facteur de transcription hépatique clé, HNF4A, sur des régions de contrôle proches de nombreux gènes des lipoprotéines et du cholestérol, tels que ceux codant les protéines ApoA1, ApoM et ApoH. Plutôt que d’agir principalement via sa fonction enzymatique connue d’« effaceur » d’une marque histone spécifique, KDM6A se comporte ici davantage comme un échafaudage. Avec HNF4A et un complexe enzymatique nommé MLL3/4, elle favorise l’établissement d’une chromatine ouverte et active — une structure ADN-protéine moins condensée — marquée par certains signaux chimiques qui facilitent l’expression des gènes. La suppression de KDM6A a affaibli ces marques actives sans augmenter de manière marquée les marques répressives qu’elle efface habituellement, ce qui suggère un rôle structurel non enzymatique.
Un troisième acteur relie l’interrupteur à la production de cholestérol
L’étude identifie également un troisième facteur, CREBH, une protéine hépatique réactive au stress qui stimule directement des gènes gouvernant le métabolisme des triglycérides et du cholestérol. À l’aide de cartes de liaison à l’échelle du génome, les auteurs montrent que lorsque KDM6A est perdu, CREBH se lie moins fortement à beaucoup de ses gènes cibles habituels impliqués dans la production d’acides biliaires, l’élimination du cholestérol et la formation du HDL. Chez les souris femelles dépourvues de KDM6A hépatique, ces gènes étaient moins actifs, les acides biliaires s’accumulaient dans le foie et le sang, et les particules de VLDL quittaient le foie enrichies de manière inhabituelle en cholestérol mais relativement pauvres en triglycérides. Cette production déséquilibrée, combinée à une moindre expression des gènes constructeurs de HDL, a favorisé une plus grande accumulation de cholestérol dans les parois artérielles.
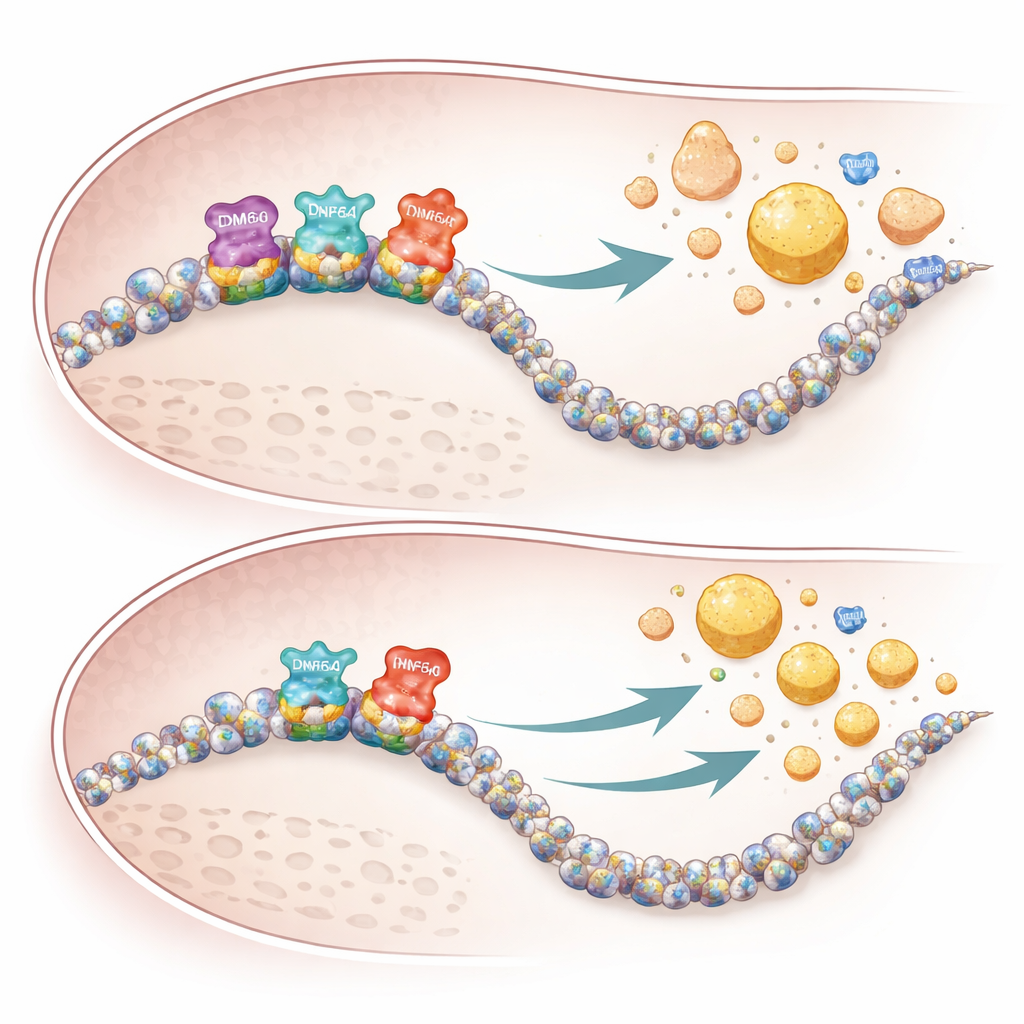
Pourquoi les femelles sont davantage affectées
Le caractère spécifique au sexe des résultats semble refléter à la fois la génétique et les systèmes de secours. Parce que KDM6A est liée au chromosome X et s’exprime plus fortement dans les tissus féminins, sa perte a un impact plus important chez les femelles. Les mâles portent un gène apparenté sur le chromosome Y, appelé KDM6C, qui peut compenser partiellement dans les cellules hépatiques. Chez les souris mâles, la suppression de KDM6A dans les hépatocytes a à peine modifié l’activité des gènes ou les profils de lipoprotéines, tandis que des manipulations similaires chez les femelles ont provoqué une reprogrammation étendue des voies du cholestérol et des changements marqués des lipides sanguins. Les données génétiques humaines provenant de grandes bases ont fait écho à ces schémas : des variants rares de KDM6A ont été associés à des niveaux plus faibles d’ApoA1 bénéfique et à des niveaux plus élevés d’ApoB athérogène chez des personnes.
Quelles implications pour les traitements futurs
Dans l’ensemble, ce travail met en lumière un réseau lié au sexe KDM6A–HNF4A–CREBH qui ajuste la façon dont le foie emballe et élimine le cholestérol. Chez les femelles, la perturbation de ce réseau incline l’équilibre vers des lipoprotéines plus obstruantes pour les artères, moins de HDL protecteur et une élimination du cholestérol via les acides biliaires altérée, autant de facteurs qui favorisent l’athérosclérose. En soulignant un centre de contrôle épigénétique qui diffère selon le sexe, l’étude suggère que les futures stratégies de réduction du cholestérol — et les médicaments ciblant les enzymes modifiant la chromatine — pourraient devoir être adaptées différemment pour les femmes et les hommes afin d’éviter des changements indésirables des profils de lipoprotéines.
Citation: Chen, L., Kang, Z., Härdfeldt, J. et al. Sex-specific KDM6A-HNF4A-CREBH network controls lipoprotein cholesterol metabolism and atherosclerosis via epigenetic reprograming of hepatocytes. Nat Commun 17, 3945 (2026). https://doi.org/10.1038/s41467-026-70846-w
Mots-clés: métabolisme du cholestérol, épi-génétique hépatique, lipoprotéines, différences sexuelles, athérosclérose