Clear Sky Science · it
La rete KDM6A-HNF4A-CREBH specifica per sesso controlla il metabolismo del colesterolo nelle lipoproteine e l’aterosclerosi tramite la riprogrammazione epigenetica degli epatociti
Perché questa ricerca è importante per la salute del cuore
Infarti e ictus spesso hanno inizio con cambiamenti graduali nel modo in cui il fegato gestisce il colesterolo. È noto che uomini e donne differiscono nei livelli di colesterolo e nel rischio di arterie occluse, ma le ragioni di fondo sono ancora in fase di scoperta. Questo studio rivela un sistema di controllo legato al sesso nelle cellule epatiche che aiuta a mantenere i grassi nel sangue in un intervallo più salutare, soprattutto nelle femmine. Comprendere questo sistema può indicare strade per terapie più personalizzate contro l’ipercolesterolemia e l’aterosclerosi.
Un interruttore epatico sul cromosoma X
Al centro di questo lavoro c’è una proteina chiamata KDM6A, prodotta da un gene sul cromosoma X. KDM6A non trasporta colesterolo; agisce invece nel nucleo cellulare come parte della macchina che decide quali geni vengono attivati o spenti. Poiché si trova sul cromosoma X e può sfuggire alla classica inattivazione di un X nelle femmine, la sua attività può differire tra femmine e maschi. Gli autori si sono chiesti se questa differenza contribuisca a spiegare perché i due sessi gestiscono colesterolo e lipoproteine—le particelle che trasportano i grassi nel sangue—in modi diversi.
Cosa succede quando l’interruttore viene abbassato
Per testare il ruolo di KDM6A, il team ha ridotto i suoi livelli in linee cellulari epatiche umane e in topi ingegnerizzati privi di KDM6A solo negli epatociti, le principali cellule del fegato. In cellule di fegato da una donatrice femminile, l’abbassamento di KDM6A ha fortemente ridotto l’attività di geni che costruiscono e processano le lipoproteine, inclusi geni che supportano la lipoproteina ad alta densità protettiva (HDL). La stessa manipolazione in cellule di origine maschile ha interessato un diverso insieme di geni e non si è concentrata sulle vie del colesterolo. Nelle femmine murine, la perdita di KDM6A nel fegato ha portato a un profilo di lipoproteine più “aterogenico”: le particelle a bassissima densità (VLDL) sono diventate insolitamente ricche di colesterolo, i livelli di HDL sono diminuiti e l’accumulo di grasso nella principale arteria è aumentato, specialmente quando gli animali sono stati sottoposti a una dieta ricca di grassi e colesterolo e a uno stimolo genetico volto a promuovere l’aterosclerosi.
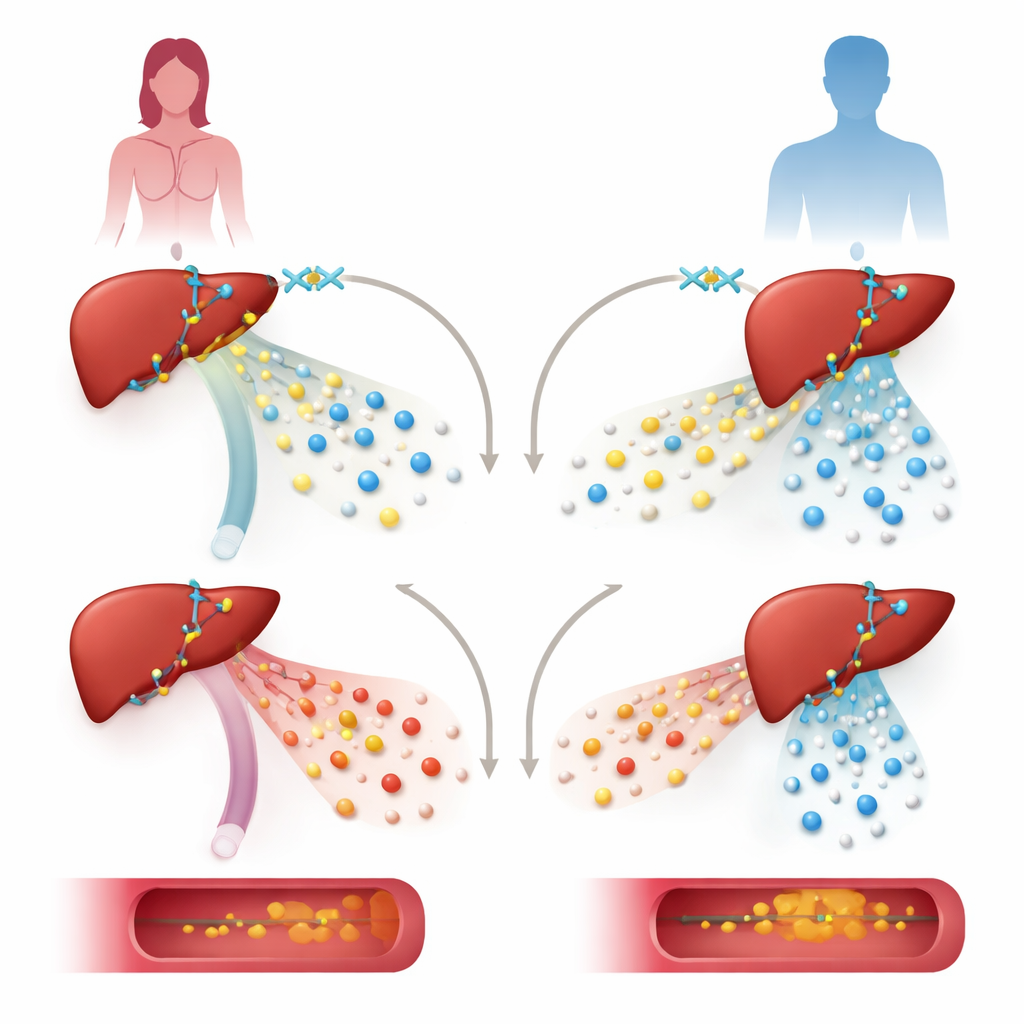
Come viene riorganizzata la rete di controllo genico epatica
Approfondendo, i ricercatori hanno mappato come KDM6A si lega al DNA e interagisce con altri regolatori. Hanno scoperto che KDM6A collabora con un importante fattore di trascrizione epatico, HNF4A, in regioni di controllo vicino a molti geni delle lipoproteine e del colesterolo, come quelli che codificano le proteine ApoA1, ApoM e ApoH. Piuttosto che agire principalmente attraverso la sua nota funzione chimica di “cancellatore” su uno specifico segnale degli istoni, KDM6A qui si comporta più come uno scaffold. Insieme a HNF4A e a un complesso enzimatico chiamato MLL3/4, contribuisce a creare una cromatina aperta e attiva—una struttura DNA-proteina meno compatta—segnalata da flag chimici che favoriscono l’attività genica. Rimuovere KDM6A indeboliva questi marchi attivi senza aumentare molto i marchi repressivi che normalmente cancella, suggerendo un ruolo strutturale non enzimatico.
Un terzo attore collega l’interruttore alla produzione di colesterolo
Lo studio identifica anche un terzo fattore, CREBH, una proteina epatica indotta dallo stress che potenzia direttamente i geni che regolano il metabolismo dei trigliceridi e del colesterolo. Usando mappe di legame genomiche, gli autori mostrano che quando KDM6A viene perso, CREBH si lega meno saldamente a molti dei suoi bersagli abituali coinvolti nella produzione di acidi biliari, nello smaltimento del colesterolo e nella formazione di HDL. Nelle femmine murine prive di KDM6A epatica, questi geni risultavano meno attivi, gli acidi biliari si accumulavano nel fegato e nel sangue, e le particelle VLDL che uscivano dal fegato erano insolitamente ricche di colesterolo ma relativamente povere di trigliceridi. Questa produzione sbilanciata, combinata con la riduzione dei geni che costruiscono HDL, ha creato le condizioni per un maggiore deposito di colesterolo nelle pareti arteriose.
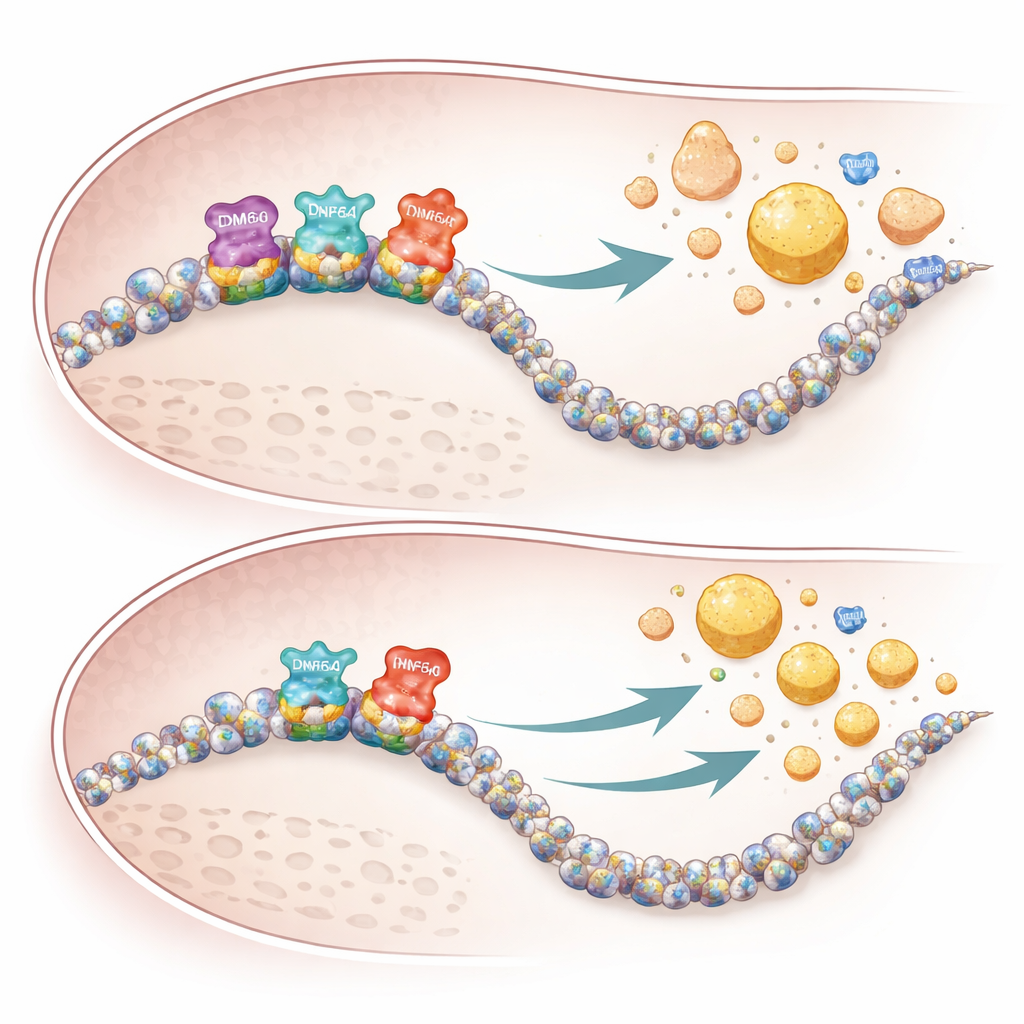
Perché le femmine sono maggiormente colpite
La natura specifica per sesso dei risultati sembra riflettere sia la genetica sia sistemi di compensazione. Poiché KDM6A è legato all’X ed è più fortemente espresso nei tessuti femminili, la sua perdita ha un impatto maggiore nelle femmine. I maschi portano un gene correlato sul cromosoma Y, chiamato KDM6C, che può compensare parzialmente nelle cellule del fegato. Nei topi maschi, la delezione di KDM6A negli epatociti ha modificato appena l’attività genica o i profili di lipoproteine, mentre manipolazioni simili nelle femmine hanno causato una ampia riprogrammazione delle vie del colesterolo e cambiamenti evidenti nei lipidi ematici. Dati genetici umani tratti da grandi banche dati riflettono questi schemi: varianti rare di KDM6A sono state associate a livelli più bassi della benefica ApoA1 e a livelli più alti della aterogenica ApoB nelle persone.
Cosa significa per i trattamenti futuri
Nel complesso, il lavoro rivela una rete legata al sesso KDM6A–HNF4A–CREBH che regola finemente il modo in cui il fegato imballa e rimuove il colesterolo. Nelle femmine, la disgregazione di questa rete sposta l’equilibrio verso lipoproteine più occludenti per le arterie, meno HDL protettivo e un’eliminazione del colesterolo mediata dagli acidi biliari compromessa, tutti fattori che favoriscono l’aterosclerosi. Evidenziando un hub di controllo epigenetico che differisce tra i sessi, lo studio suggerisce che le strategie future per abbassare il colesterolo—e i farmaci che prendono di mira gli enzimi che modificano la cromatina—potrebbero dover essere adattate in modo diverso per donne e uomini per evitare spostamenti indesiderati nei profili delle lipoproteine.
Citazione: Chen, L., Kang, Z., Härdfeldt, J. et al. Sex-specific KDM6A-HNF4A-CREBH network controls lipoprotein cholesterol metabolism and atherosclerosis via epigenetic reprograming of hepatocytes. Nat Commun 17, 3945 (2026). https://doi.org/10.1038/s41467-026-70846-w
Parole chiave: metabolismo del colesterolo, epigenetica epatica, lipoproteine, differenze di sesso, aterosclerosi