Clear Sky Science · he
רשת KDM6A-HNF4A-CREBH תלויה במין ושולטת במטבוליזם של כולסטרול בליפופרוטאינים ובאטורוסקלרוזיס דרך תכנות אפיגנטי של תאי כבד
מדוע המחקר הזה חשוב לבריאות הלב
התקפי לב ושבצים בדרך כלל מתחילים בשינויים איטיים באופן שבו הכבד מטפל בכולסטרול. ידוע כי גברים ונשים שונים ברמות הכולסטרול שלהם ובסיכון לסתימות בעורקים, אך הסיבות הבסיסיות עדיין מתגלות. מחקר זה חושף מערכת בקרה מקושרת למין בתאי הכבד שעוזרת לשמור על שומנים בדם בטווח בריא יותר, במיוחד בנקבות. הבנת המערכת הזו עשויה להצביע על דרכים לטיפולים מותאמים אישית ביתר לחץ דם ושעמום שומנים בכלי הדם.
מפסל בכבד על כרומוזום X
במרכז העבודה נמצא חלבון שנקרא KDM6A, המיוצר מגן על כרומוזום X. KDM6A לא נושא כולסטרול בעצמו; במקום זאת הוא פועל בגרעין התא כחלק מהמכונה שמכריעה אילו גנים פעילים או כבויים. מכיוון שהוא ממוקם על כרומוזום X ויכול להימנע מדיכוי ההשבתה הרגיל של אחד ה־X בנקבות, פעילותו יכולה להשתנות בין נשים לגברים. החוקרים בחנו האם ההבדל הזה מסביר מדוע שני המינים מטפלים בכולסטרול וליפופרוטאינים — חלקיקי נשיאת שומן בדם — באופן שונה.
מה קורה כשמשתקים את המפסל
כדי לבדוק את תפקיד KDM6A, הצוות הוריד את רמותיו בקווי תאים של כבד אנושי ובחולדות ומהונדסים שלא הביטוי של KDM6A רק בהפטוציטים, תאי הכבד העיקריים. בתאי כבד מן תורמת נשית, הורדת KDM6A הורידה בחוזקה את הפעילות של גנים הבונים ומעבדים ליפופרוטאינים, כולל גנים התומכים בליפופרוטאין המגן HDL. אותו מהלך בתאים שמקורם בזכר השפיע על סט שונה של גנים ולא התמקד במסלולי כולסטרול. בעכברים נקבות, אובדן KDM6A בכבד הוביל לפרופיל ליפופרוטאין פרו־אטורוגני: חלקיקי VLDL הפכו עשירים במיוחד בכולסטרול, רמות HDL ירדו והצטברה משקעים שומניים בעורק הראשי, במיוחד כאשר החיות קיבלו תזונה עתירת שומן וכולסטרול וכלי גנטי שמזרז אטרוסקלרוזיס.
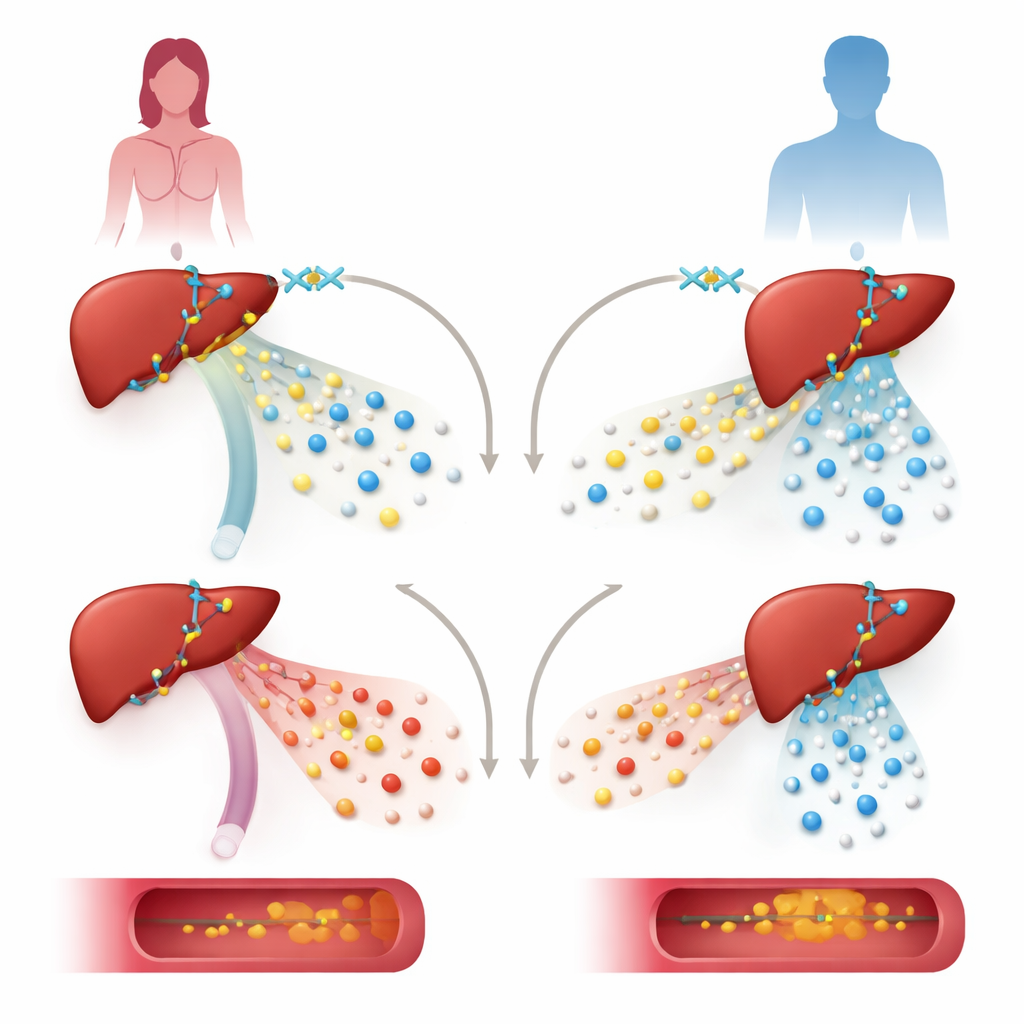
כיצד רשת בקרה של הכבד משתנה
בחפירה עמוקה יותר, החוקרים מיפו היכן KDM6A נקשר ל־DNA וכיצד הוא מתקשר עם רגולטורים אחרים. הם מצאו ש־KDM6A משתף פעולה עם גורם שעתוק מרכזי בכבד, HNF4A, באיזורי בקרה ליד רבים מהגנים של ליפופרוטאינים וכולסטרול, כגון אלו שמייצרים את החלבונים ApoA1, ApoM ו‑ApoH. במקום לפעול בעיקר דרך פונקציית ה"מחק" הכימית הידועה שלו על סימן היסטוני ספציפי, KDM6A כאן מתנהג יותר כשלד מבני. ביחד עם HNF4A ומתחם האנזימים MLL3/4, הוא מסייע ליצירת כרומטין פתוח ופעיל — מבנה DNA‑חלבון רופף — המסומן בדגלים כימיים שמעדיפים פעילות גנטית. הסרת KDM6A החלישה את הסימנים הפעילים האלה ללא עלייה משמעותית בסימנים המעכבים שהוא בדרך כלל מוחק, מה שמעיד על תפקיד מבני ולא אנזימטי.
גורם שלישי מקשר את המפסל לתפוקת הכולסטרול
המחקר גם מזהה שחקן שלישי, CREBH, חלבון תגובת־מתח של הכבד שמגביר ישירות גנים השולטים בטיפול בטריגליצרידים ובכולסטרול. בעזרת מפות קשירה ברחבי הגנום, המחברים מראים שכש־KDM6A חסר, CREBH נקשר בצורה חלשה יותר להרבה מהגנים שאליהם הוא יעד בדרך כלל, המעורבים בייצור חומצות מרה, בפינוי כולסטרול ובהיווצרות HDL. בעכברות חסרות KDM6A בכבד, גנים אלה היו פחות פעילים, חומצות מרה הצטברו בכבד ובדם, וחלקיקי VLDL שהופרשו מהכבד היו בלתי רגיל עשירים בכולסטרול אך יחסית דלים בטריגליצרידים. תפוקה מעוותת זו, בשילוב עם ירידה בגנים הבונים HDL, יצרה תנאים להטמעת כולסטרול מוגברת בדפנות העורקים.
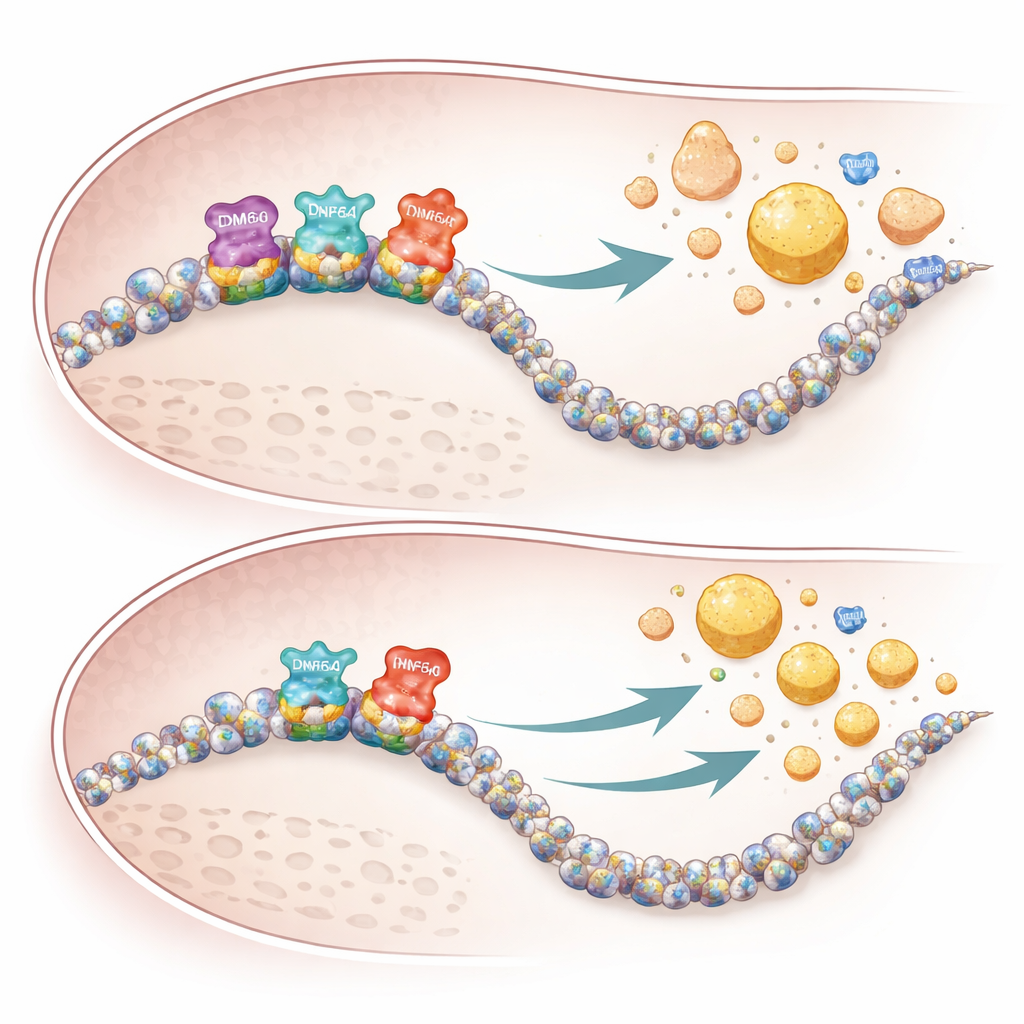
מדוע הנקבות מושפעות יותר
האופי התלוי במין של הממצאים נראה משקף הן גנטיקה והן מערכות גיבוי. כיוון ש־KDM6A מקושר לכרומוזום X ובטוחות ביטוי מוגברות ברקמות נשיות, אובדנו משפיע יותר בנקבות. לזכרים יש גן קרוב על כרומוזום Y, שנקרא KDM6C, שיכול לפצות חלקית בתאי הכבד. בעכברים זכרים, מחיקת KDM6A בהפטוציטים כמעט ולא שינתה פעילות גנטית או דפוסי ליפופרוטאינים, בעוד שמניפולציות דומות בנקבות גרמו לתכנות רחב של מסלולי כולסטרול ולשינויים בולטים בשומני הדם. נתונים גנטיים אנושיים ממאגרי מידע גדולים השמיעו הד תקין: וריאנטים נדירים ב־KDM6A היו קשורים לרמות נמוכות של ApoA1 המועיל ולרמות גבוהות של ApoB הפרו‑אטורוגני באנשים.
מה המשמעות לטיפולים עתידיים
בסך הכל, העבודה חושפת רשת KDM6A–HNF4A–CREBH המקושרת למין שמכווננת כיצד הכבד מארז ומפנה כולסטרול. בנקבות, שיבוש רשת זו מזיז את המאזן לכיוון ליפופרוטאינים שמגבירים סתימות בעורקים, פחות HDL מגן ופינוי כולסטרול המונע על ידי חומצות מרה — כל אלה מקדמים אטרוסקלרוזיס. בהדגשת מרכז בקרה אפיגנטי המשתנה בין המינים, המחקר רומז כי אסטרטגיות להפחתת כולסטרול — ובמיוחד תרופות שפועלות על אנזימים שמשנים כרומטין — עשויות להצטרך להיות מותאמות בנפרד לנשים ולגברים כדי למנוע הזזות בלתי רצויות בפרופיל הליפופרוטאינים.
ציטוט: Chen, L., Kang, Z., Härdfeldt, J. et al. Sex-specific KDM6A-HNF4A-CREBH network controls lipoprotein cholesterol metabolism and atherosclerosis via epigenetic reprograming of hepatocytes. Nat Commun 17, 3945 (2026). https://doi.org/10.1038/s41467-026-70846-w
מילות מפתח: מטבוליזם של כולסטרול, אפיגנטיקה של הכבד, ליפופרוטאינים, הבדלים בין המינים, אטורוסקלרוזיס