Clear Sky Science · de
Sex-spezifisches KDM6A-HNF4A-CREBH-Netzwerk steuert Lipoprotein‑Cholesterinstoffwechsel und Atherosklerose über epigenetische Umprogrammierung von Hepatozyten
Warum diese Forschung für die Herzgesundheit wichtig ist
Herzinfarkte und Schlaganfälle beginnen häufig mit langsamen Veränderungen darin, wie die Leber mit Cholesterin umgeht. Es ist bekannt, dass Männer und Frauen sich in ihren Cholesterinwerten und im Risiko für verstopfte Arterien unterscheiden, die zugrunde liegenden Ursachen werden aber noch erforscht. Diese Studie zeigt ein geschlechtsgebundenes Kontrollsystem in Leberzellen, das hilft, Blutfette in einem gesünderen Bereich zu halten, besonders bei Frauen. Das Verständnis dieses Systems könnte Wege zu personalisierteren Behandlungen für hohen Cholesterinspiegel und Atherosklerose aufzeigen.
Ein Leber-Schalter auf dem X‑Chromosom
Im Mittelpunkt dieser Arbeit steht ein Protein namens KDM6A, das von einem Gen auf dem X‑Chromosom hergestellt wird. KDM6A transportiert kein Cholesterin; stattdessen wirkt es im Zellkern als Teil der Maschinerie, die entscheidet, welche Gene an- oder abgeschaltet werden. Weil es auf dem X‑Chromosom liegt und der üblichen Inaktivierung eines X bei Frauen entkommen kann, kann seine Aktivität zwischen Frauen und Männern variieren. Die Autoren fragten, ob dieser Unterschied helfen kann zu erklären, warum die beiden Geschlechter Cholesterin und Lipoproteine — die fetttransportierenden Partikel im Blut — unterschiedlich handhaben.
Was passiert, wenn der Schalter heruntergedreht wird
Um die Rolle von KDM6A zu testen, reduzierte das Team dessen Menge in menschlichen Leberzelllinien und in Mäusen, bei denen KDM6A nur in Hepatozyten fehlte, den wichtigsten Leberzellen. In Leberzellen einer weiblichen Spenderin führte die Herunterregulierung von KDM6A zu einer starken Abnahme der Aktivität von Genen, die Lipoproteine aufbauen und verarbeiten, einschließlich Genen, die schützendes High‑Density‑Lipoprotein (HDL) unterstützen. Dieselbe Manipulation in Zellen männlicher Herkunft betraf eine andere Gruppe von Genen und zielte nicht vorrangig auf Cholesterinwege ab. In weiblichen Mäusen führte der Verlust von KDM6A in der Leber zu einem stärker „atherogenen“ Lipoproteinmuster: Very‑low‑density‑Lipoproteine (VLDL) wurden ungewöhnlich reich an Cholesterin, HDL‑Spiegel sanken und Fettablagerungen in der Hauptarterie nahmen zu — besonders wenn die Tiere mit einer fettreichen, cholesterinreichen Diät und einem atherosklerosefördernden genetischen Tool belastet wurden.
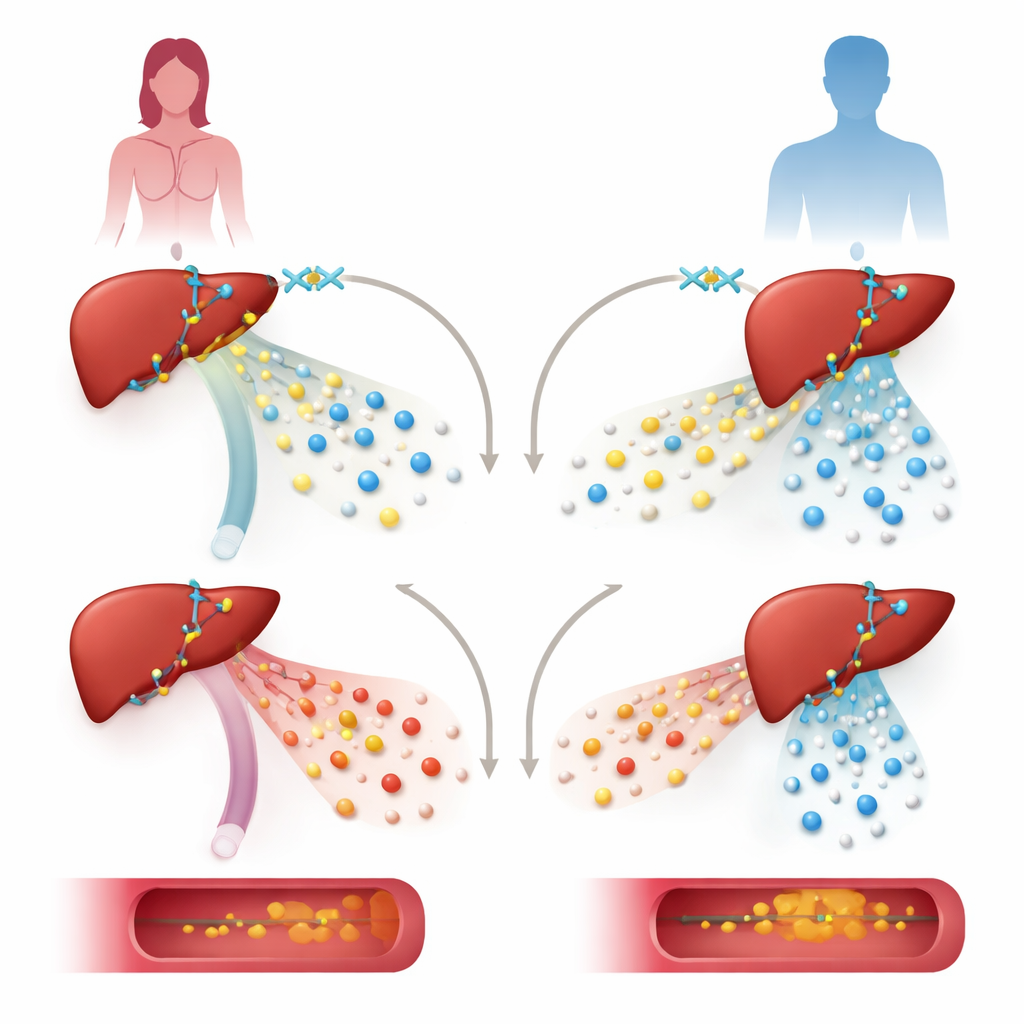
Wie das Genregulationsnetz der Leber umverdrahtet wird
Bei genauerer Untersuchung kartierten die Forschenden, wie KDM6A auf der DNA sitzt und mit anderen Regulatoren interagiert. Sie fanden, dass KDM6A mit einem wichtigen Leber-Transkriptionsfaktor, HNF4A, an Kontrollregionen in der Nähe vieler Lipoprotein‑ und Cholesterin‑Gene zusammenarbeitet, etwa jener, die die Proteine ApoA1, ApoM und ApoH herstellen. Anstatt hauptsächlich über seine bekannte chemische „Radierfunktion“ auf eine bestimmte Histonmarke zu wirken, agiert KDM6A hier eher als Gerüst. Zusammen mit HNF4A und einem Enzymkomplex namens MLL3/4 hilft es, offene, aktive Chromatinzustände zu erzeugen — locker verpackte DNA‑Protein‑Strukturen — die durch bestimmte chemische Kennzeichen Genaktivität begünstigen. Das Entfernen von KDM6A schwächte diese aktiven Markierungen, ohne die repressive Markierung, die es üblicherweise entfernt, stark zu erhöhen, was auf eine nicht‑enzymatische, strukturelle Rolle hinweist.
Ein dritter Akteur verbindet den Schalter mit der Cholesterinausgabe
Die Studie identifiziert außerdem einen dritten Faktor, CREBH, ein in der Leber stressreaktives Protein, das die Gene für Triglycerid‑ und Cholesterinverarbeitung direkt verstärkt. Mit genomweiten Bindungskarten zeigen die Autoren, dass CREBH bei Verlust von KDM6A an vielen seiner üblichen Zielgene — etwa solche für Gallensäureproduktion, Cholesterinabbau und HDL‑Bildung — schwächer bindet. In weiblichen Mäusen ohne hepatisches KDM6A waren diese Gene weniger aktiv, Gallensäuren häuften sich in Leber und Blut an, und VLDL‑Partikel verließen die Leber ungewöhnlich cholesterinreich, aber relativ arm an Triglyceriden. Diese verzerrte Ausgabe, kombiniert mit reduzierten HDL‑aufbauenden Genen, bereitete den Boden für mehr Cholesterinablagerungen in den Arterienwänden.
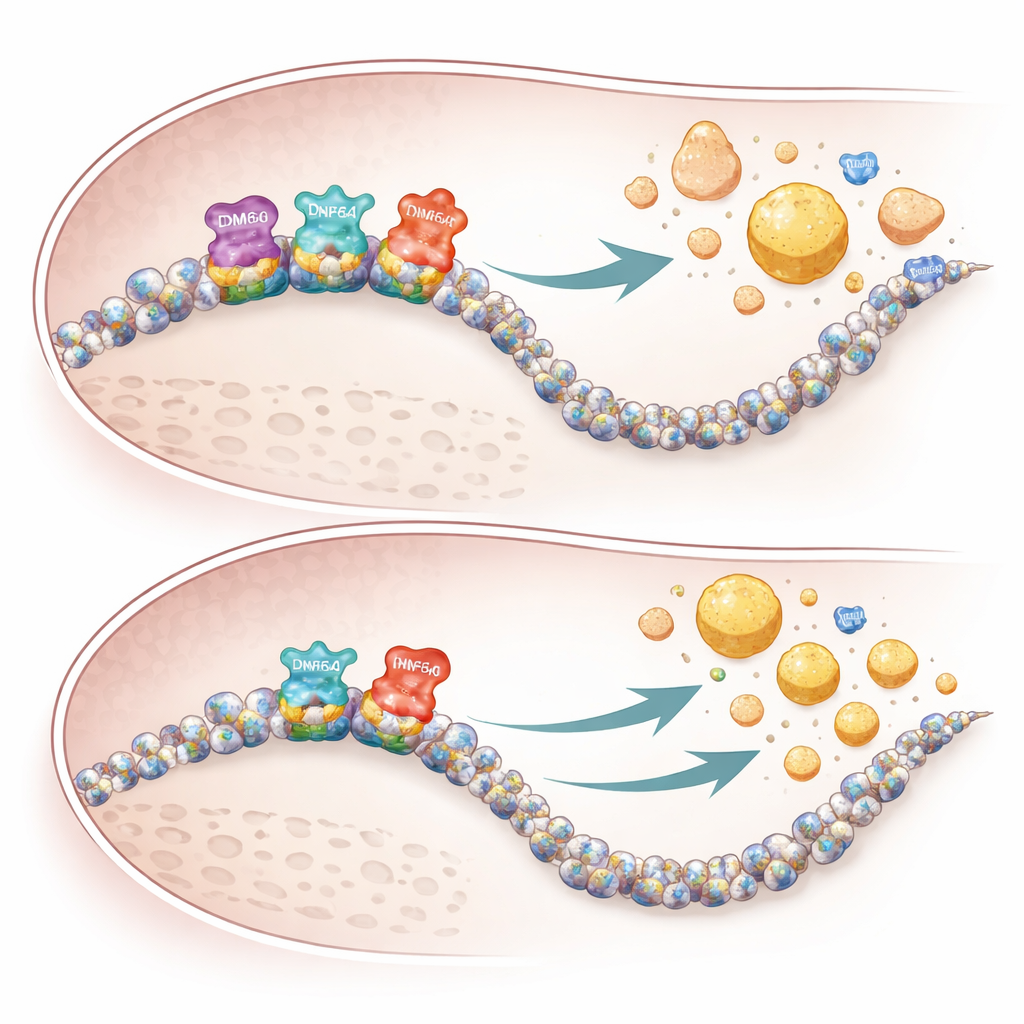
Warum Frauen stärker betroffen sind
Die geschlechtsspezifische Natur der Befunde scheint sowohl Genetik als auch Kompensationsmechanismen widerzuspiegeln. Weil KDM6A X‑gebunden ist und in weiblichen Geweben stärker exprimiert wird, hat sein Verlust eine größere Auswirkung bei Frauen. Männer tragen ein verwandtes Gen auf dem Y‑Chromosom, KDM6C, das in Hepatozyten teilweise kompensieren kann. Beim Löschen von KDM6A in männlichen Mäusen veränderten sich Genaktivität und Lipoproteinprofile kaum, während ähnliche Manipulationen bei weiblichen Tieren zu einer weitreichenden Umprogrammierung von Cholesterinwegen und auffälligen Veränderungen der Blutlipide führten. Human‑genetische Daten aus großen Datenbanken spiegelten diese Muster: Seltene KDM6A‑Varianten waren mit niedrigeren Spiegeln des nützlichen ApoA1 und höheren Spiegeln des atherogenen ApoB beim Menschen assoziiert.
Was das für künftige Therapien bedeutet
Insgesamt zeigt die Arbeit ein geschlechtsgebundenes KDM6A–HNF4A–CREBH‑Netzwerk, das feinjustiert, wie die Leber Cholesterin verpackt und entsorgt. Bei Frauen verschiebt die Störung dieses Netzwerks das Gleichgewicht zugunsten von arterienverstopfenden Lipoproteinen, weniger schützendem HDL und beeinträchtigter gallensäuregetriebener Cholesterinausscheidung — alles Faktoren, die die Atherosklerose fördern. Indem die Studie ein epigenetisches Kontrollzentrum aufzeigt, das sich zwischen den Geschlechtern unterscheidet, legt sie nahe, dass künftige cholesterinsenkende Strategien — und Medikamente, die chromatinmodifizierende Enzyme anvisieren — womöglich geschlechtsspezifisch angepasst werden müssen, um unerwünschte Verschiebungen der Lipoproteinprofile zu vermeiden.
Zitation: Chen, L., Kang, Z., Härdfeldt, J. et al. Sex-specific KDM6A-HNF4A-CREBH network controls lipoprotein cholesterol metabolism and atherosclerosis via epigenetic reprograming of hepatocytes. Nat Commun 17, 3945 (2026). https://doi.org/10.1038/s41467-026-70846-w
Schlüsselwörter: Cholesterinstoffwechsel, Leberepigenetik, Lipoproteine, Geschlechtsunterschiede, Atherosklerose