Clear Sky Science · sv
REDD1–NF-κB–miRNAs–eNOS/SIRT1-axeln medierar fetmainducerad endotelcellsenescens och hypertoni
Varför våra blodkärl åldras snabbare vid fetma
Det är välkänt att fetma ökar risken för högt blodtryck, hjärtinfarkt och stroke, men exakt hur överskottsfett gör våra blodkärl gamla och stela har varit oklart. Denna studie avslöjar en molekylär "konversation" i det tunna cellskiktet som klär artärerna och visar hur metabol stress från fetma kan få dessa celler att åldras i förtid, skada njurarna och driva fram hypertoni. Att förstå denna händelsekedja pekar ut nya, mycket specifika måltavlor för läkemedel som kan skydda blodkärlen hos personer med fetma.
Den dolda belastningen på kärlskinnets celler
Det innersta skiktet i blodkärlen består av endotelceller, som fungerar som grindvakter för blodflöde, kärlavslappning och inflammation. Vid fetma stiger nivåerna av fettsyror, kolesterol, socker och hormonsignaler i blodet. Forskarna gav möss en fettrik diet för att efterlikna detta tillstånd och behandlade mänskliga endotelceller med fetmarelaterade faktorer som palmitinsyra, oxiderat LDL, hög glukos, leptin och resistin. Dessa förhållanden fick cellerna att uppvisa klassiska tecken på senescens, ett tillstånd av permanent tillväxtstopp där celler slutar dela sig, ansamlar avfallsprodukter och frisätter inflammatoriska ämnen. Hos mössen utvecklade aortan — huvudartären från hjärtat — fläckar av åldrande endotelceller och förlorade förmågan att slappna av ordentligt, vilket bidrog till förhöjt blodtryck.
En stressensor som skjuter celler in i ålderdom
Teamet fokuserade på ett stresskänsligt protein kallat REDD1, som aktiveras av metabolisk och oxidativ stress. De fann att metabola riskfaktorer kraftigt ökade REDD1-nivåerna i odlade mänskliga och musendotelceller och i artärerna hos feta möss. När REDD1 experimentellt ökades i blodkärl blev endotelceller snabbt senescenta, kväveoxidproduktionen sjönk och artärerna stelnade, vilket drev fram hypertoni. I kontrast orsakade inte en muterad form av REDD1 som inte längre kunde signalera via en nyckelinflammatorisk väg dessa problem. Möss som genetiskt saknade REDD1, eller saknade REDD1 specifikt i sina endotelceller, var i stort sett skyddade: deras artärer visade färre senescenta celler, högre nivåer av skyddande molekyler, bättre kärlavslappning och lägre blodtryck trots fetma.
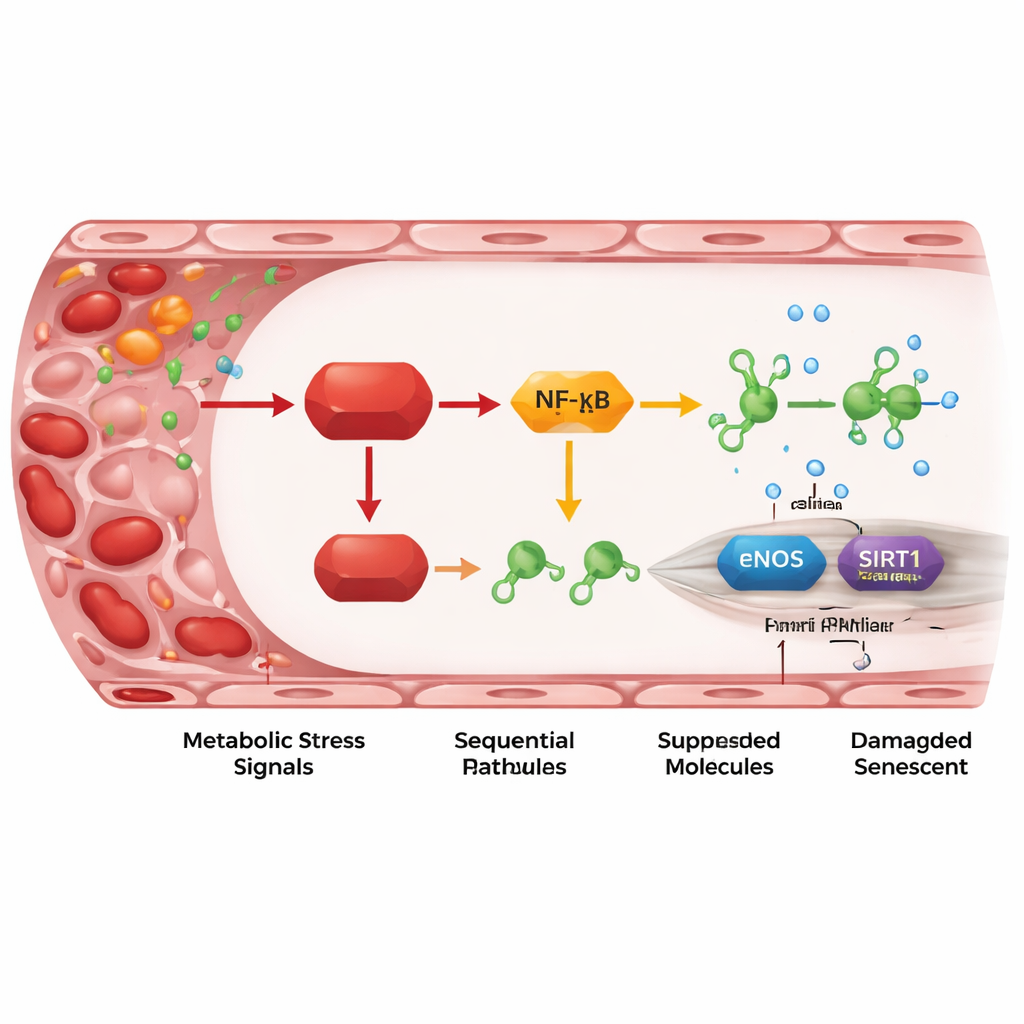
En inflammatorisk reläkedja från REDD1 till skyddande gener
Genom att gå djupare kartlade forskarna en kedja av molekylära steg som länkar REDD1 till vaskulär skada. REDD1 aktiverar en "atypisk" variant av NF-κB-vägen, en huvudregulator för inflammation. Detta höjer i sin tur nivåerna av två små regulatoriska RNA, miR-155-5p och särskilt miR-214-3p. Dessa mikroRNA fungerar som små bromsar på två skyddande proteiner i endotelceller: eNOS, som producerar kväveoxid för att slappna av kärlen, och SIRT1, som hjälper till att bevara cellernas ungdomlighet och DNA-stabilitet. När REDD1 var högt steg mikroRNA-nivåerna, eNOS och SIRT1 sjönk, kväveoxidproduktionen minskade och markörer för senescens ökade. Att blockera mikroRNA eller öka SIRT1 eller kväveoxid kunde återställa mycket av skadan, vilket visar att denna axel inte bara är associerad med utan faktiskt driver åldringsprocessen i kärlväggen.
Bevis från genetiska modeller och njurpåverkan
Flera musmodeller gjorde det möjligt för författarna att testa varje steg i denna axel i levande djur. Feta möss som saknade REDD1, uttryckte den icke-signaliserande REDD1-mutanten eller var konstruerade för att ta bort REDD1 endast i endotelceller visade alla minskad arteriell åldrande och lägre blodtryck. Möss som saknade miR-214-3p var likaledes skyddade: även om REDD1 fortfarande ökade vid fetma förblev eNOS och SIRT1 högre, kväveoxidsignaleringen bevarades bättre och vaskulär senescens och hypertoni minskades. Samma REDD1–mikroRNA-väg påverkade njurarna, organ som är avgörande för långtidskontroll av blodtrycket. Hos feta vildtypmöss förstorades njurarna, blev fibrotiska och läckte mer kreatinin till blodet. Dessa tecken på njurskada var mycket mildare hos möss som saknade REDD1, saknade endotelial REDD1 eller saknade miR-214-3p, vilket tyder på att skydd av blodkärlen också hjälpte till att bevara njurfunktionen.
Vad detta betyder för framtida behandlingar
För en lekmannabetraktare visar detta arbete att fetma inte bara höjer blodtrycket genom extra kroppsmassa; det omprogrammerar biologin i kärlskiktet på djupet. Studien identifierar en nyckelkedja av bovar — REDD1, atypisk NF-κB-signalering och mikroRNA miR-155-5p och miR-214-3p — som tillsammans slår ner de skyddande eNOS och SIRT1, vilket får blodkärl och njurar att åldras snabbare och ökar blodtrycket. Eftersom varje länk i denna kedja kan förändras i möss för att återställa friskare kärl även efter att fetma etablerats, framträder REDD1–NF-κB–mikroRNA–eNOS/SIRT1-axeln som en lovande ritning för läkemedel inriktade på att förebygga eller behandla fetmarelaterad hypertoni och dess komplikationer.
Citering: Choi, Y.K., Lee, DK., Park, M. et al. The REDD1–NF-κB–miRNAs–eNOS/SIRT1 axis mediates obesity-induced endothelial cell senescence and hypertension. Nat Commun 17, 3843 (2026). https://doi.org/10.1038/s41467-026-70601-1
Nyckelord: fetma, endotelcellsenescens, hypertoni, mikroRNA, kväveoxid