Clear Sky Science · ru
Ось REDD1–NF-κB–микроРНК–eNOS/SIRT1 опосредует старение эндотелия и гипертензию, вызванные ожирением
Почему наши кровеносные сосуды стареют быстрее при ожирении
Ожирение известно тем, что повышает риск высокого артериального давления, инфарктов и инсультов, но то, как именно избыток жира делает сосуды «старыми» и жёсткими, оставалось не вполне ясным. В этом исследовании выявлена молекулярная «переписка» в тонком слое клеток, выстилающем наши артерии, которая показывает, как метаболический стресс при ожирении может преждевременно состарить эти клетки, повредить почки и привести к гипертензии. Понимание этой цепочки событий указывает на новые, очень специфичные мишени для лекарств, которые могли бы защищать сосуды у людей с ожирением.
Скрытая нагрузка на клетки оболочки сосудов
Внутреннюю оболочку кровеносных сосудов составляют эндотелиальные клетки, которые выступают регуляторами кровотока, расслабления сосудов и воспаления. При ожирении в крови повышаются уровни жирных кислот, холестерина, сахара и гормоноподобных сигналов. Авторы кормили мышей высокожировой диетой, чтобы имитировать это состояние, и обрабатывали человеческие эндотелиальные клетки факторами, связанными с ожирением, такими как пальмитиновая кислота, окисленный ЛПНП, высокий глюкозы, лептин и резистин. Эти условия вызвали у клеток типичные признаки сенесценции — состояния постоянной остановки деления, накопления отходов и выделения провоспалительных веществ. У мышей аорта — главный сосуд, выходящий из сердца — развивала участки с постаревшими эндотелиальными клетками и теряла способность правильно расслабляться, что способствовало повышению артериального давления.
Датчик стресса, который переводит клетки в старость
Команда сосредоточилась на стресс-чувствительном белке REDD1, который включается при метаболическом и окислительном стрессе. Они обнаружили, что факторы метаболического риска существенно повышают уровень REDD1 в культивируемых человеческих и мышиных эндотелиальных клетках и в артериях мышей с ожирением. Когда REDD1 экспериментально повышали в сосудах, эндотелиальные клетки быстро переходили в состояние сенесценции, производство оксида азота снижалось, а артерии жестилились, что приводило к гипертензии. Напротив, мутантная форма REDD1, утратившая способность передавать сигнал через ключевой воспалительный путь, не вызывала этих проблем. Мыши, генетически лишённые REDD1, или у которых REDD1 отсутствовал только в эндотелиальных клетках, были в значительной степени защищены: их артерии содержали меньше сенесцентных клеток, уровни защитных молекул были выше, реакция сосудов на расслабление лучше, а кровяное давление ниже несмотря на ожирение.
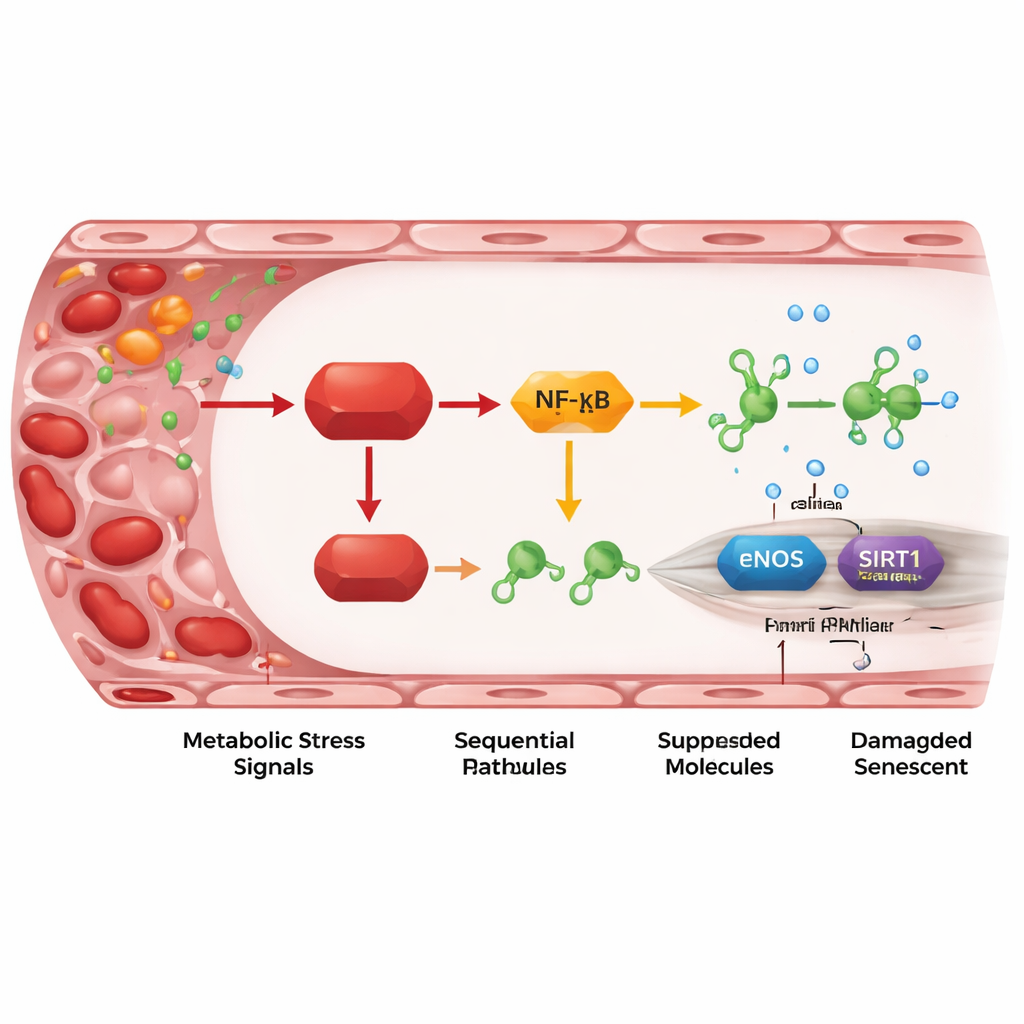
Воспалительная передача от REDD1 к защитным генам
Углубляясь, исследователи проследили каскад молекулярных шагов, связывающих REDD1 с повреждением сосудов. REDD1 активирует «атипичную» версию пути NF-κB, главного регулятора воспаления. Это, в свою очередь, повышает уровни двух маленьких регуляторных РНК — miR-155-5p и особенно miR-214-3p. Эти микроРНК действуют как крошечные «тормоза» для двух защитных белков в эндотелиальных клетках: eNOS, который вырабатывает оксид азота для расслабления сосудов, и SIRT1, который поддерживает молодость клетки и стабильность ДНК. При высоком уровне REDD1 уровни микроРНК повышались, уровни eNOS и SIRT1 падали, выработка оксида азота снижалась, а маркеры сенесценции увеличивались. Блокирование микроРНК или повышение SIRT1 либо оксида азота могло обратить значительную часть повреждений, что показывает: эта ось не просто ассоциирована с процессом старения сосудистой стенки, а непосредственно его вызывает.
Доказательства из генетических моделей и влияние на почки
Несколько моделей мышей позволили авторам проверить каждый шаг этой оси в живых животных. Мыши с ожирением, лишённые REDD1, экспрессирующие неспособный к сигнализации мутант REDD1 или сконструированные так, чтобы удалять REDD1 только в эндотелии, демонстрировали уменьшенное артериальное старение и более низкое давление. Мыши, лишённые miR-214-3p, были аналогично защищены: несмотря на то, что REDD1 при ожирении всё ещё повышался, eNOS и SIRT1 оставались на более высоком уровне, сигналы оксида азота были лучше сохранены, а сосудистая сенесценция и гипертензия были ослаблены. Та же путь REDD1–микроРНК затрагивал почки — органы, критичные для долгосрочного контроля артериального давления. У ожиревших животных диких линий почки увеличивались, становились более фиброзными и пропускали в кровь больше креатинина. Эти признаки почечного повреждения были значительно мягче у мышей, лишённых REDD1, с эндотелиальным удалением REDD1 или без miR-214-3p, что указывает на то, что защита сосудов также помогает сохранять функцию почек.
Что это значит для будущих терапий
Для непрофессионала эта работа показывает: ожирение повышает давление не просто за счёт лишней массы тела; оно глубоко перепрограммирует биологию сосудистой оболочки. Исследование выделяет ключевую цепочку виновников — REDD1, атипичный NF-κB и микроРНК miR-155-5p и miR-214-3p — которые совместно подавляют защитные eNOS и SIRT1, заставляя сосуды и почки стареть быстрее и повышая давление. Поскольку каждое звено этой цепи можно изменить у мышей с восстановлением здорового состояния сосудов даже после развития ожирения, ось REDD1–NF-κB–микроРНК–eNOS/SIRT1 выступает как перспективная схема для разработки препаратов, направленных на профилактику или лечение гипертензии, связанной с ожирением, и её осложнений.
Цитирование: Choi, Y.K., Lee, DK., Park, M. et al. The REDD1–NF-κB–miRNAs–eNOS/SIRT1 axis mediates obesity-induced endothelial cell senescence and hypertension. Nat Commun 17, 3843 (2026). https://doi.org/10.1038/s41467-026-70601-1
Ключевые слова: ожирение, старение эндотелия, гипертензия, микроРНК, оксид азота