Clear Sky Science · pt
O eixo REDD1–NF-κB–miRNAs–eNOS/SIRT1 media a senescência endotelial e a hipertensão induzidas pela obesidade
Por que nossos vasos sanguíneos envelhecem mais rápido na obesidade
É bem sabido que a obesidade aumenta o risco de pressão alta, infartos e AVCs, mas exatamente como o excesso de gordura torna nossos vasos sanguíneos antigos e rígidos permaneceu obscuro. Este estudo revela uma "conversa" molecular dentro da fina camada de células que reveste as artérias, mostrando como o estresse metabólico da obesidade pode envelhecer essas células precocemente, danificar os rins e provocar hipertensão. Entender essa cadeia de eventos aponta para novos alvos bastante específicos para fármacos que poderiam proteger os vasos sanguíneos em pessoas com obesidade.
A tensão oculta sobre as células do revestimento vascular
O revestimento mais interno dos vasos é formado por células endoteliais, que atuam como guardiãs do fluxo sanguíneo, do relaxamento vascular e da inflamação. Na obesidade, níveis de ácidos graxos, colesterol, glicose e sinais hormonais aumentam na corrente sanguínea. Os autores alimentaram camundongos com dieta rica em gordura para mimetizar esse estado e trataram células endoteliais humanas com fatores relacionados à obesidade, como ácido palmítico, LDL oxidado, glicose alta, leptina e resistina. Essas condições fizeram as células exibirem sinais clássicos de senescência, um estado de parada permanente em que as células deixam de se dividir, acumulam resíduos e liberam substâncias inflamatórias. Nos camundongos, a aorta — a principal artéria que sai do coração — desenvolveu manchas de células endoteliais envelhecidas e perdeu a capacidade de relaxar adequadamente, contribuindo para o aumento da pressão arterial.
Um sensor de estresse que empurra as células para a velhice
A equipe concentrou-se em uma proteína sensível ao estresse chamada REDD1, que é ativada pelo estresse metabólico e oxidativo. Eles descobriram que fatores de risco metabólicos aumentaram fortemente os níveis de REDD1 em células endoteliais humanas e de camundongo em cultura e nas artérias de camundongos obesos. Quando o REDD1 foi aumentado experimentalmente nos vasos, as células endoteliais rapidamente tornaram-se senescentes, a produção de óxido nítrico diminuiu e as artérias se tornaram rígidas, levando à hipertensão. Em contraste, uma forma mutante de REDD1 que não conseguia mais sinalizar através de uma via inflamatória chave deixou de causar esses problemas. Camundongos geneticamente sem REDD1, ou sem REDD1 especificamente em suas células endoteliais, ficaram em grande parte protegidos: suas artérias mostraram menos células senescentes, níveis mais altos de moléculas protetoras, melhor relaxamento vascular e pressão arterial menor apesar da obesidade.
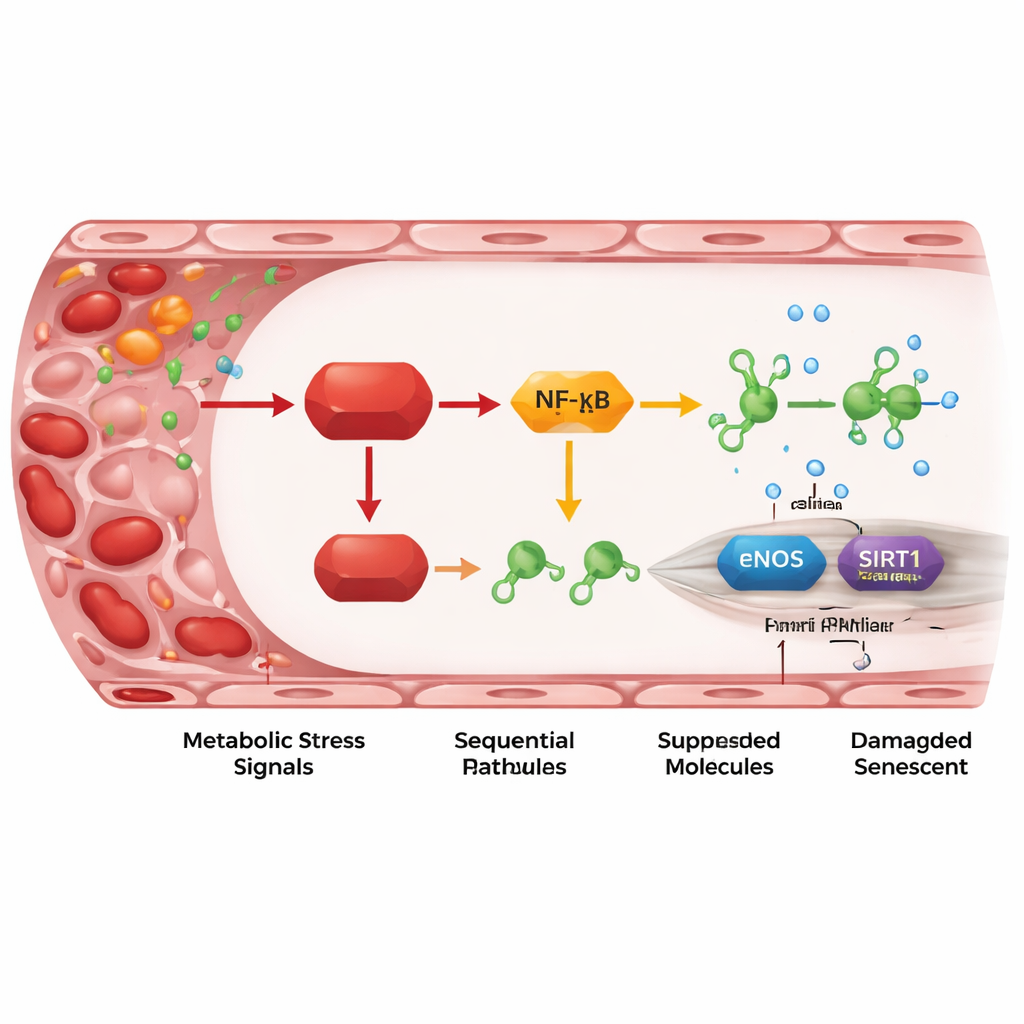
Um revezamento inflamatório do REDD1 até genes protetores
Ao aprofundar, os pesquisadores mapearam um revezamento de etapas moleculares ligando o REDD1 ao dano vascular. O REDD1 ativa uma versão "atípica" da via NF-κB, um controlador mestre da inflamação. Isso, por sua vez, eleva os níveis de dois pequenos RNAs regulatórios, miR-155-5p e, especialmente, miR-214-3p. Esses microRNAs atuam como pequenos freios em duas proteínas protetoras nas células endoteliais: eNOS, que produz óxido nítrico para relaxar os vasos, e SIRT1, que ajuda a manter a juventude celular e a estabilidade do DNA. Quando o REDD1 estava alto, os níveis dos microRNAs aumentaram, eNOS e SIRT1 diminuíram, a produção de óxido nítrico caiu e os marcadores de senescência aumentaram. Bloquear os microRNAs ou aumentar a SIRT1 ou o óxido nítrico pôde reverter grande parte do dano, mostrando que esse eixo não está apenas associado, mas realmente dirige o processo de envelhecimento na parede do vaso.
Provas a partir de modelos genéticos e efeitos renais
Vários modelos de camundongo permitiram aos autores testar cada etapa desse eixo em animais vivos. Camundongos obesos sem REDD1, expressando o mutante REDD1 sem capacidade de sinalização, ou projetados para deletar REDD1 apenas nas células endoteliais, mostraram redução do envelhecimento arterial e pressão arterial mais baixa. Camundongos que não tinham miR-214-3p foram protegidos de forma semelhante: embora o REDD1 ainda aumentasse com a obesidade, eNOS e SIRT1 permaneceram mais altos, a sinalização do óxido nítrico foi melhor preservada e a senescência vascular e a hipertensão foram atenuadas. A mesma via REDD1–microRNA afetou os rins, órgãos cruciais para o controle da pressão arterial a longo prazo. Em camundongos obesos do tipo selvagem, os rins aumentaram de tamanho, tornaram-se fibróticos e vazaram mais creatinina para o sangue. Esses sinais de dano renal foram muito mais leves em camundongos sem REDD1, sem REDD1 endotelial ou sem miR-214-3p, sugerindo que proteger os vasos também ajudou a salvaguardar a função renal.
O que isso significa para terapias futuras
Para um observador leigo, este trabalho mostra que a obesidade não apenas eleva a pressão arterial pelo aumento de massa corporal; ela reprograma a biologia do revestimento vascular em um nível profundo. O estudo identifica uma cadeia chave de culpados — REDD1, sinalização atípica de NF-κB e os microRNAs miR-155-5p e miR-214-3p — que juntos desligam eNOS e SIRT1 protetores, fazendo com que vasos sanguíneos e rins envelheçam mais rápido e elevem a pressão arterial. Como cada elo dessa cadeia pode ser alterado em camundongos para restaurar vasos mais saudáveis mesmo após o estabelecimento da obesidade, o eixo REDD1–NF-κB–microRNA–eNOS/SIRT1 surge como um roteiro promissor para fármacos destinados a prevenir ou tratar a hipertensão ligada à obesidade e suas complicações.
Citação: Choi, Y.K., Lee, DK., Park, M. et al. The REDD1–NF-κB–miRNAs–eNOS/SIRT1 axis mediates obesity-induced endothelial cell senescence and hypertension. Nat Commun 17, 3843 (2026). https://doi.org/10.1038/s41467-026-70601-1
Palavras-chave: obesidade, senescência endotelial, hipertensão, microRNA, óxido nítrico