Clear Sky Science · ar
محور REDD1–NF-κB–الـmiRNAs–eNOS/SIRT1 يتوسط شيخوخة الخلايا البطانية وارتفاع ضغط الدم الناجمين عن السمنة
لماذا تتقدم أوعيتنا الدموية أسرع في السمنة
من المعروف أن السمنة ترفع خطر الإصابة بارتفاع ضغط الدم والنوبات القلبية والسكتات الدماغية، لكن كيفية جعل الدهون الزائدة أوعيتنا الدموية تتقدم في السن وتصبح متصلبة ظلّت غير واضحة. تكشف هذه الدراسة عن «حوار» جزيئي داخل الطبقة الرقيقة التي تبطّن شراييننا، موضحة كيف يمكن للإجهاد الأيضي الناجم عن السمنة أن يهرم هذه الخلايا مبكراً، ويُتلف الكليتين، ويُسرِّع ارتفاع ضغط الدم. وفهم سلسلة الأحداث هذه يشير إلى أهداف دوائية جديدة ومحددة قد تحمي الأوعية الدموية لدى الأشخاص المصابين بالسمنة.
الإجهاد الخفي على خلايا بطانة الأوعية
البطانة الداخلية للأوعية الدموية مكوَّنة من خلايا بطانية تعمل كحارسات لتدفق الدم واسترخاء الأوعية والالتهاب. في السمنة ترتفع مستويات الأحماض الدهنية والكوليسترول والسكر والإشارات الهرمونية في مجرى الدم. أطعمت الباحثون الفئران بنظام غذائي عالي الدسم لمحاكاة هذه الحالة وعالجوا خلايا بطانية بشرية بعوامل مرتبطة بالسمنة مثل حمض بالميتات، LDL المؤكسد، الجلوكوز العالي، اللبتين، والريزينتين. أدت هذه الظروف إلى إظهار الخلايا لعلامات كلاسيكية للشيخوخة الخلوية (السِنِنة)، وهي حالة توقّف دائم تتوقف فيها الخلايا عن الانقسام وتراكم الفضلات وتفرز مواد التهابية. في الفئران، طورت الأبهر —الشريان الرئيسي الخارج من القلب— رقعاً من الخلايا البطانية المسنة وفقدت قدراتها على الاسترخاء بشكل صحيح، ما ساهم في زيادة ضغط الدم.
مستشعر إجهاد يدفع الخلايا إلى الشيخوخة
ركز الفريق على بروتين استشعاري للإجهاد يدعى REDD1، يتم تشغيله بواسطة الإجهاد الأيضي والأكسدي. وجدوا أن عوامل المخاطر الأيضية رفعت مستويات REDD1 بشدة في خلايا بطانية بشرية وفأرية مزروعة وفي شرايين الفئران المصابة بالسمنة. عندما زادوا REDD1 تجريبياً في الأوعية الدموية، أصبحت الخلايا البطانية مسنة بسرعة، انخفض إنتاج أكسيد النيتريك، وتصلبت الشرايين مما دفع نحو ارتفاع ضغط الدم. بالمقابل، لم يتسبب شكل طفري من REDD1 غير القادر على الإشارة عبر مسار التهابي رئيسي في هذه المشاكل. الفئران التي تفتقر جينياً إلى REDD1، أو تفتقر إلى REDD1 تحديداً في خلاياها البطانية، كانت محمية إلى حد كبير: أظهرت شرايينها خلايا مسنة أقل ومستويات أعلى من الجزيئات الواقية، وتحسناً في استرخاء الأوعية وانخفاضاً في ضغط الدم رغم السمنة.
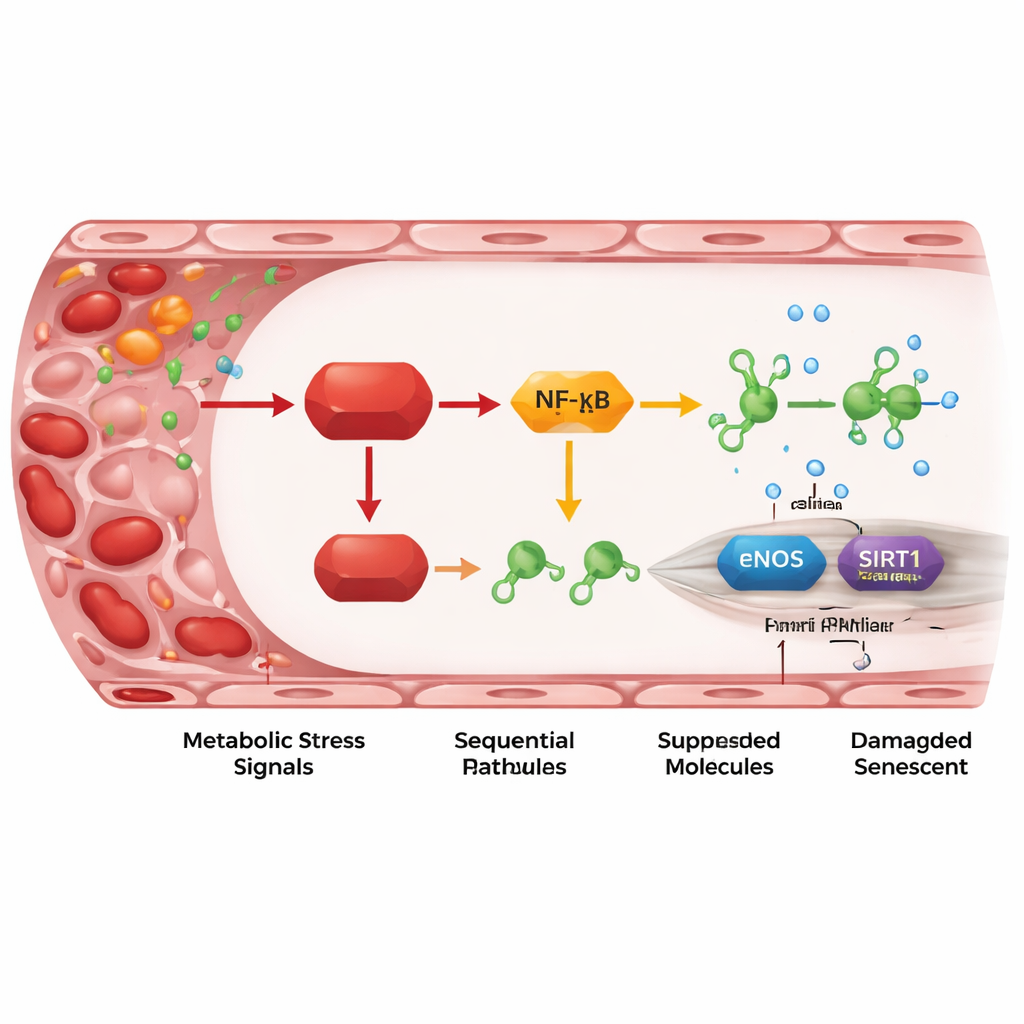
تتابع التهابي من REDD1 إلى الجينات الواقية
بالغوص أعمق، رسم الباحثون خريطة لخطوات جزيئية تربط REDD1 بالضرر الوعائي. يُفعِّل REDD1 نسخة «غير اعتيادية» من مسار NF-κB، وهو المتحكم الرئيسي في الالتهاب. هذا بدوره يرفع مستويات اثنين من الحمضيات الريبية التنظيمية الصغيرة، miR-155-5p وخصوصاً miR-214-3p. تعمل هذه الميكروRNAs ككوابح صغيرة على بروتينين واقيين في الخلايا البطانية: eNOS الذي ينتج أكسيد النيتريك لاسترخاء الأوعية، وSIRT1 الذي يساعد في الحفاظ على حيوية الخلايا واستقرار الحمض النووي. عندما كان REDD1 مرتفعاً، ارتفعت مستويات الميكروRNA، وانخفضت مستويات eNOS وSIRT1، وتراجع إنتاج أكسيد النيتريك، وازداد ظهور مؤشرات الشيخوخة. إيقاف عمل هذه الميكروRNA أو تعزيز SIRT1 أو أكسيد النيتريك أمكن أن يعكس كثيراً من الضرر، مما يدل على أن هذا المحور ليس مجرد مرتبط بالشيخوخة الوعائية بل هو محرك فعلي للعملية.
دليل من النماذج الجينية وتأثيرات على الكلية
أتاحت عدة نماذج فئران للباحثين اختبار كل خطوة من هذا المحور في حيوانات حية. أظهرت الفئران المصابة بالسمنة التي تفتقر إلى REDD1، أو تُعبّر شكل REDD1 غير المرسل، أو مُعدّة لحذف REDD1 فقط في الخلايا البطانية، تقلصاً في شيخوخة الشرايين وانخفاضاً في ضغط الدم. كانت الفئران الخالية من miR-214-3p محمية بالمثل: على الرغم من ارتفاع REDD1 مع السمنة، بقيت مستويات eNOS وSIRT1 أعلى، وحُفظت إشارة أكسيد النيتريك بشكل أفضل، وتلاشت شيخوخة الأوعية وارتفاع ضغط الدم. أثَّر نفس مسار REDD1–الميكروRNA أيضاً على الكليتين، وهما عضوان حاسمان في التحكم طويل الأمد في ضغط الدم. في الفئران البرية المصابة بالسمنة، تَضخَّمت الكليتان، وأصابتهما ليفية، وتسربت المزيد من الكرياتينين إلى الدم. كانت علامات الضرر الكلوي هذه أخف بكثير في الفئران التي تفتقر إلى REDD1 أو إلى REDD1 البطاني أو إلى miR-214-3p، مما يشير إلى أن حماية الأوعية الدموية ساهمت أيضاً في حفظ وظيفة الكلية.
ماذا يعني هذا للعلاجات المستقبلية
للمشاهد العادي، تُبيّن هذه الدراسة أن السمنة لا ترفع ضغط الدم ببساطة عبر زيادة الكتلة الجسمية؛ بل تعيد برمجة بيولوجيا بطانة الأوعية على مستوى عميق. تحدد الدراسة سلسلة من المذنبات الرئيسية—REDD1، إشارة NF-κB غير الاعتيادية، والميكروRNAs miR-155-5p وmiR-214-3p—التي معاً تُعطّل eNOS وSIRT1 الوقائيين، مسببةً تسريع شيخوخة الأوعية والكليتين ورفع ضغط الدم. وبما أن كل حلقة في هذه السلسلة يمكن تعديلها في الفئران لاستعادة أوعية أكثر صحة حتى بعد حدوث السمنة، يبرز محور REDD1–NF-κB–الميكروRNA–eNOS/SIRT1 كخارطة واعدة لتطوير أدوية تهدف إلى الوقاية أو العلاج من ارتفاع ضغط الدم المرتبط بالسمنة ومضاعفاته.
الاستشهاد: Choi, Y.K., Lee, DK., Park, M. et al. The REDD1–NF-κB–miRNAs–eNOS/SIRT1 axis mediates obesity-induced endothelial cell senescence and hypertension. Nat Commun 17, 3843 (2026). https://doi.org/10.1038/s41467-026-70601-1
الكلمات المفتاحية: السمنة, شيخوخة الخلايا البطانية, ارتفاع ضغط الدم, الميكروRNA, أكسيد النيتريك